14.【図解】電子配置の書き方攻略!炭素・窒素・鉄を「ホテルの入居ルール」で3分マスター

※本記事にはアフィリエイトリンクが含まれる可能性があります。
こんにちは! 
生化学の勉強を頑張っている皆さん、
今日も本当にお疲れさまです。
なぜ鉄剤で貧血🩸が治るのか。
その答えは、教科書の隅にある電子配置『4sと3dの逆転』に隠されています。
ただのひっかけ問題だと思ってたのに、実は臨床の面白さを理解するためのカギ🔑だったりするのです。
電子を”ホテルの宿泊客🏨”に例えて、1秒で納得できる『生きた化学』を学びましょう。
📚 目次


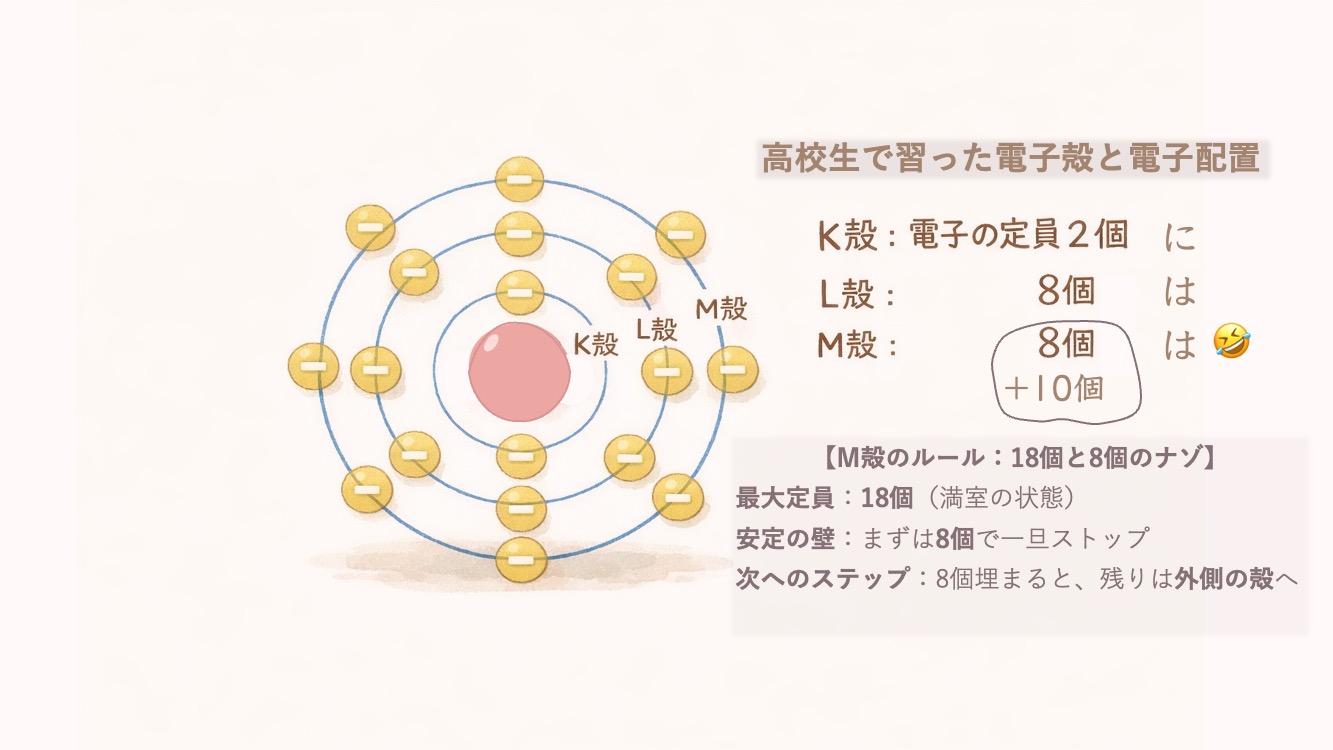
KLM殻・spdf軌道については、こちらの記事をよんでね。
👉 【図解】電子配置は「ホテル」でわかる!KLM殻とspdf軌道のきほん
1. 電子が入る順番(エネルギーのルール)
▲目次へ
電子(お客さん)は、原子核に近い「安くて居心地がいい部屋」から順番に埋めていきます。
1s → 2s → 2p → 3s → 3p → 4s …
2階よりも1階の方が、階段を登らなくていいよね。
お部屋タイプsは、丸くて居心地がいいんだ。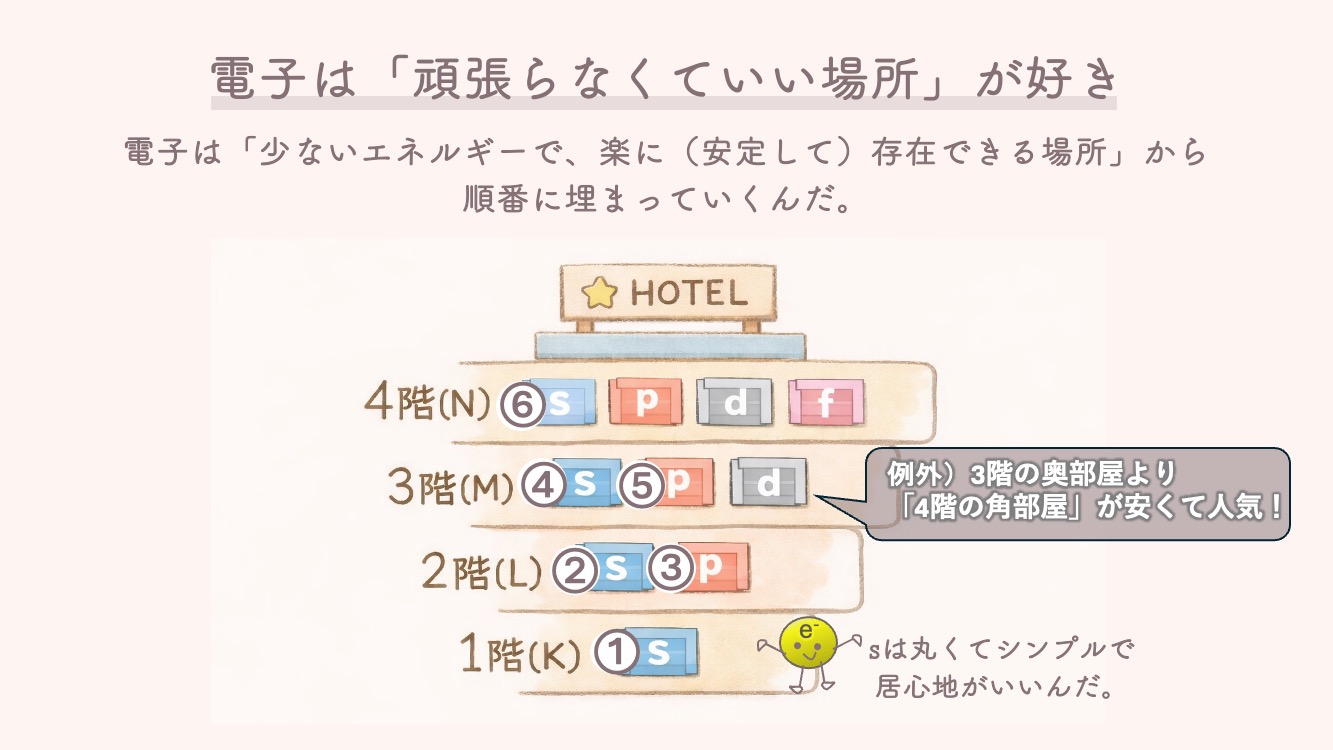
それでは、各お部屋(軌道)を詳しく紹介しましょう。
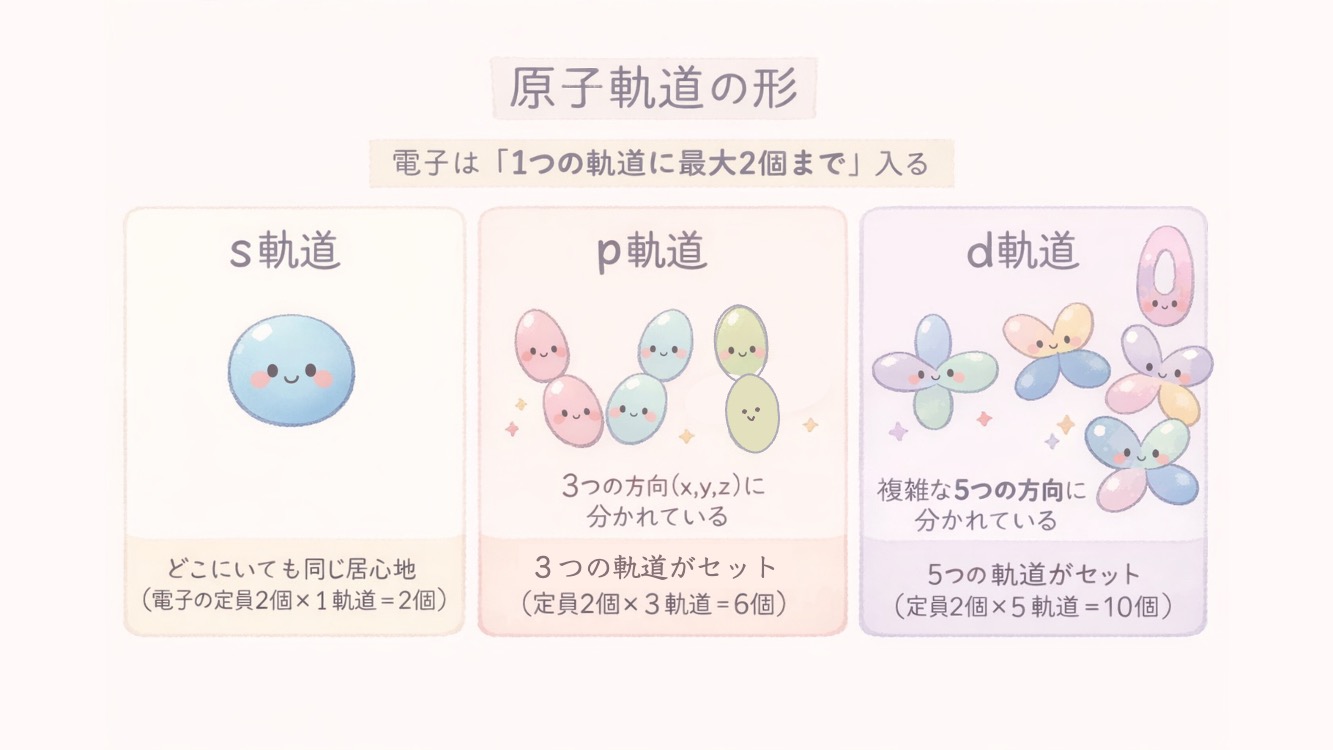
それぞれの軌道に入れる電子の数は?
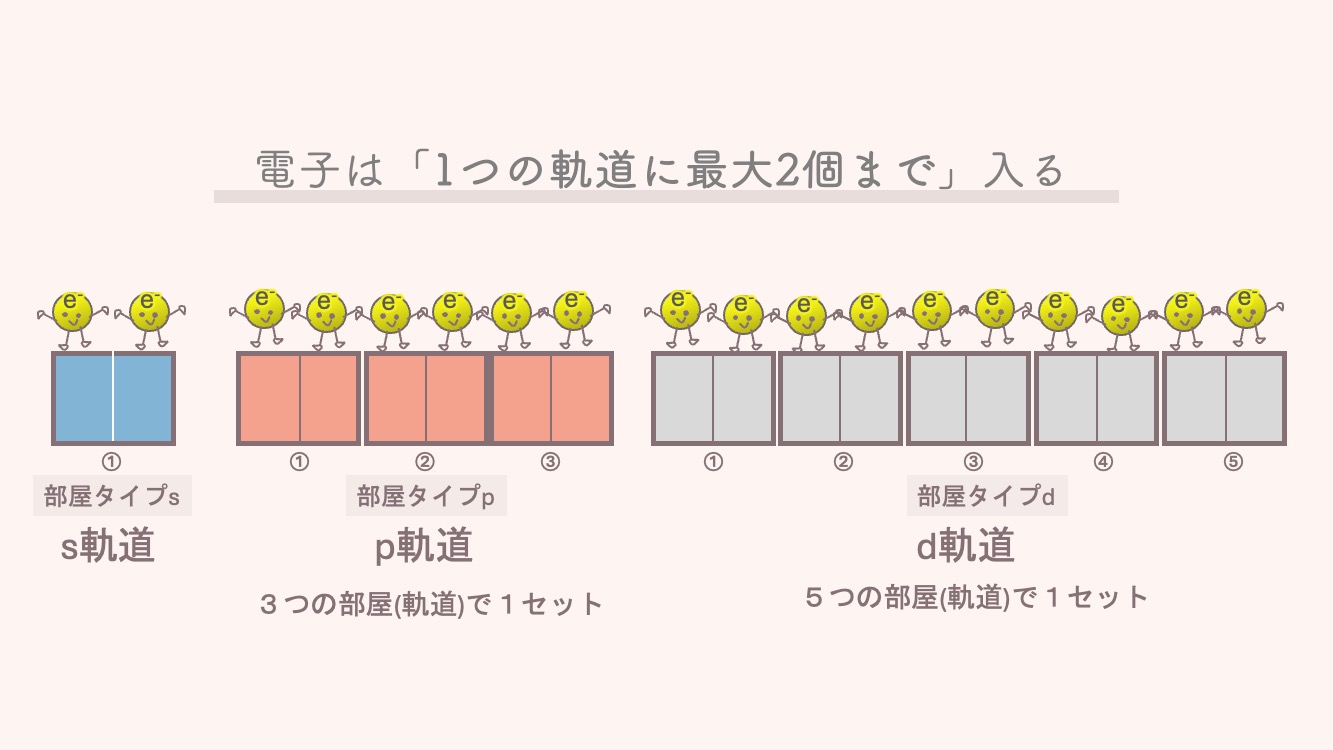
ではいよいよ!順番に電子を入れていくよ。
ここで大事な規則が登場する。フントの規則だよ。
💡 フントの規則: 電子は仲が悪いので、同じ階なら「まずは1人ずつ」別々の部屋に入ります。満員になって初めて相部屋になります。
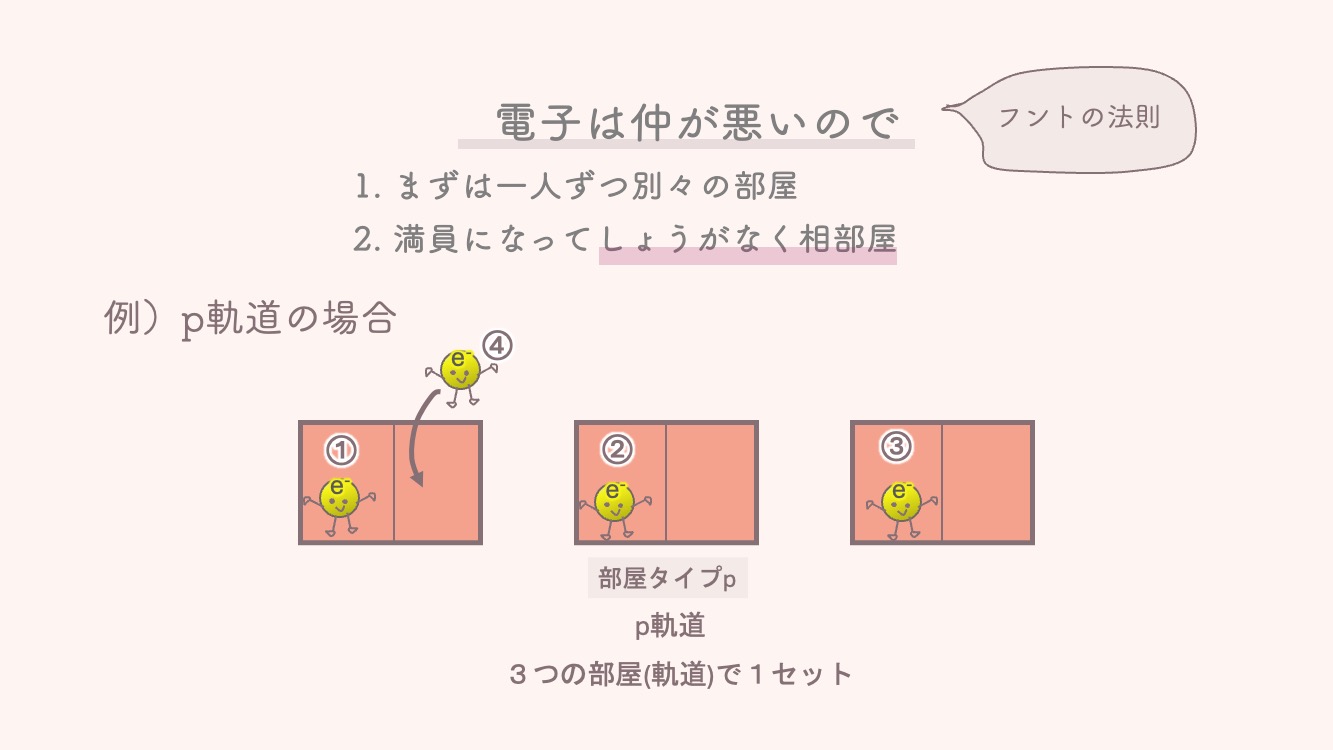
2. 矢印(スピン)の書き方
▲目次へ
では電子がどの軌道に入っていくかを書いてみよう。
電子はいつもクルックルッ回っているんだ。つまり自転しているんだね。
その電子の自転を「矢印( ↑ や ↓ )」で表すんだ。勢いを感じるよね🤣
さて、矢印の書き方で忘れてはいけないのがバウリの排他的原理だよ。
パウリの排他原理:1つの軌道(部屋)には電子は最大2個まで入れますが、2個入った場合は必ず矢印を**「逆向き( ↑↓ )」**にするのがルールです。
「なぜ同じ向きではいけないのか?」
一言でいうと**「磁石同士が反発を避けて、安定している様子を表すため」**です。
-
電子は小さな磁石: 電子は自転(スピン)しているため、一つひとつが小さな「磁石」のような性質を持っています。
-
同じ向き(↑↑)の場合: 磁石の同じ極(NとN)を近づけるのと同じで、強く反発し合ってしまい、同じ部屋にはいられません。
-
逆向き(↑↓)の場合: 磁石の異なる極(NとS)が向き合うような形になり、反発が抑えられて、狭い一つの部屋に安定して収まることができます。
つまり、**「同じ部屋で仲良く過ごしていることを表現している」**と考えるとわかりやすいかな。
パウリの排他原理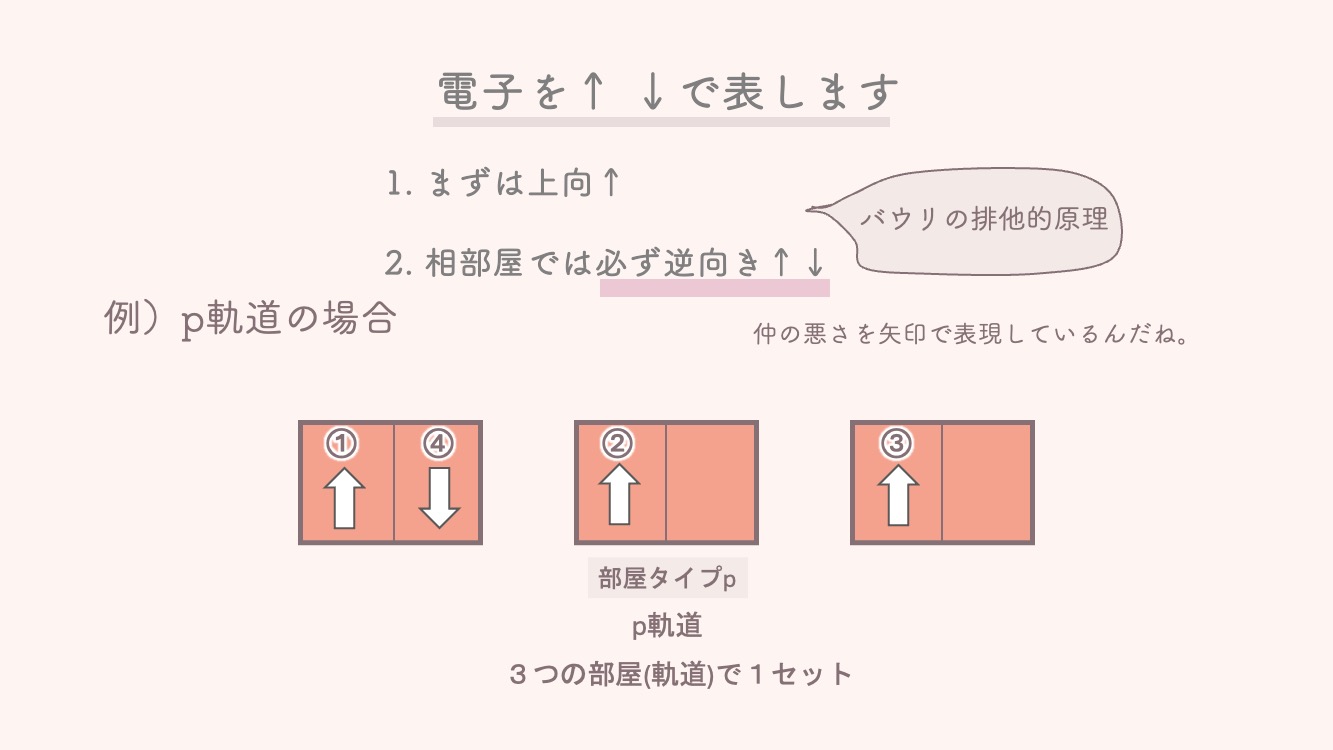
3. 実践例:炭素(C)と窒素(N)
▲目次へ
炭素と、その隣にある窒素を例に見てみましょう。
わかりやすいように最外殻電子を並べてみました。ご参考程度に。
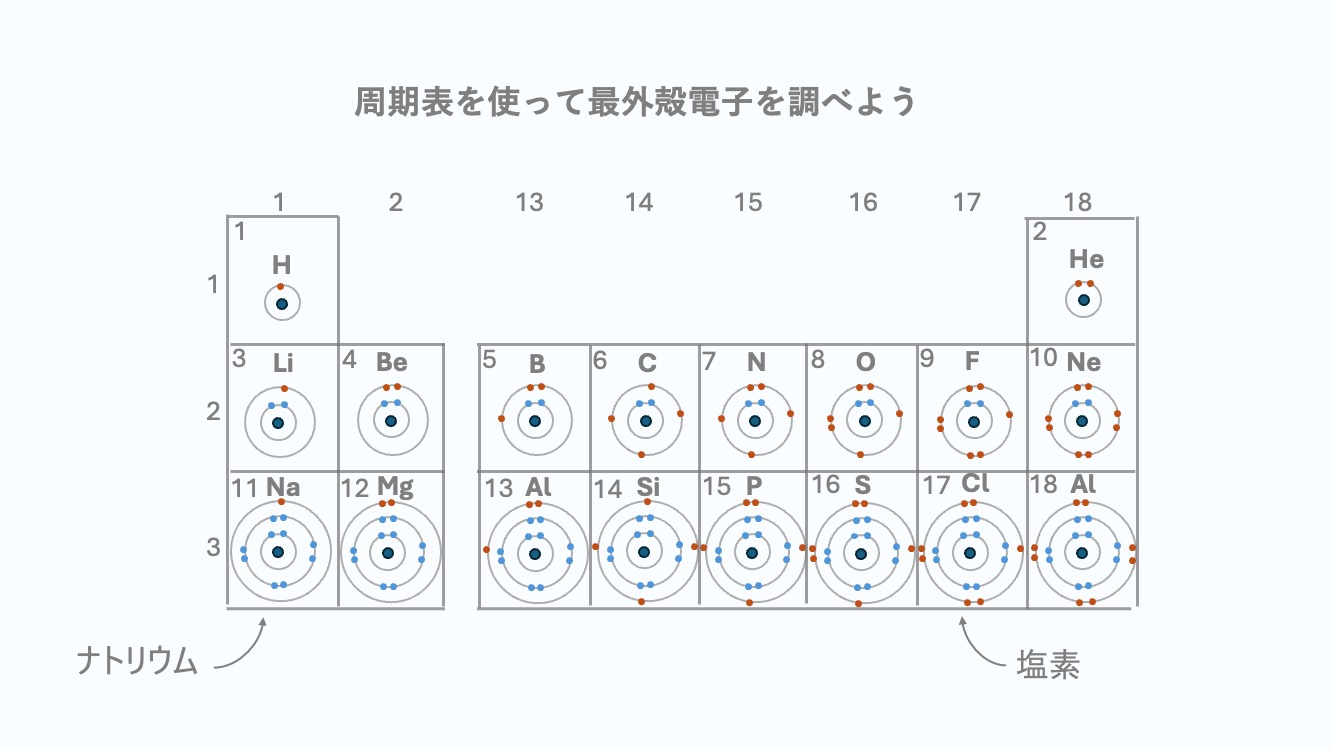
炭素 (Carbon, 原子番号6)
電子の数は6個です。
- 1s軌道:2個入ります(↑↓)→ 満員
- 2s軌道:2個入ります(↑↓)→ 満員
- 2p軌道:残りの2個が入ります。
2pには部屋が3つありますが、電子は仲が悪いので、別々の部屋に上向き(↑)で1つずつ入ります。
1s: [↑↓]
2s: [↑↓]
2p: [↑ ][ ↑ ][ ]
窒素 (Nitrogen, 原子番号7)
電子の数は7個です。炭素より1つ増えます。
- 1s軌道:[↑↓]
- 2s軌道:[↑↓]
- 2p軌道:残りの3個が入ります。
3つの部屋に、1つずつ上向き(↑)で入ります。これで2pのすべての部屋に1人ずつ入った状態になります。
1s: [↑↓]
2s: [↑↓]
2p: [↑ ][ ↑ ][ ↑ ]
🍀 まとめ:ミスを防ぐコツ
- 矢印はまず「上向き」から書く:同じエネルギーの軌道(2pなど)には、まず上向きを並べてから、戻って下向きを書き込みます。
- 4sと3dの逆転に注意:試験ではよく”3pの次は3dではなく「4s」が先に来る”というひっかけが登場しますが、まずは基本の1s〜2pを完璧にマスターしましょう!
【確認しよう】炭素・窒素電子配置の実践クイズ
▲目次へ
4. 【保存版】4sと3dの逆転現象
▲目次へ
★ 3階の奥(3d)より、4階の角部屋(4s)の方が安い!
「えっ、順番通りじゃないの?」と誰もが一度は混乱し、そして試験で狙われるポイントです。
実は、3階の奥にある豪華なスイートルーム(3d)よりも、4階にあるシンプルで入りやすい部屋(4s)の方が**「エネルギーが低い(=コスパが良くて楽に泊まれる)」**という逆転現象が起きています。
1s → 2s → 2p → 3s → 3p → 4s …
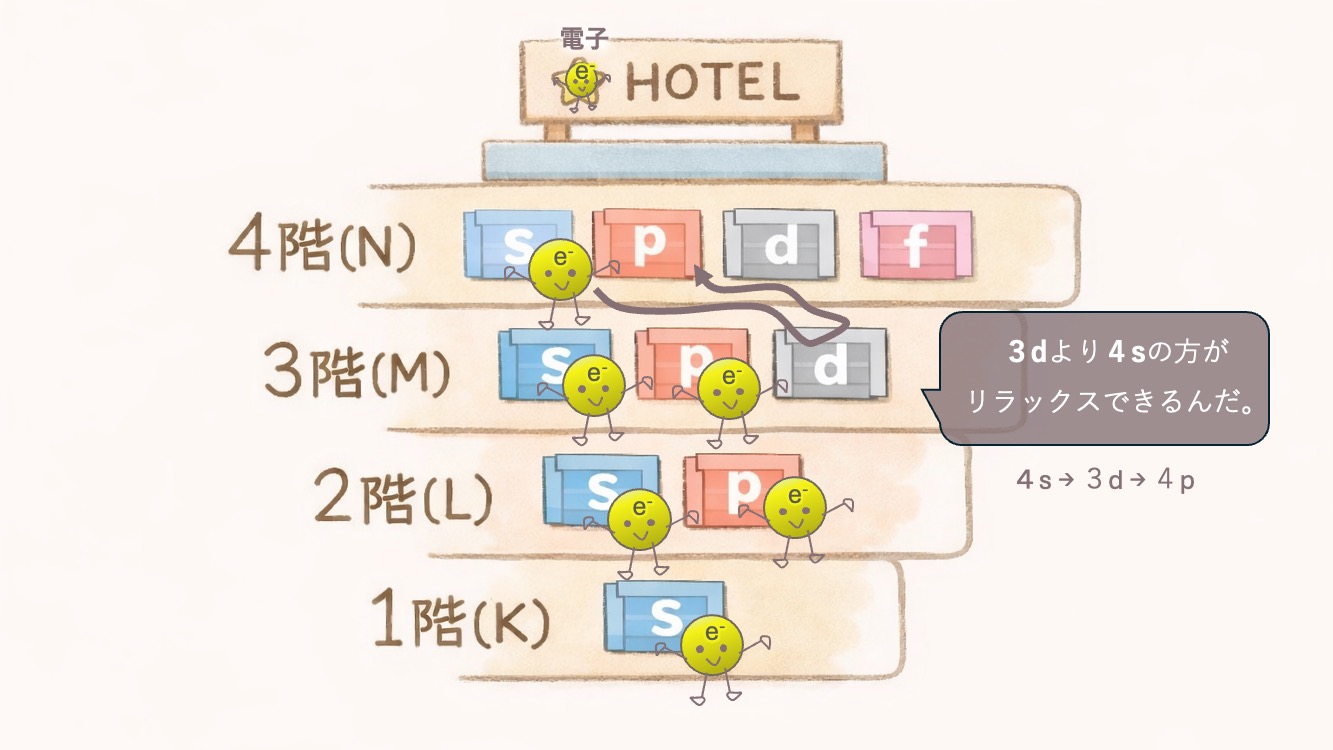
実践:カリウム → カルシウム → 鉄
【カリウム(K)原子番号19】
3pが満員になったら、次は3dを飛ばして、4sに1個入ります。
3p[↑↓][↑↓][↑↓]
4s[↑ ]
【カルシウム(Ca)原子番号20】
**「ここは試験に出る!」**ポイントです。
3dはまだ空室のまま、4sが先に満員になります。
3p[↑↓][↑↓][↑↓]
4s[↑↓]
【鉄(Fe)原子番号26】
4sという「入りやすい部屋」が埋まって初めて、電子は3dに戻ってきます。
3p→4s→3d
5つの部屋に1つずつ入った後、1つだけ相部屋になります。
3d[↑↓][↑ ][↑ ][↑ ][↑ ]
4s[↑↓]
5. 医学・薬学へのリンク:鉄の重要性
▲目次へ
鉄の3d軌道には「1人部屋の電子」が4つもあります。この「スキマ」があるおかげで、鉄は磁石のような力を持ち、酸素を運ぶことができるのです。
3d[↑↓][↑ ][↑ ][↑ ][↑ ]
4s[↑↓]
鉄の「3dのスキマ」こそが、酸素運搬の心臓部!




