15.【保存版】炭素の励起「sp3 混成軌道」を完全攻略! 電子配置から繋がる立体構造の秘密

※本記事にはアフィリエイトリンクが含まれる可能性があります。
丸暗記を卒業し、薬理や代謝を「論理」で支配する。
その本質である電子の動きを掴むことが、
あなたを市場価値の高い専門家へと押し上げます。
「なぜ炭素の腕は4本なの?」
医学生・薬学生が最も苦労する「sp³混成軌道」。
教科書の説明が難しすぎて、思考停止していませんか?
(もちろん、学生時代の私も思考停止していました…!)
実はアミノ酸も、このsp³混成軌道で形作られています。
アミノ酸の性質を真に理解するために、sp³混成軌道のマスターは絶対に不可欠。
ここさえクリアすれば、タンパク質も酵素反応も、
パズルを解くようにスルスル頭に入るようになります。
現役医師・医学博士が教える「ホテルの部屋割り」攻略法
複雑な軌道の概念を、独自のアナロジーで極限まで噛み砕いて解説。
炭素が「本気」を出して4本の腕を作るプロセスさえ理解すれば、
有機化学は手に取るように分かるパズルに変わります。
- ✔︎ テスト直前に焦って泣きたくない
- ✔︎ 高配点の記述問題で確実に満点を取りたい
そんなあなたのために、図解を交えた
「最速攻略ガイド」をお届けします。
📚 目次


炭素がどうやって4本の腕を作るのか、解説していくよ。
1. 前回の復習と炭素の「腕」の謎
▲目次へ
前回の記事で、電子は「居心地がいい部屋」から順に埋まることを学びました。
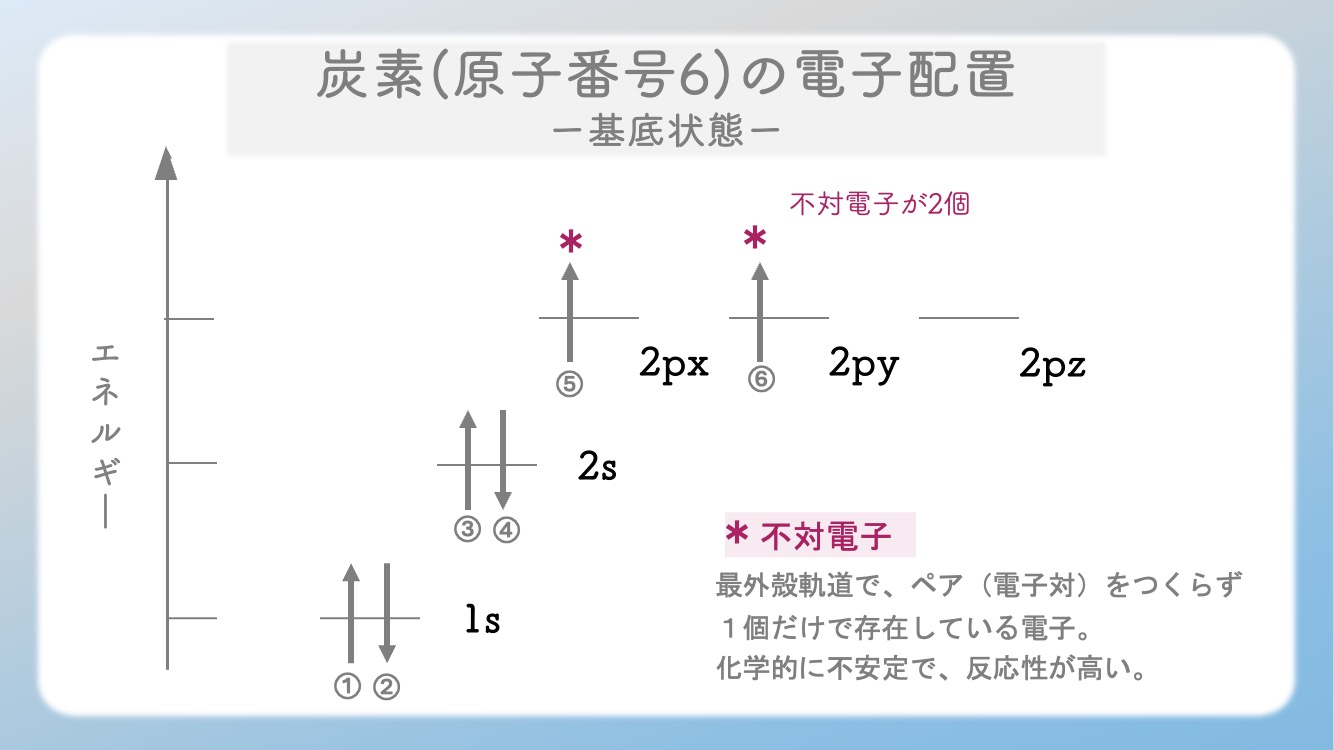
炭素(原子番号6)の電子配置を復習しましょう。
・1s:2個(満員)
・2s:2個(満員)
・2p:2個(3部屋のうち2部屋に1個ずつ)
ここで重要ルール。「共有結合は、1人ぼっちの電子(不対電子)同士が手をつなぐこと」でしたね。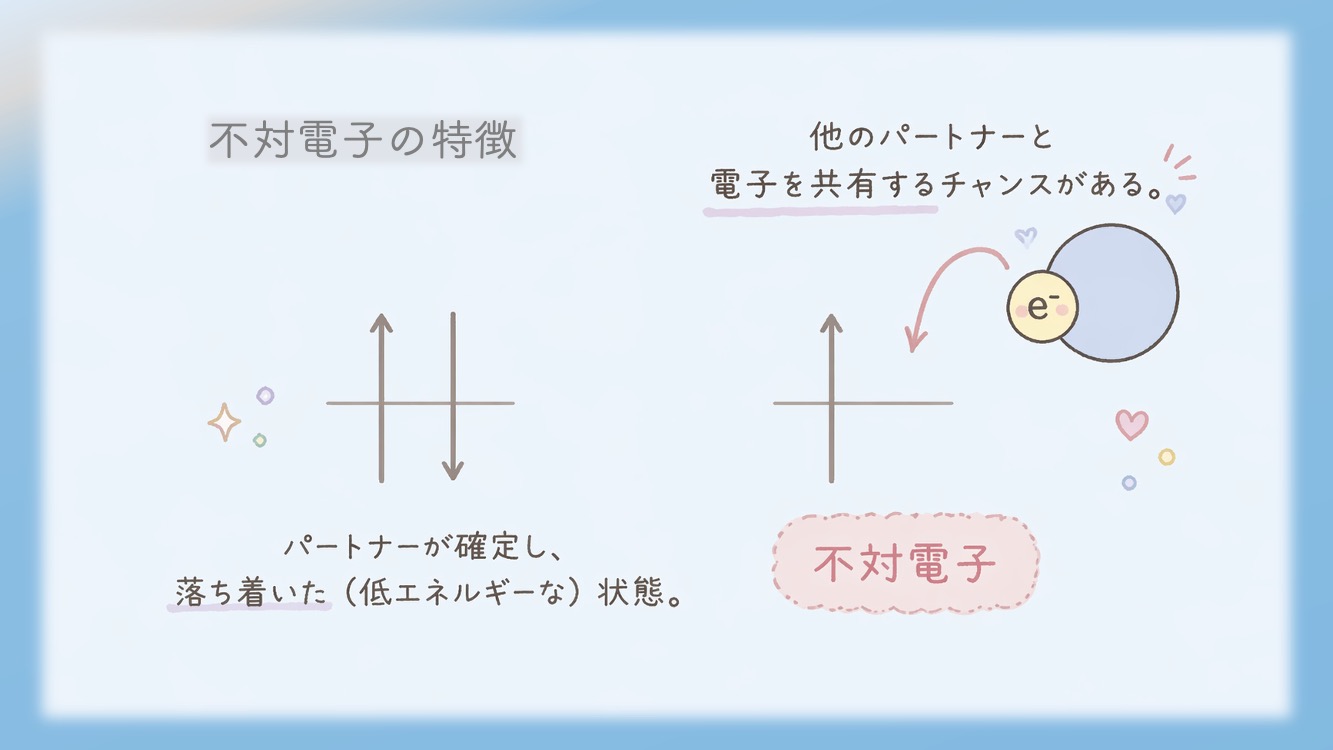
⚠️ 炭素の不対電子、2個しかなくない?
2. 炭素の「本気」:電子のジャンプ(励起)
▲目次へ
そうなのです。炭素の不対電子は2個です。
しかし炭素は他の原子と結合する際、エネルギー⚡️を使って自分をアップデートさせるのです。並々ならぬ気合を感じますね。
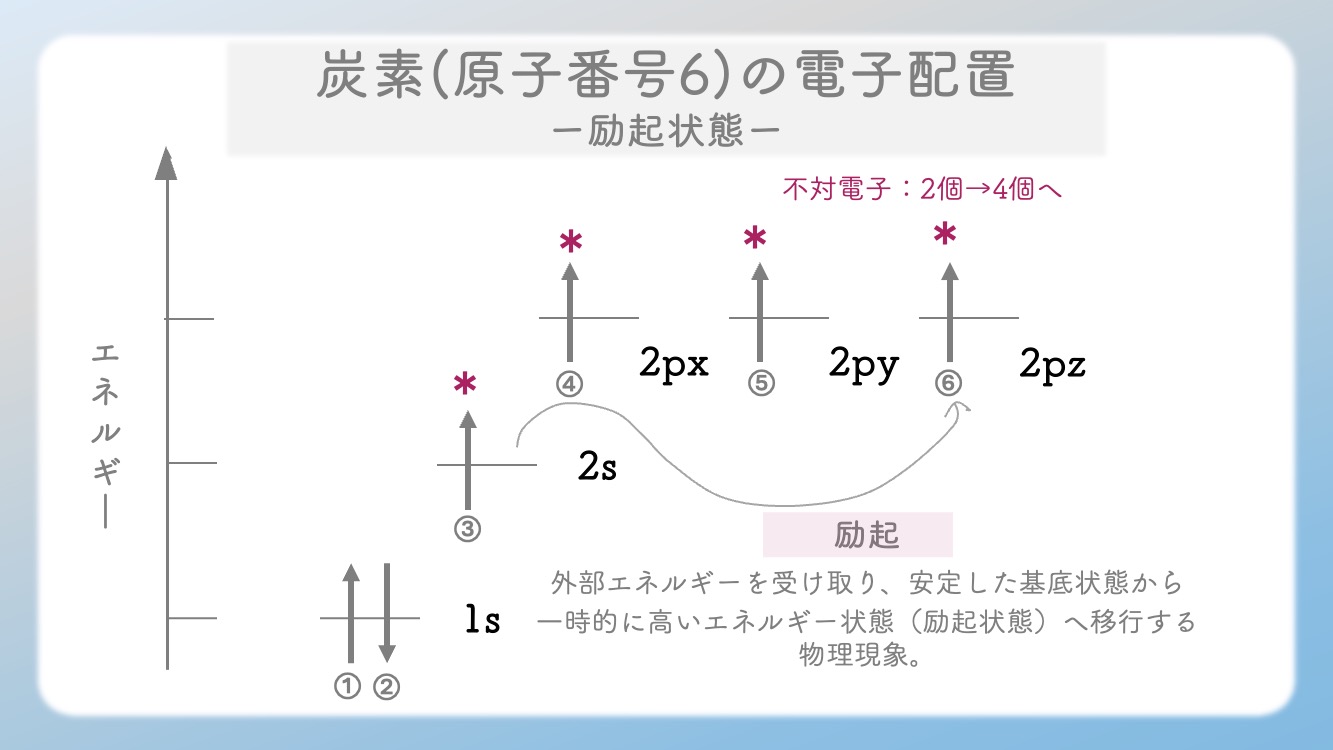
これを励起(れいき)といいます。
・2s:1個
・2p:3個(各部屋に1個ずつ)
これで不対電子が合計4個になりました!
3. 次なる壁:形がバラバラ問題
▲目次へ
さて、励起して電子を移動させるということは、理論上はわかりました。
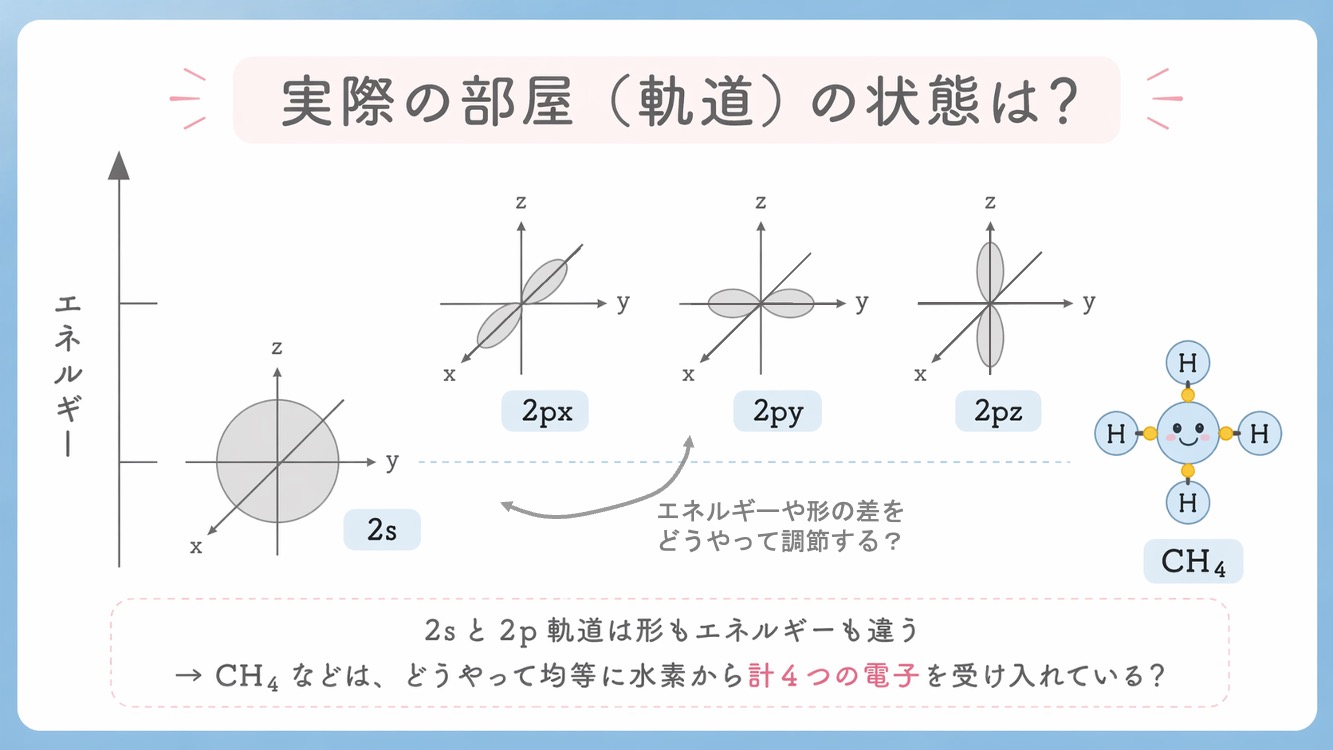
でも実際の部屋(軌道)はどうやって準備をすすめているのでしょう?
「2s(球形)」と「2p(ダンベル形)」。 これらは形もエネルギーもバラバラです。つまり、そのままでは「4つの等しい結合」を作ることなど不可能なのです。
しかし、現実のメタン(CH₄)を見てください。 中心の炭素に、4つの水素が寸分の狂いもなく均等に結合しています。腕の長さも、角度も、すべてが完全に等価。
一体、どうやってこの矛盾を解決しているのでしょうか?
4. 解決策:これが sp3 混成軌道だ!
▲目次へ
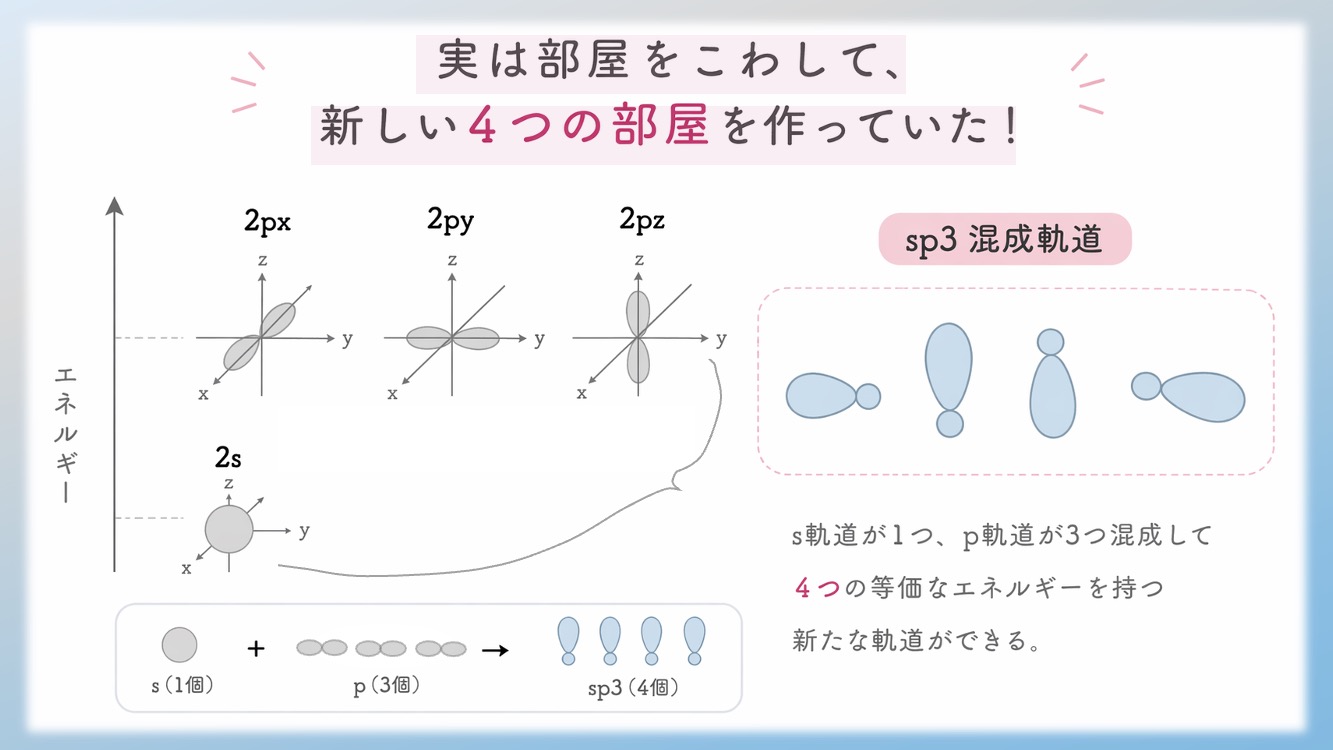
なんと!炭素はエネルギーを使い、既存の部屋をすべて「壊して作り直している」のです。
形もエネルギーも違うバラバラな部屋を一度シャッフルし、全く新しい4つの均一な部屋へと再生する——。これこそが、「sp³混成軌道」の正体です。
形もエネルギーも均一な部屋だから、4人の水素と仲良く手をつなぐことができます。
5. なぜ109.5度なのか?数学的に「最速」で理解する
▲目次へ
CH4(メタン)のように、炭素に結合する原子がすべて同じ場合、sp3混成軌道は完璧な正四面体を形成し、その結合角は109.5度となります。
4つの頂点(水素)が中心(炭素)から均等に離れている
=『頂点が4つある正多面体は?』→『正四面体』。
=中心から見て4つの腕が最もバランスよく広がった形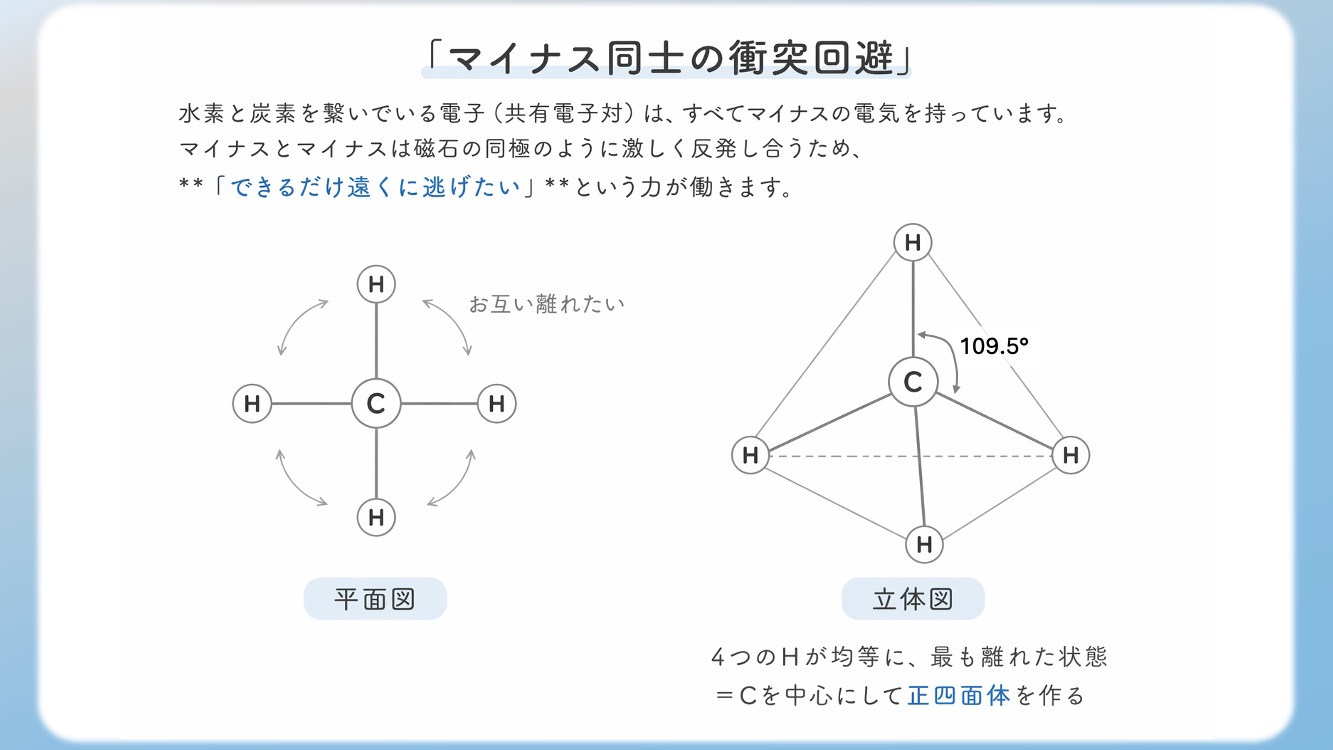
この109.5度という数字。試験でもよく聞かれます。今日はこの数字を丸暗記するのではなく、ベクトルを使って、スマートに導く方法を紹介します。
ステップ1:座標を「箱」でイメージする
 炭素(中心)を原点 O(0, 0, 0) とします。1辺の長さが「2」の立方体をイメージして、そのカド(対角線上)に水素を配置します。
炭素(中心)を原点 O(0, 0, 0) とします。1辺の長さが「2」の立方体をイメージして、そのカド(対角線上)に水素を配置します。
- 📍 中心(炭素): O (0, 0, 0)
- 📍 頂点A(水素): A (1, 1, 1)
- 📍 頂点B(水素): B (1, -1, -1)
ステップ2:ベクトルの「内積公式」を使う
2つのベクトル OA と OB のなす角を θ(シータ)とすると、公式は以下の通りです。
ステップ3:数値を代入して計算
① 内積を計算
(1 × 1) + (1 × -1) + (1 × -1) = -1
② ベクトルの長さを計算
√(1² + 1² + 1²)= √3
③ cosθ を求める
-1 = √3 × √3 × cosθ
-1 = 3 × cosθ
cosθ = -1/3
ステップ4:結論
cosθ = -1/3 を逆算すると、以下の角度が導かれます。
θ = 約 109.5度
これが、電子たちが反発から逃げ切り、最も安定したポジションを確保した瞬間の正体です。
💡 今回のパワーワード
- 109.5度は、反発から逃げ切った「妥協の極致」。
- cosθ = -1/3。このシンプルな数字がアミノ酸の立体構造を支配している。
- 丸暗記は不要。マイナスの反発が、幾何学的にこの角度を導き出す。
- ただし、アミノ酸は不斉炭素を持ち、結合する分子の種類がすべて異なるため、電気的な反発に差が生じて構造がわずかに歪みます。
5. まとめ:なぜ sp3 が必要なのか
▲目次へ
- 励起:電子を移動させ、腕を4本にする。
- 混成:軌道を混ぜて、均一な4つの部屋を作る。
- 結果:安定した正四面体構造が完成する!





