16.【医・薬学生必見】なぜペプチド結合は平面で、回転しないのか?sp2混成軌道で紐解く試験の急所

※本記事にはアフィリエイトリンクが含まれる可能性があります。
丸暗記を卒業し、薬理や代謝を「論理」で支配する。
その本質である電子の動きを掴むことが、
あなたを市場価値の高い専門家へと押し上げます。
sp3 がピラミッドなら、sp2 は「硬い板」。
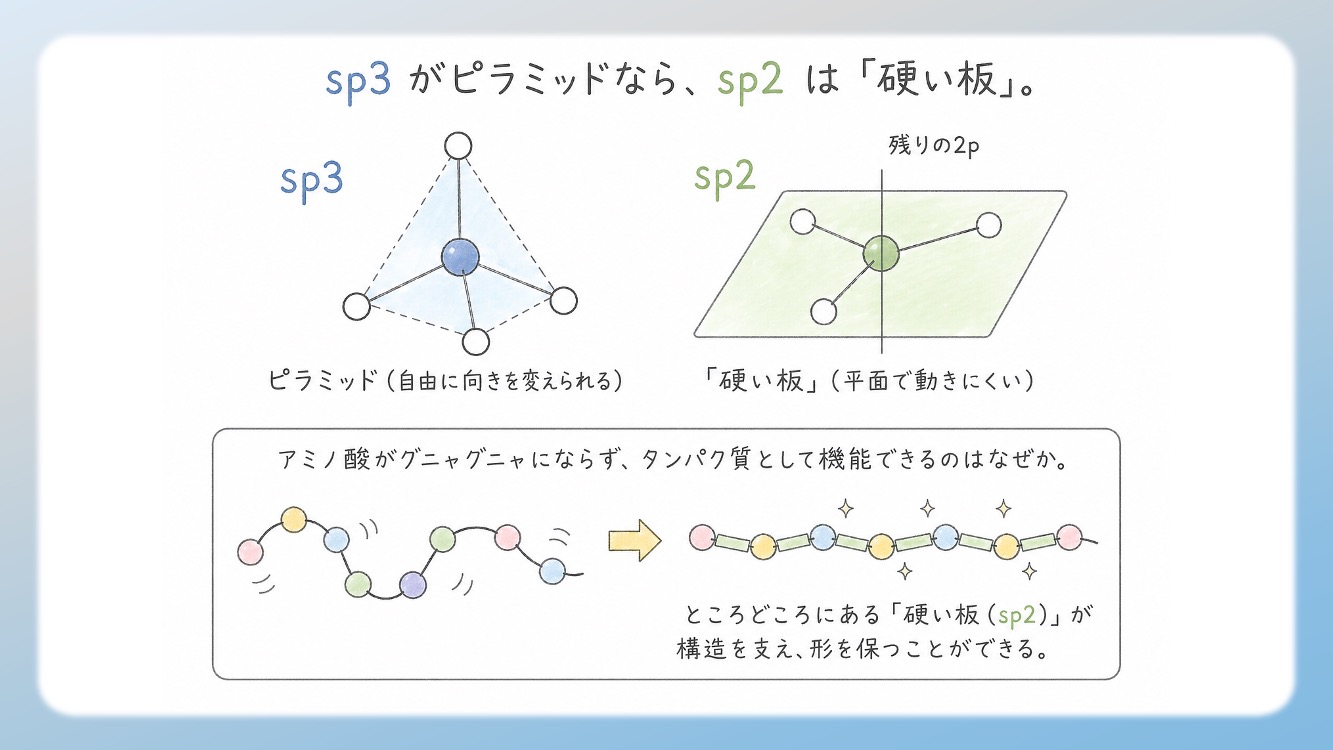
アミノ酸がグニャグニャにならず、タンパク質として機能できるのはなぜか。
試験頻出の「平面構造」の正体を、どこよりもスッキリ解説します。
📚 目次:sp2混成軌道と平面構造の謎を完全マスター!
1. sp2混成の基礎|sp3との決定的な違いを最速復習
▲ 目次へ
炭素原子はもともと4つの電子(価電子)を持っています。
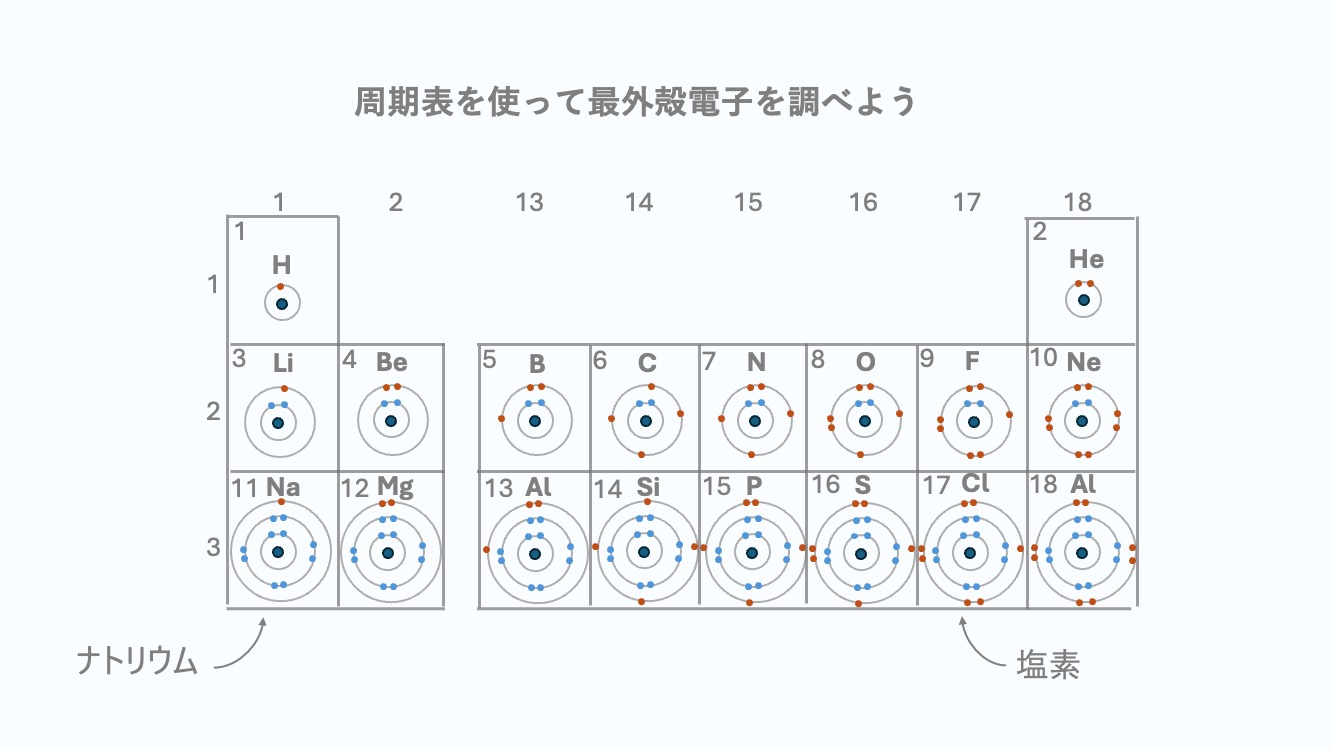
前回学んだ sp3 では、s 軌道1つと p 軌道3つを全部混ぜて
「4本の等価な腕」を作りました。
しかし、今回の sp2 混成軌道では、混ぜ合わせるのは以下の3つだけです。
- ✅ s 軌道 × 1
- ✅ p 軌道 × 2
sが1個とpが2個なので「sp2」👍
残りの p 軌道1つは、混ぜずにそのまま残しておきます💤
2. 電子のジャンプ!sp2軌道ができるまでの全工程図解
▲ 目次へ
ではsp2 混成軌道ができるまでを詳しくみていきましょう📚
まずは、炭素がもっとも落ち着いた『基底状態🍀』から、
エネルギー⚡️をもらって、電子がひとつ上の2p軌道へジャンプした『励起状態(れいきじょうたい)🔥』を見てみましょう。
電子配置の書き方はこちらをみてね。
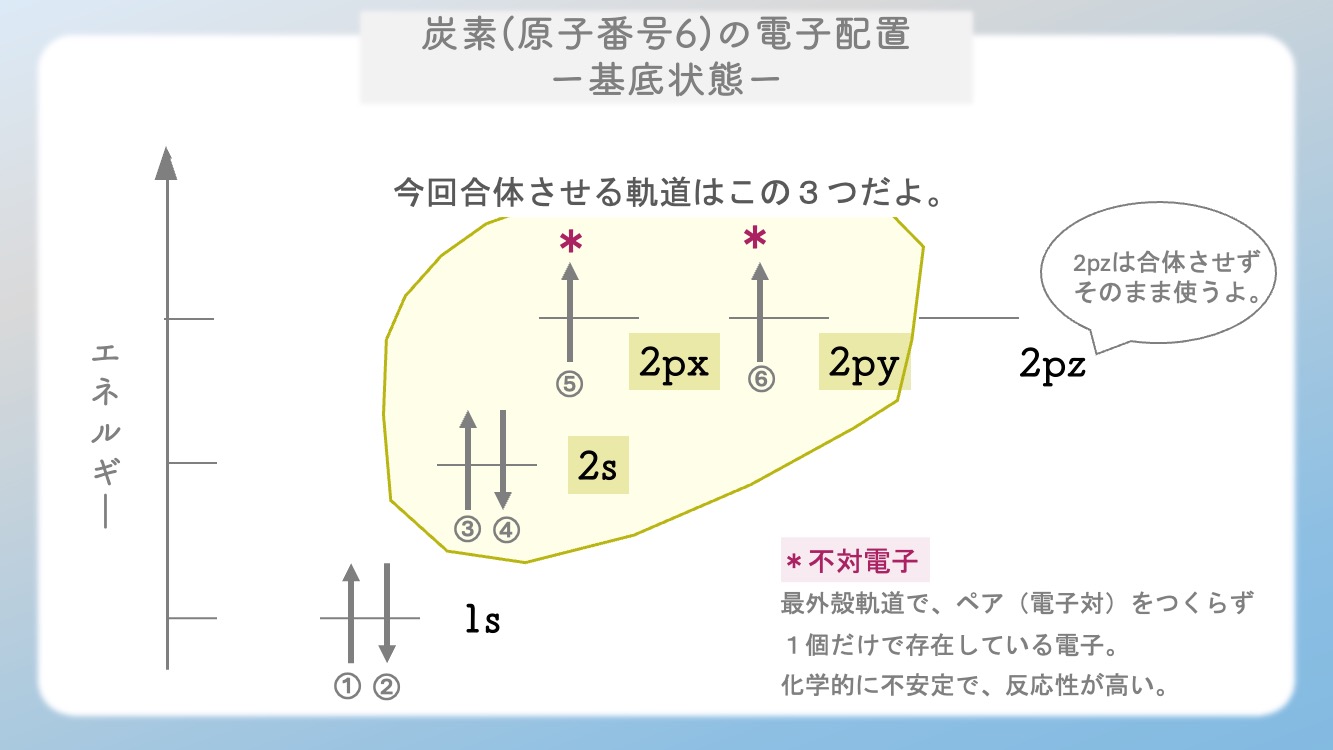
① 炭素がもっとも落ち着いた『基底状態🍀』
炭素は全部で6個の電子を持ちます。
一番内側の1s軌道に2個(満室)
二番目の2s軌道に2個(満室)
三番目の2p軌道に2個(2/6 埋まってる状態)
2s 軌道: ( ↑↓ )
1s 軌道: ( ↑↓ )
② 電子がジャンプした直後(励起状態)
エネルギーを貰って、2sの電子1個が2pにジャンプします
4つの電子が、それぞれバラバラの部屋に入っている状態です。
2s 軌道: ( ↑ )
③ sp2 混成軌道の完成
ここで、2s の1部屋と、2p のうち2部屋だけが合体して、同じ高さ(同じエネルギー)の新しい部屋になります。
sp2 混成軌道: ( ↑ ) ( ↑ ) ( ↑ )
1s 軌道: ( ↑↓ )
なぜ1つ残すのか?
この「混ぜてもらえなかった 2p 軌道」が、実は非常に重要な仕事をします。
3. 120度の平面構造と「垂直なp軌道」が作る空間配置
▲ 目次へ


📍 sp2 の3人組(平面の土台)
混ぜて作った 3つの sp2 軌道は、互いに一番遠ざかろうとして「同じ平面上で120度」に広がります。これがシグマ結合(強い骨組み)になります。
📍 ぼっちの 2p くん(垂直の壁)
混ぜ合わせに参加しなかった残りの1本は、三角形の平面に対して垂直(真上と真下)に突き刺さっています。これが隣の炭素と重なると、二重結合(パイ結合)が生まれます。
✨ 今回の「スッキリ」ポイント
- ✅ 3本の sp2 軌道:平面的な土台(強い結合)
- ✅ 1本の p 軌道:平面から垂直に飛び出している
4. なぜ sp2 は「平面」なのか? 3本の腕が導き出す「120度の必然」
▲ 目次へ
ちょっと待って。なぜsp2軌道はなぜ平面を作るの?
結論から言うと、「3つの腕が互いに一番遠ざかろうとすると、正三角形(平面)になるしかないから」です。


3本の腕が一番ケンカしない(反発し合う)形を探すと、物理的に平面になるしかないんだ。
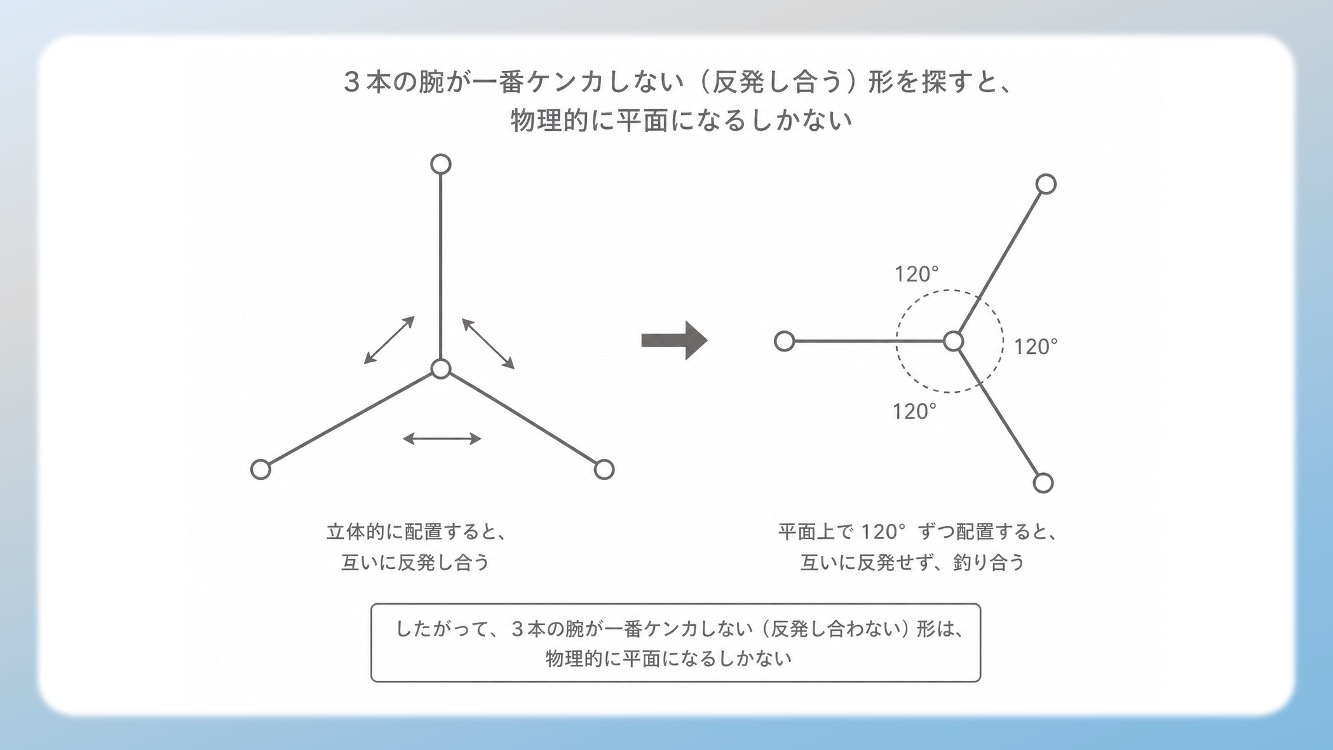
腕の本数が「形」を決める
前回学んだ sp3 混成軌道は、4本の腕を持っていました。4本の腕が空間で最も離れようとすると、3次元的に広がる「正四面体(立体)」になります。
しかし、今回の sp2 混成軌道は「3本の腕」しかありません。
- 2つの点(腕)を結ぶと「線」になる。
- 3つの点(腕)を同じ力で反発させると、必然的に「平面上の正三角形(120度)」に落ち着く。
3点を通る面は必ず一つに定まるため、この3本は絶対に立体にはなれず、平面になるのです。
5. なぜ余った2p軌道は平面に垂直なのか?
▲ 目次へ


混成軌道を作るとき、原子の中では軌道(電子の雲)同士が猛烈に反発し合っています。
互いに最大限に離れようとして、同じ平面上で120度ずつに広がります。
この3本から最も効率よく離れられる場所を探します。
もし 2pz が平面の近くに倒れてしまうと、隣にある sp2 軌道と近くなりすぎて、強い反発(ストレス)が生まれてしまいます。
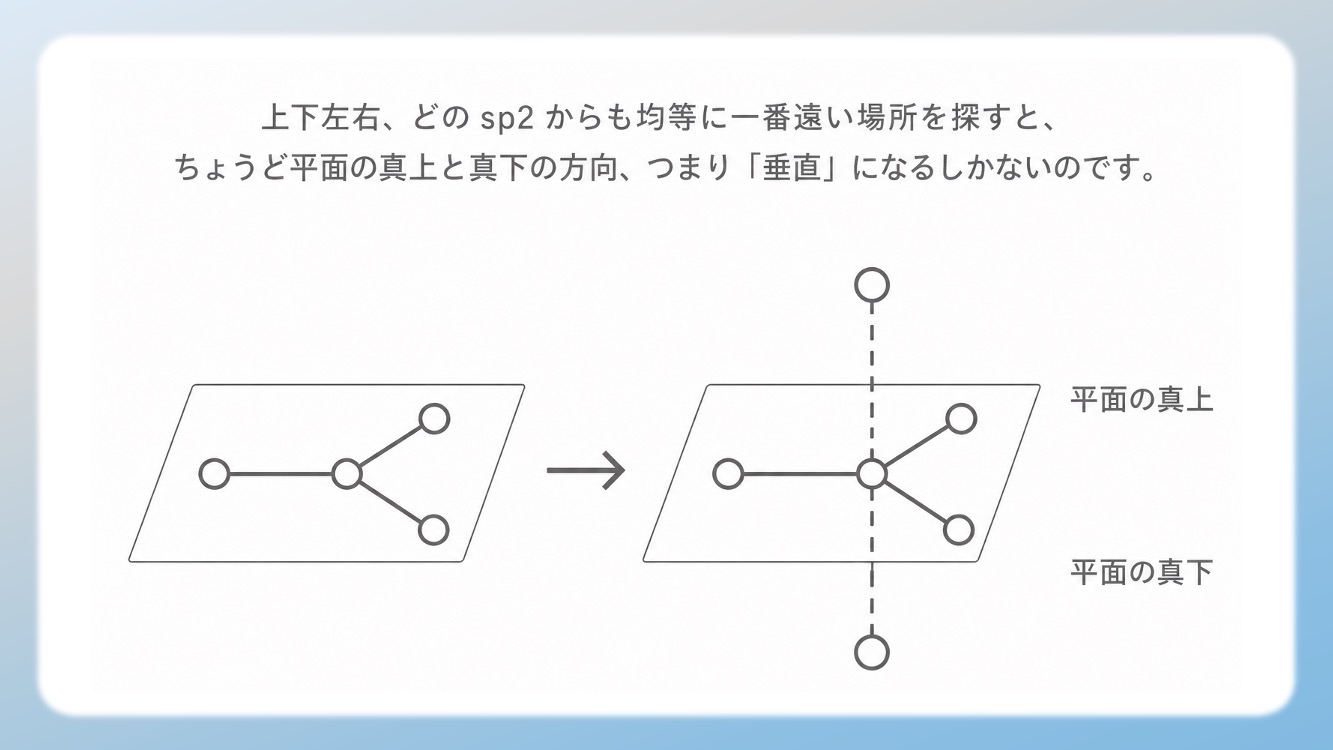
上下左右、どの sp2 からも均等に一番遠い場所を探すと、ちょうど平面の真上と真下の方向、つまり「垂直」になるしかないのです。
🧠 試験で役立つイメージ思考法
360度全方位に広がるイメージ
3人で引っ張り合うフラットな円
この「3本による平面」という土台があるからこそ、アミノ酸のペプチド結合はカチッと固まった「硬い板」のようになり、タンパク質が複雑な立体構造を維持できるのです。
次は、この「平面」がどうやって二重結合の「回転禁止」に繋がるのか、
詳しく見ていきましょう。
6. シグマとパイの使い分け|二重結合が「回らない」本当の理由
▲ 目次へ戻る
この sp2 炭素同士がくっつくと、面白いことが起こります。
📍 二重結合の正体:シグマ結合と パイ結合
中心軸で重なるので、これだけなら独楽(こま)のように回れます。
混ぜなかった p 軌道同士が、横側でふわっと重なります。
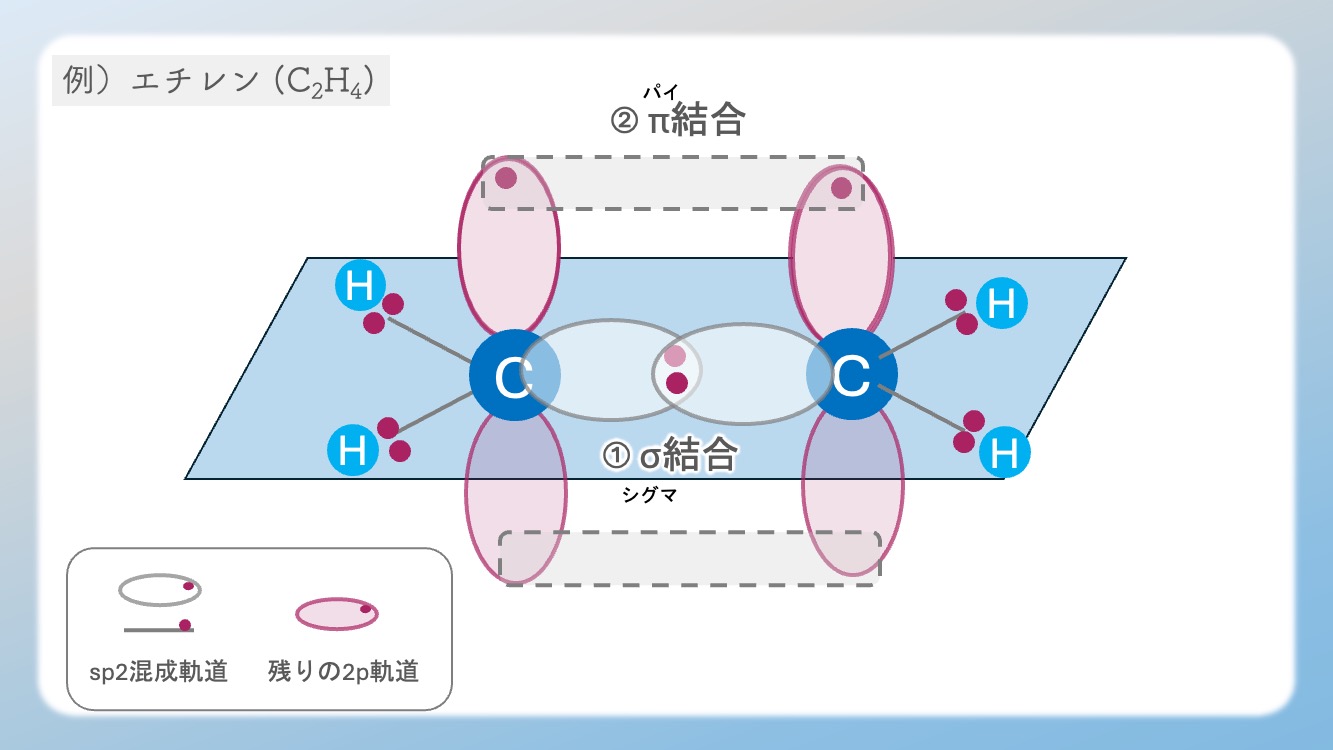
つまり、二重結合ってこういうこと。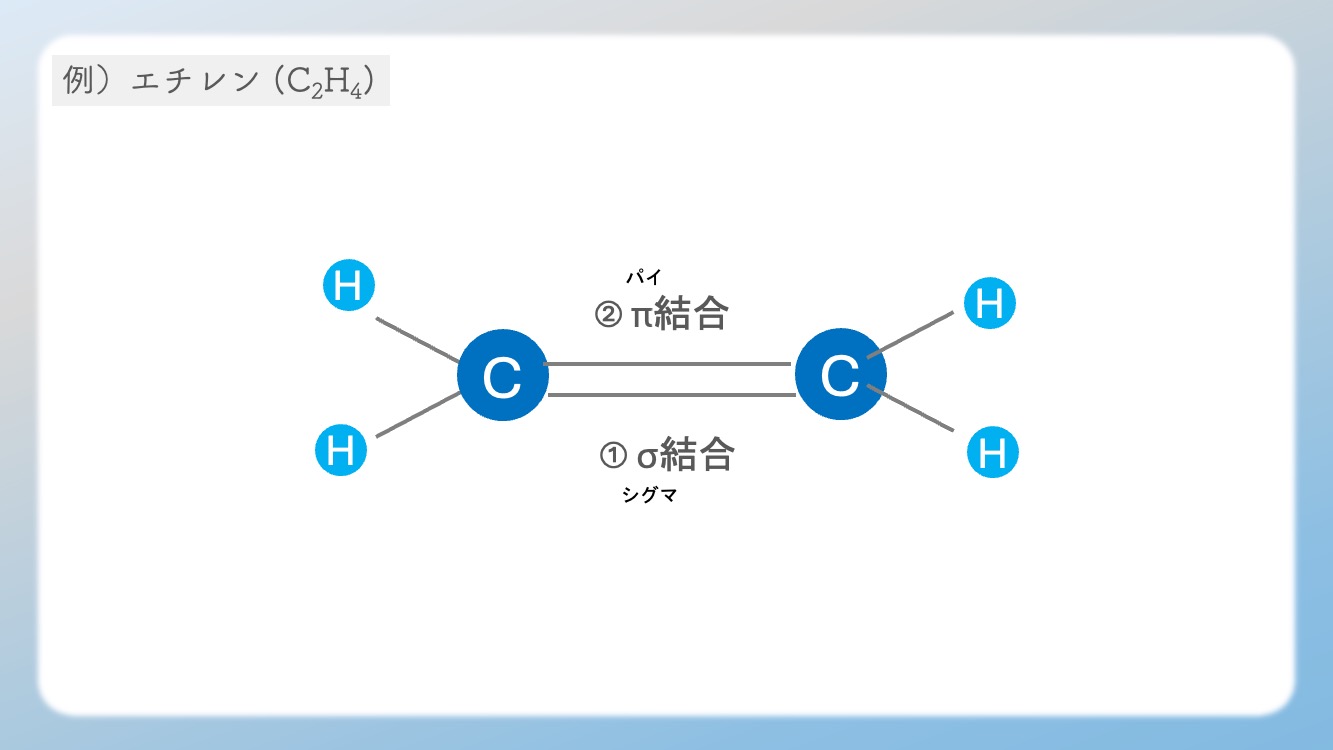
そして、この二重結合は回転しないんだ。
なぜだかわかる?
⚠️ なぜ二重結合は回らないのか?
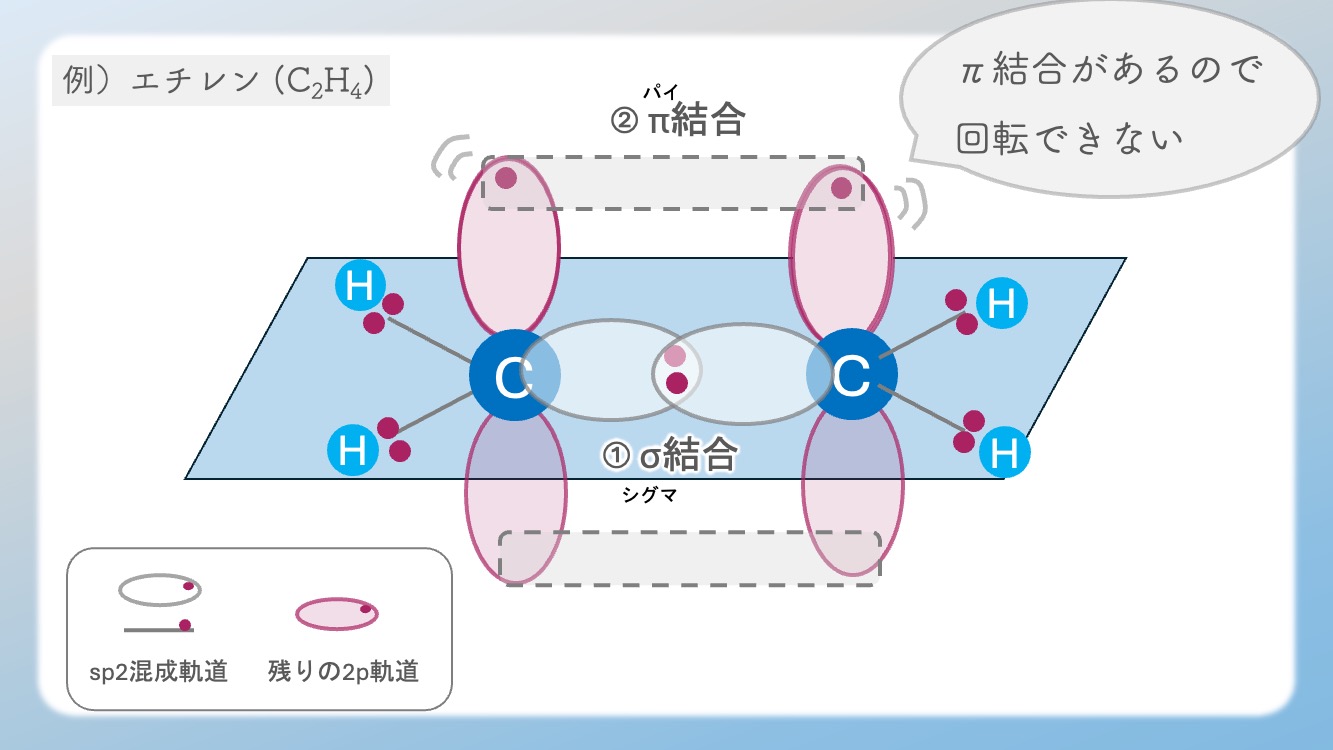
パイ結合は、2つの炭素の上下にある p 軌道が「横向きに重なり合う」ことで成立しています。
もしこの結合を無理やり回転させようとすると、並行に並んでいた p 軌道が互いに離れてしまい、この パイ結合がブチッと千切れてしまう ことになります。
結合を千切るには莫大なエネルギーが必要なため、通常の状態で二重結合が勝手に回ることはありません。この「回転禁止」というルールがあるおかげで、アミノ酸のペプチド結合はカチッと固まった板のような構造を保てるのです。
7. アミノ酸攻略|ペプチド結合を「平らな板」に変える魔法
▲ 目次へ戻る


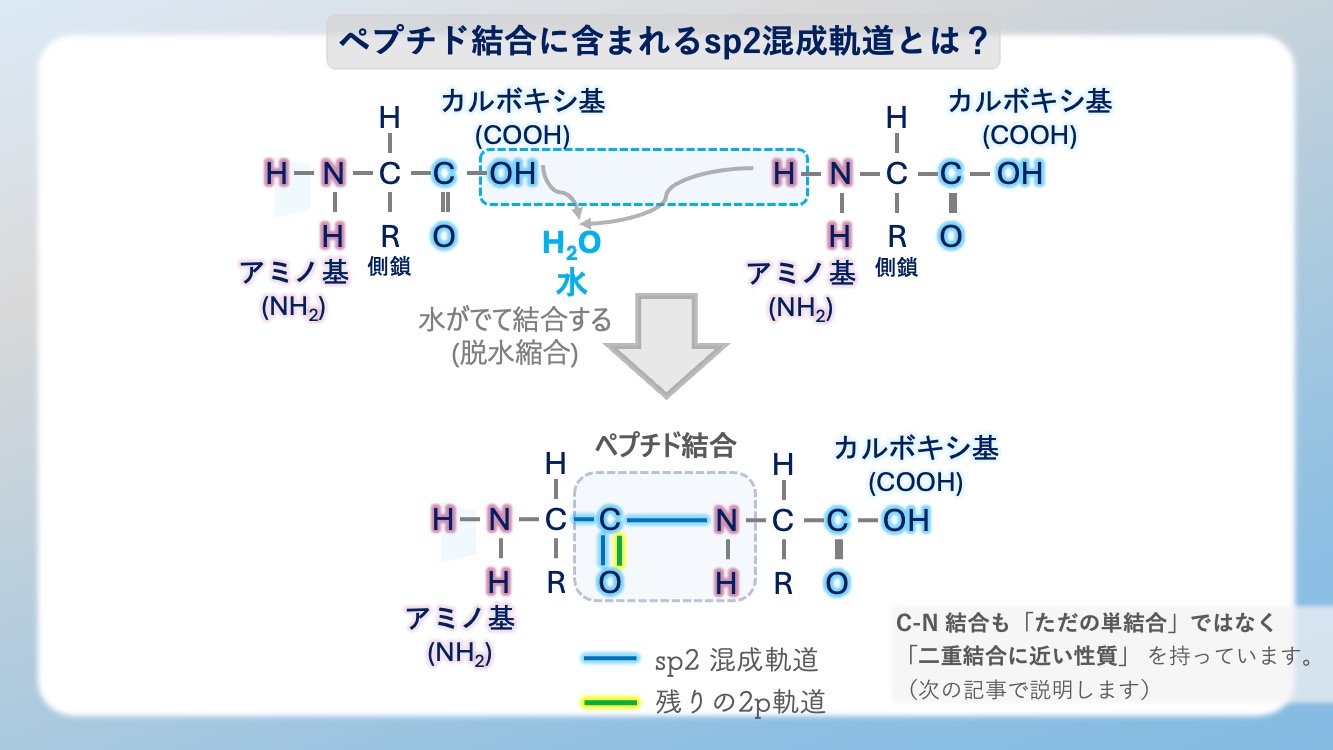
アミノ酸が繋がってタンパク質になるとき、「ペプチド結合」というものが作られます。
実はこのペプチド結合の周りでは、電子がこの sp2 混成のような状態をとっています。その結果、ペプチド結合の部分は「回転できない平らな板」のようになります。
クルクル回れる自由な関節
カチッと固定された平らなパネル
もしアミノ酸の結合がどこでも自由に回っていたら、タンパク質はグニャグニャになってしまい、酵素や筋肉としての形を保てません。
この「sp2 的な平面構造」があるおかげで、タンパク質は精密な設計図通りの形を作れるのです。
8. 📝 本日のスッキリまとめ:sp2混成軌道と二重結合の正体
▲ 目次へ戻る
📍 そもそも「sp2混成軌道」とは?
炭素原子が持つ「1つのs軌道」と「2つのp軌道」がまざり合ってできた、新しくできた3本の同じ形の軌道のこと。1本だけ混ぜ合わせに参加しなかった「2pz軌道」が余るのが最大の特徴です。
📍 今日の重要ポイント・チェック!
3本の腕が電子同士の反発を避けて互いに最も遠ざかろうとすると、物理的に「120度ずつ開いた正三角形」の形に並び、平面構造になります。
平面上の3本の腕から最も遠くへ逃げられる場所は、その平面の真上と真下しかありません。そのため、平面を貫く「垂直な串」のような形で存在します。
二重結合は、正面で繋がる「シグマ結合」と、垂直なp軌道同士が横で重なる「パイ結合」の2階建て。回転させようとするとパイ結合が千切れてしまうため、ガチッと固定されます。


次回のテーマ:
「17. アミノ酸攻略|ペプチド結合を『平らな板』に変える魔法」
🐾 Dr.シロネコの応援メモ
使い終わった教科書📚はどうしていますか?医学書は価値が高いうちに整理するのが賢い方法です。次のステップへ進むための軍資金にするのも手ですよ。👍





