〜pKa・等電点・緩衝域を一気につなぐ〜
※本記事にはアフィリエイトリンクが含まれる可能性があります。

こんにちは!
生化学の勉強を頑張っている皆さん、
今日も本当にお疲れさまです。
1. この記事が解決してくれること
滴定曲線、まだ形だけ🧠暗記していませんか。
pKa、等電点、緩衝域。
✏️試験でつながらなくなる。
この記事では、グリシン を使って、
滴定曲線を1本の流れとして読めるようにします。💯
2.H⁺ がつく場所と外れる場所。 まず基本をおさえよう

まず前提として、
アミノ酸には、H⁺ を受け取れる場所 と、
H⁺ を手放せる場所 があるよ。
受け取れる場所と、手放せる場所があるの?

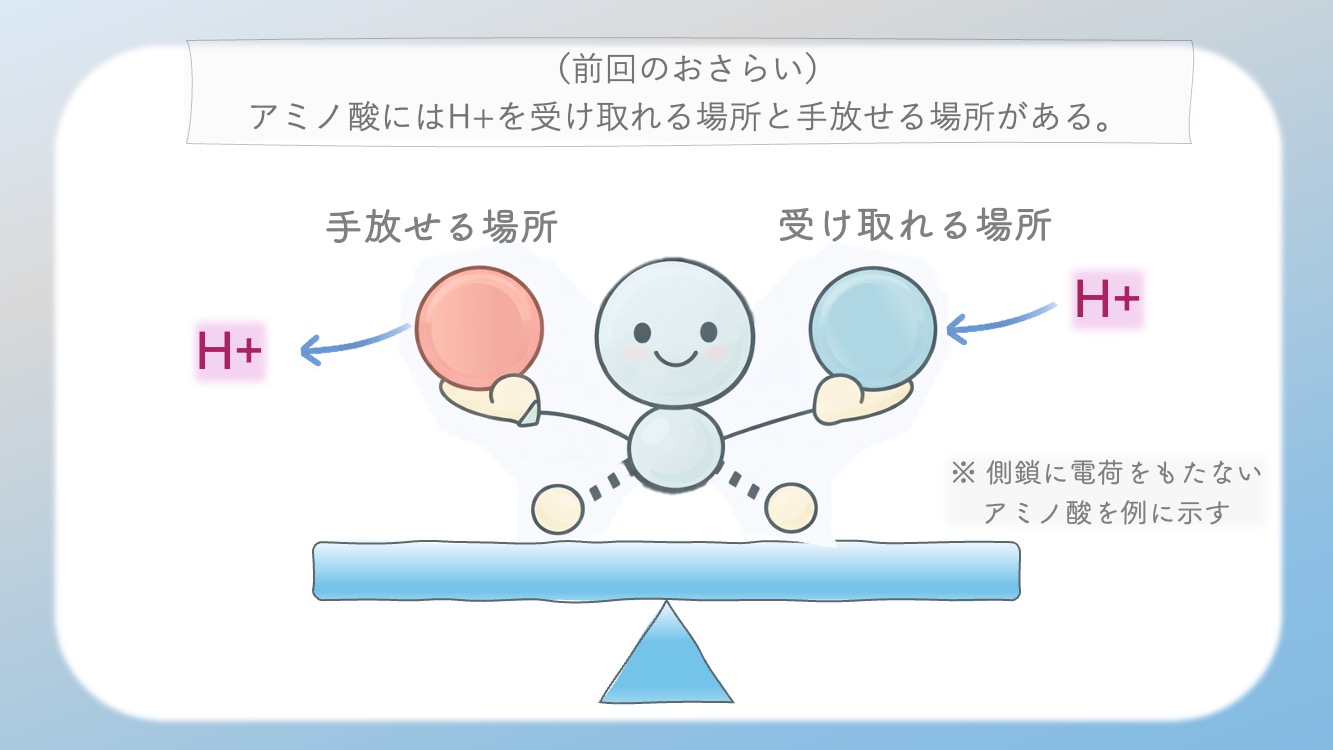

そう。
・マイナスの場所は、
プラスを受け取れる。
・H+を持っているからプラスの状態である場合、
H+を手放すことができるんだ。
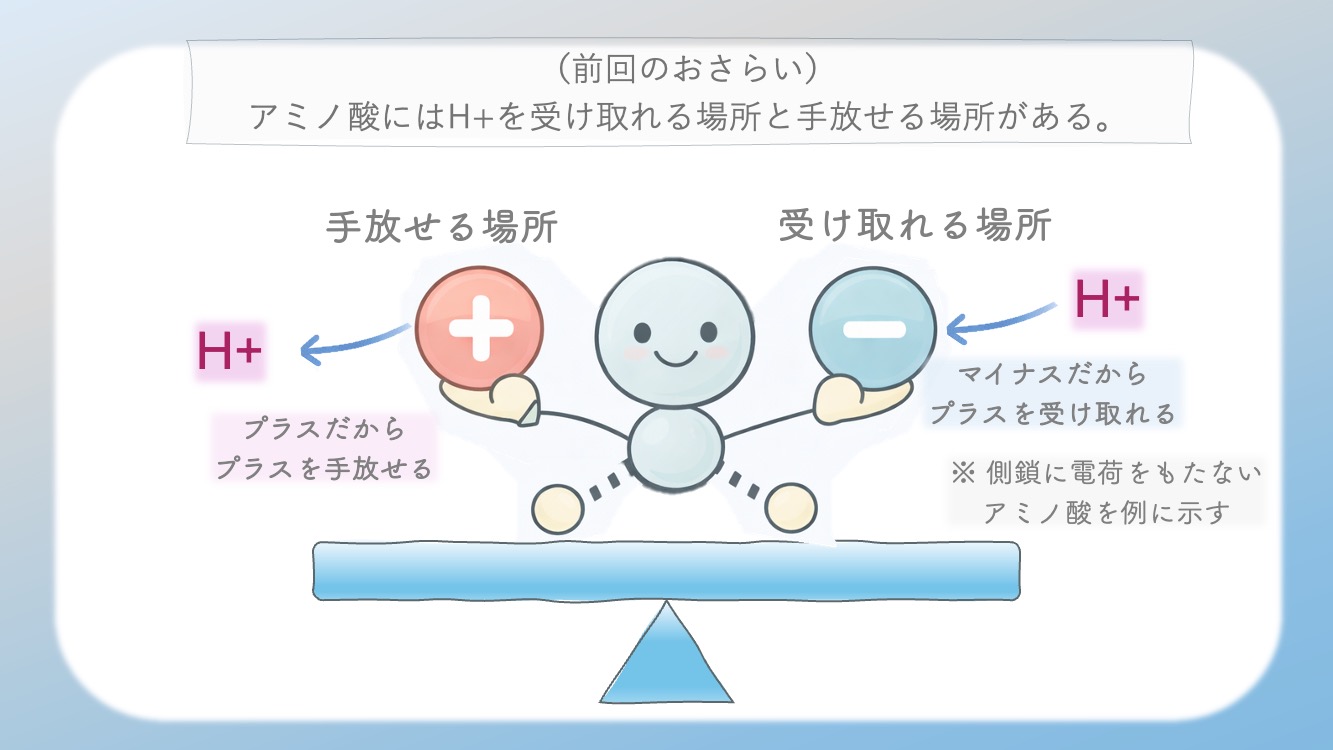

どこが受け取れる場所なのか?
どこが手放す場所なのか?
常に意識しておくと、今何がおこっているのか
わかりやすくなるよ。

では
その場所はどこなのか?
詳しくみていこう。
前回のブログ記事、
”アミノ酸のイオン性”の
おさらいになるけれど、
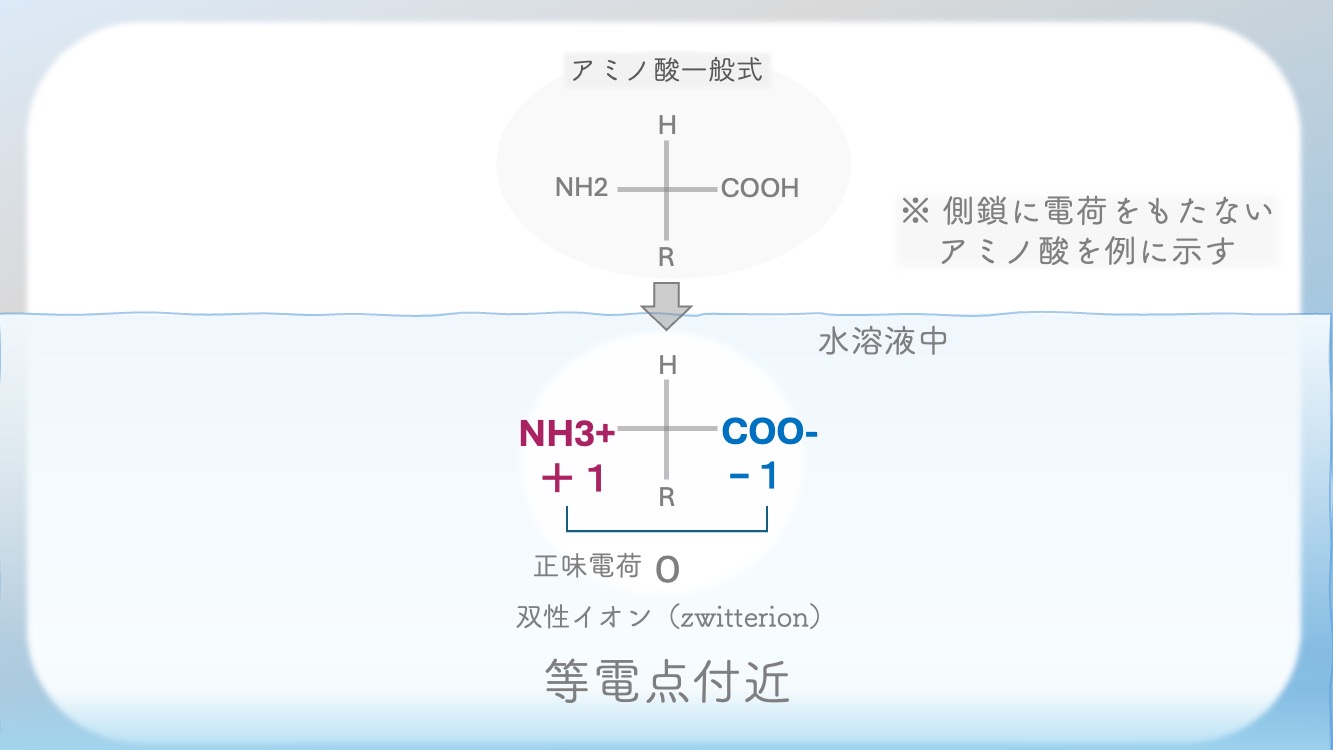
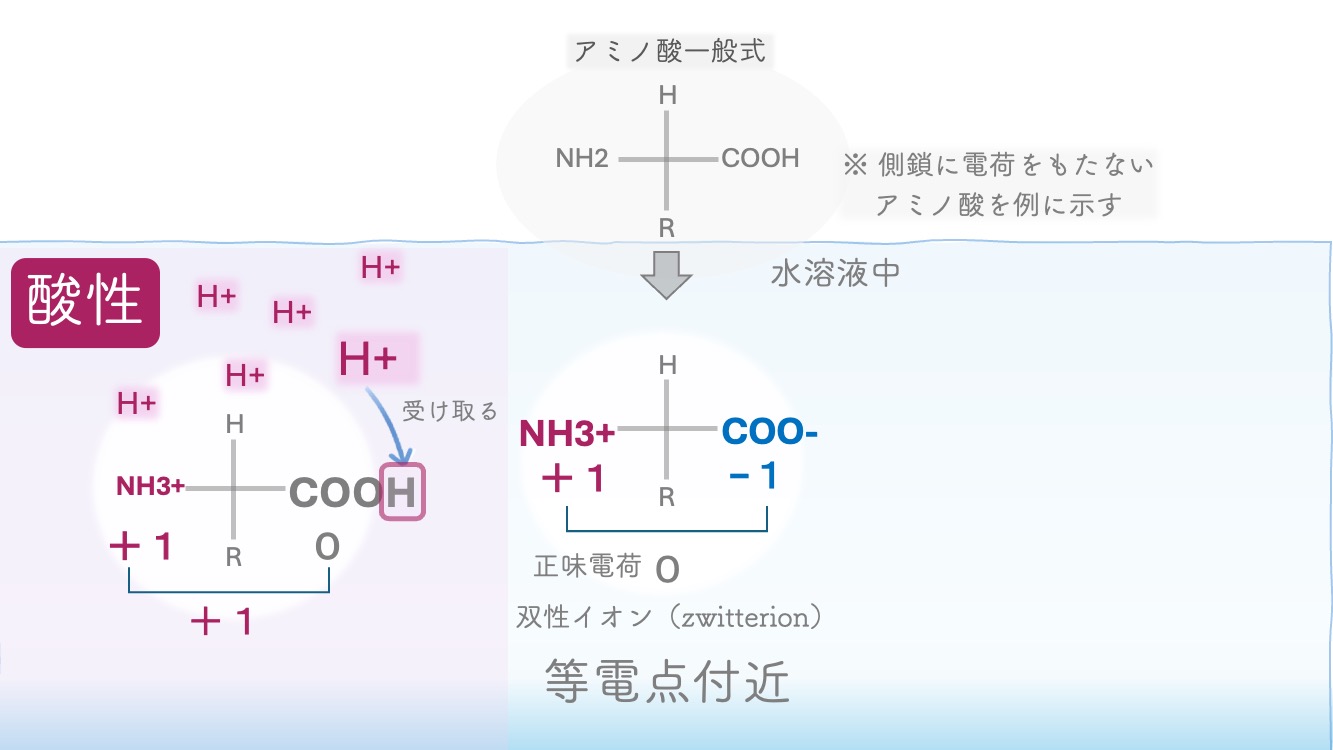
アミノ酸は中性付近の水溶液の中では
NH3+とCOO-の状態で存在するよ。
あ、思い出した。
水の中では、その形が多いんだよね。


そう。
酸性、つまり pH が低いと、H⁺ が多い。
だからアミノ酸は、H⁺ を受け取った形に
なりやすいんだ。
H⁺ がたくさんあると、
受け取るほうに傾くのか。

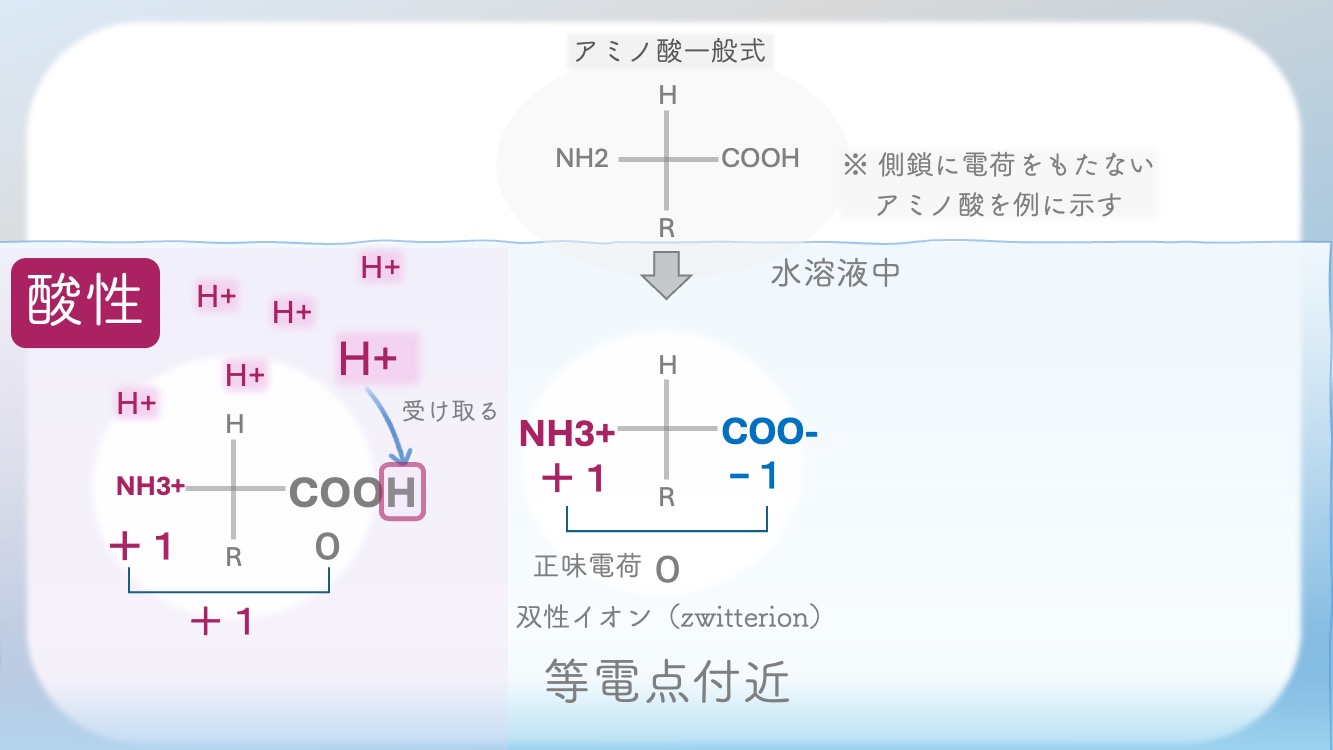

逆に、pH が上がると、H⁺ は少なくなる。
だからアミノ酸は、
少しずつ H⁺ を手放していくよ。
なるほど。
今度は持っている H⁺ を手放していくんだね。

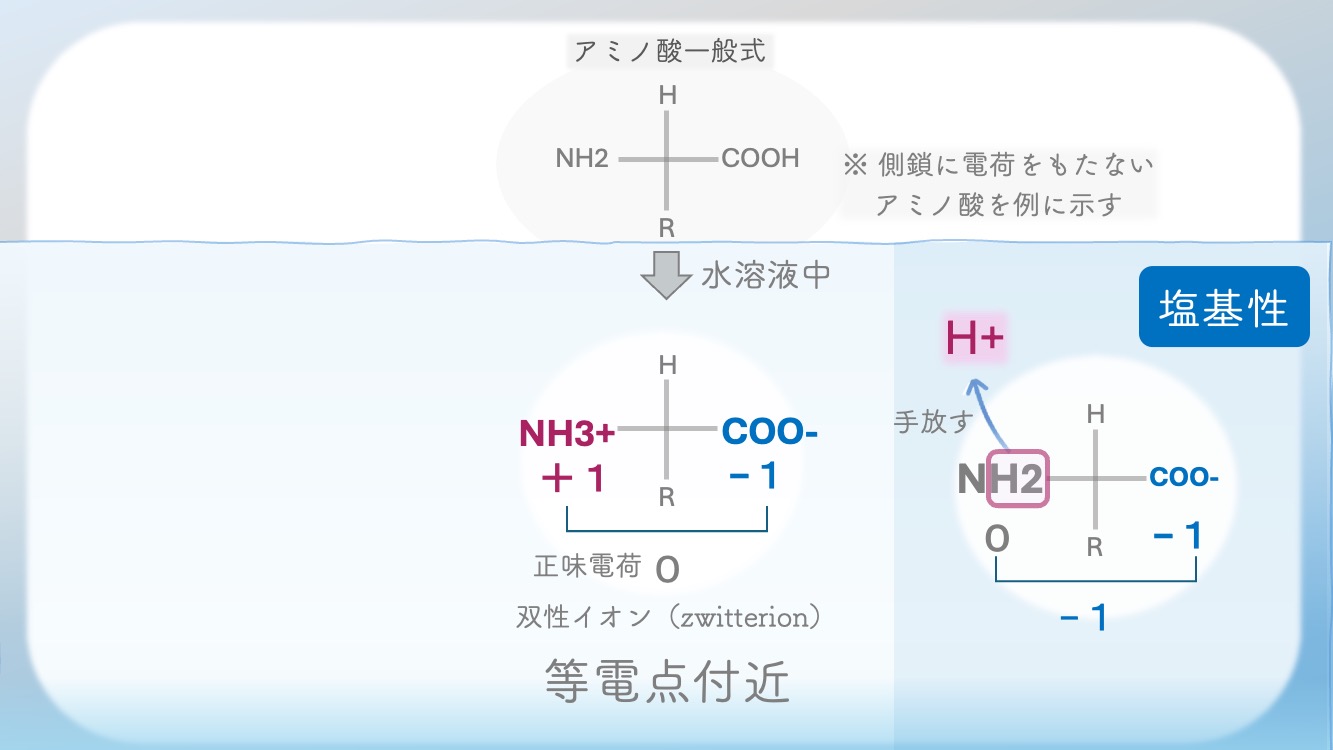

COO-はH+を受け取れる場所。
NH3+はH+を手放せる場所。
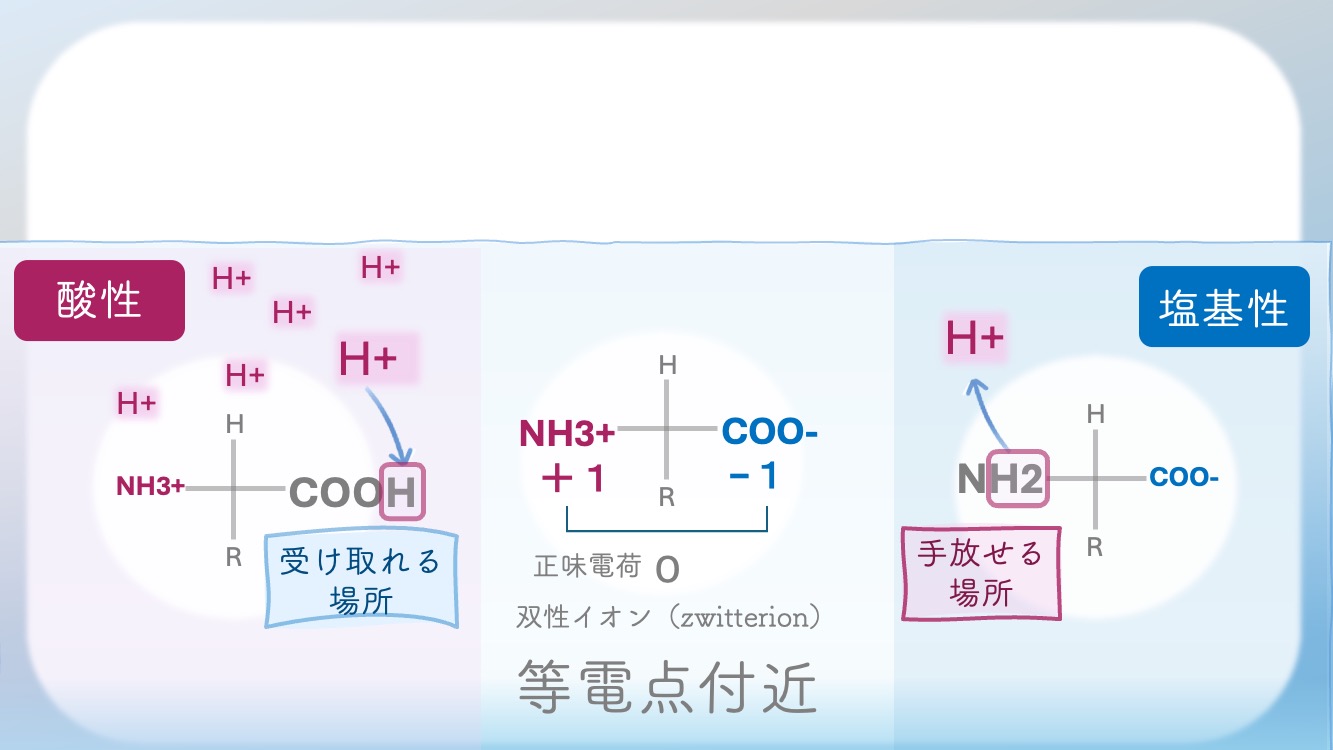
それぞれの”場所”の意味を
ここでしっかり確認しよう!

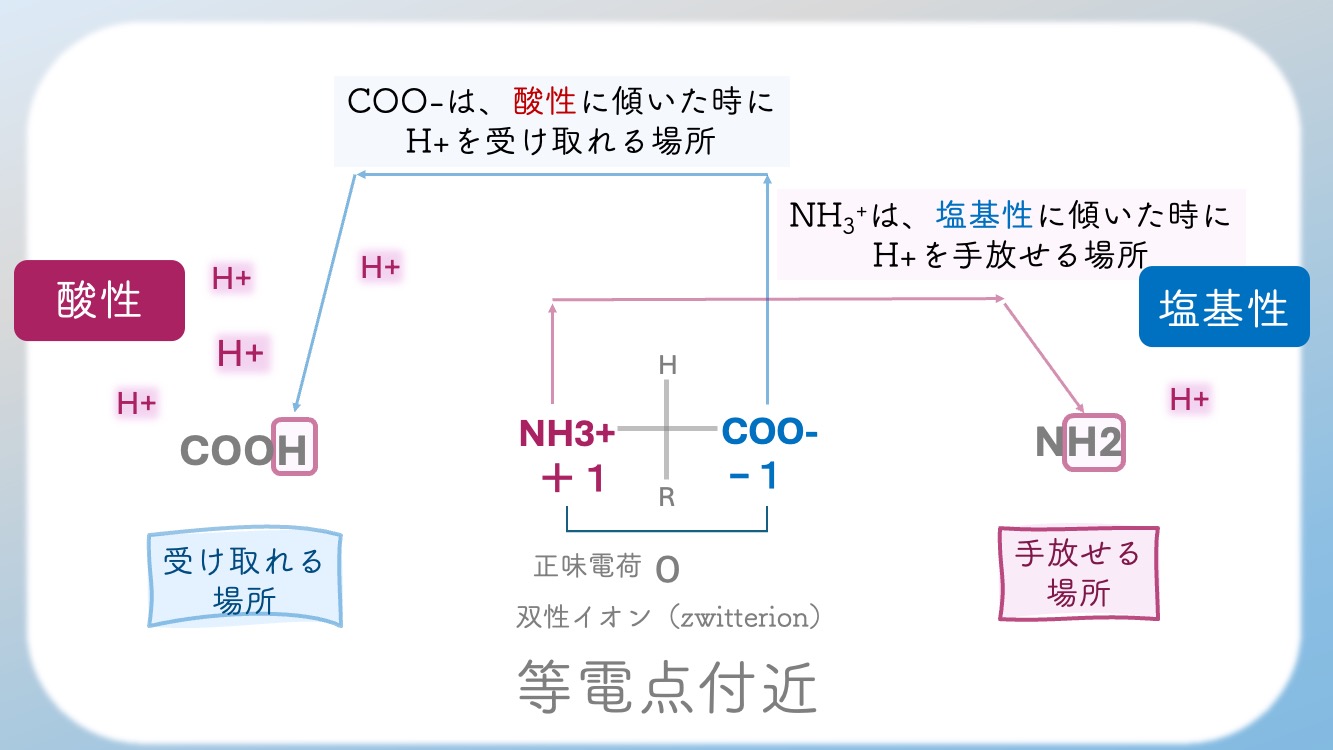

電気的なバランスはこんな感じ。
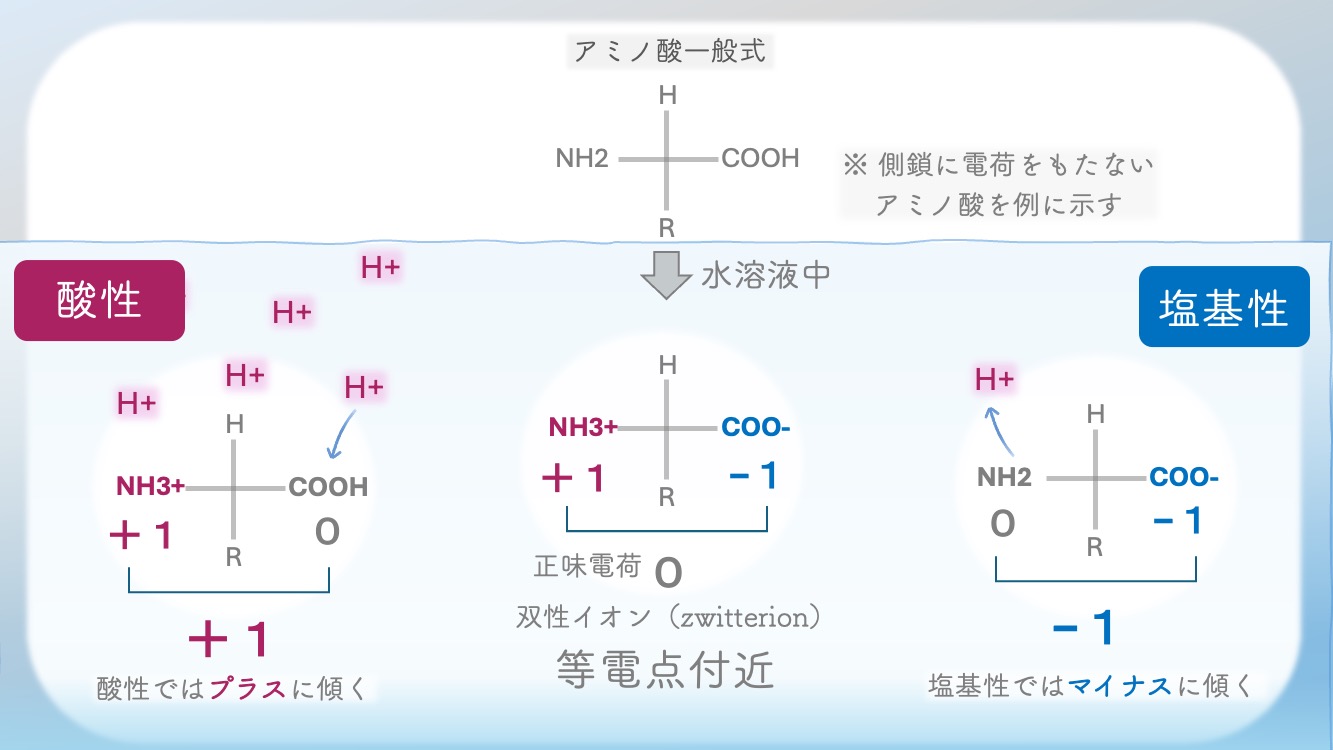

・H+がたくさんあると、
H+を受け取るからプラスに傾く。
・H+が少ししかないと、
持っているH+を手放すからマイナスに傾く。
周囲のH+に応じて、プラス寄りになるか、
マイナス寄りになるかが変わるんだ。

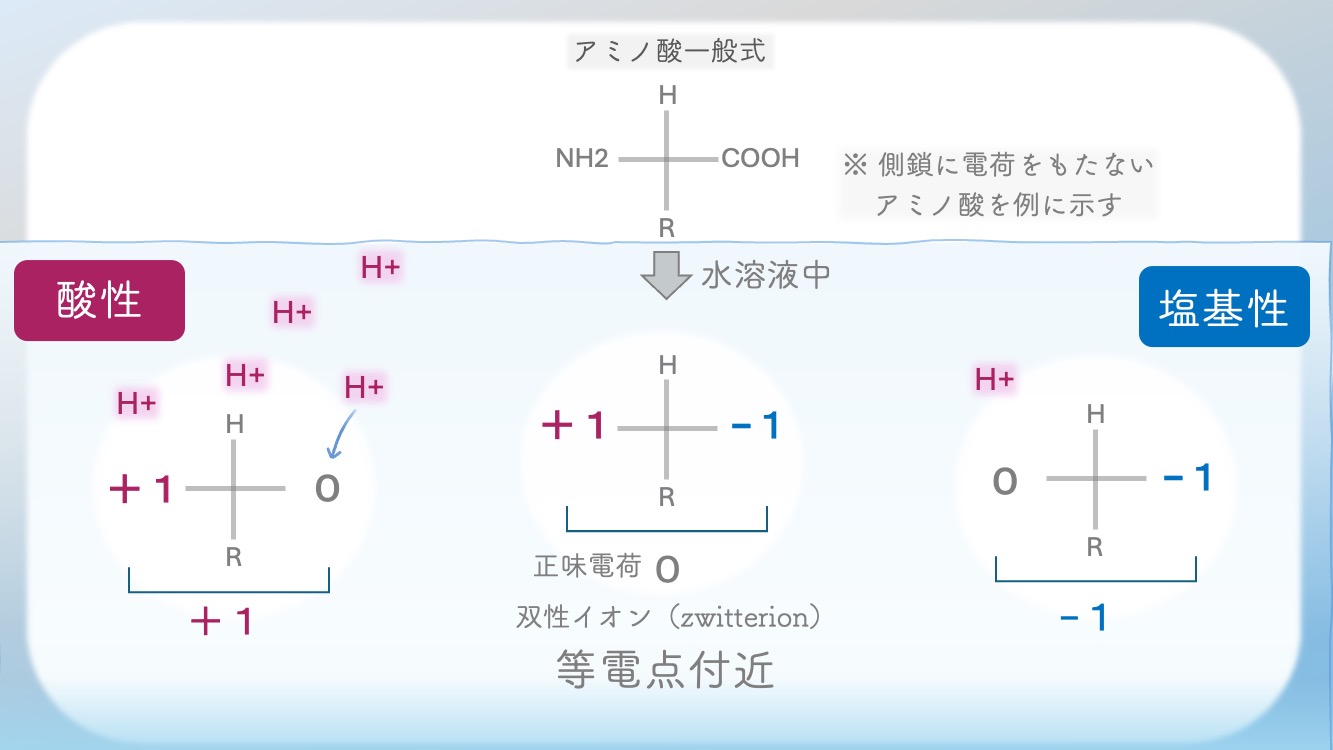

要するに、COOーとNH3+はこんな風に変化するんだ。
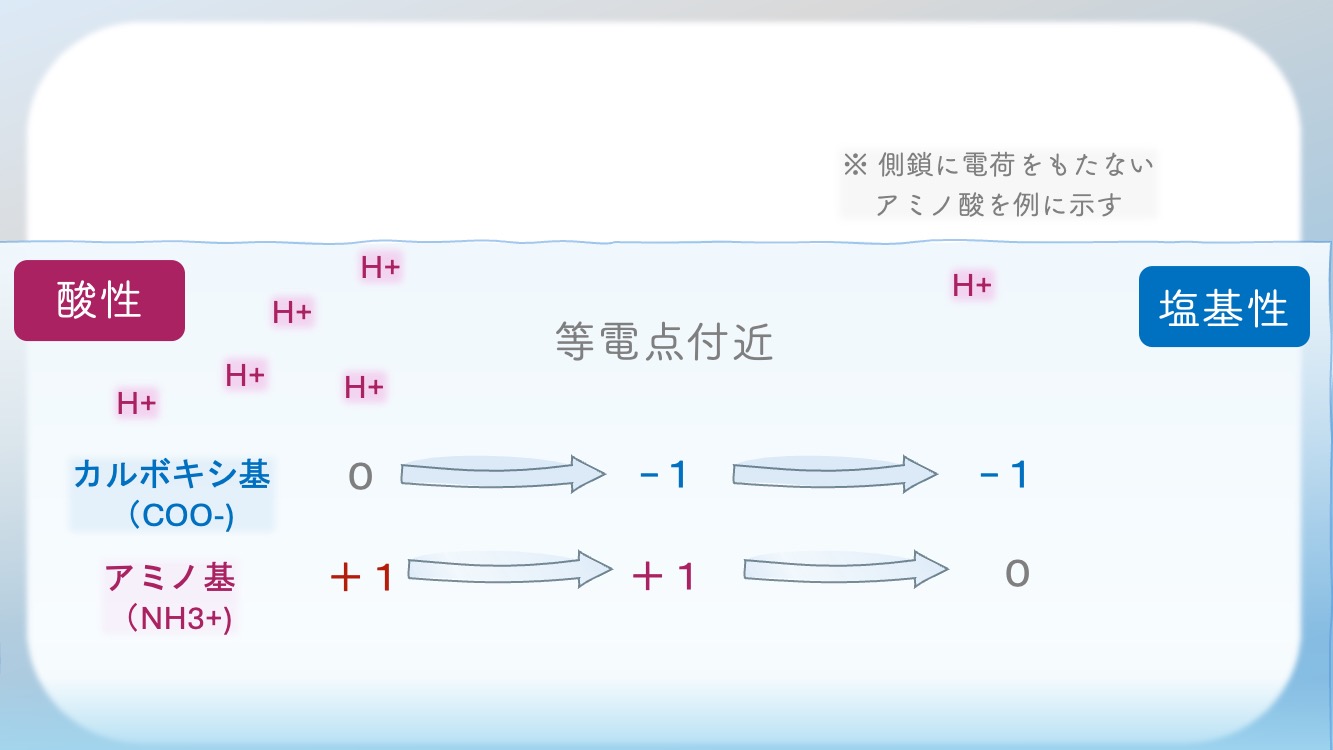

アミノ酸滴定曲線は、
この H⁺ の出入り を線で見せている図なんだ。
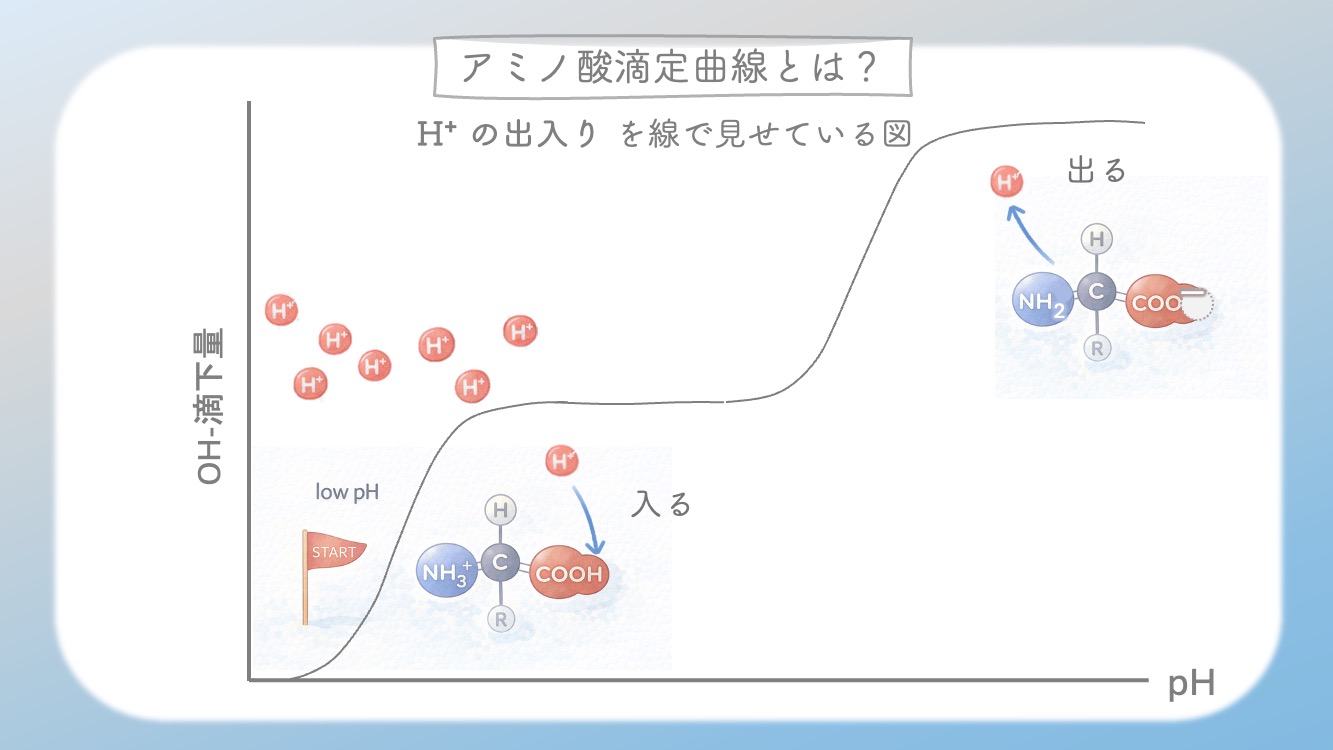

今回は、
横軸を pH、
縦軸を OH⁻ の滴下量に
しているよ。
酸性の溶液からスタートして、
それにOH⁻を少しずつ加えると、H+が中和されるから
溶液は酸性からだんだん中性→アルカリ性に変わっていく。
そのとき、アミノ酸のイオン性がどう変化するのかを
見ているよ。

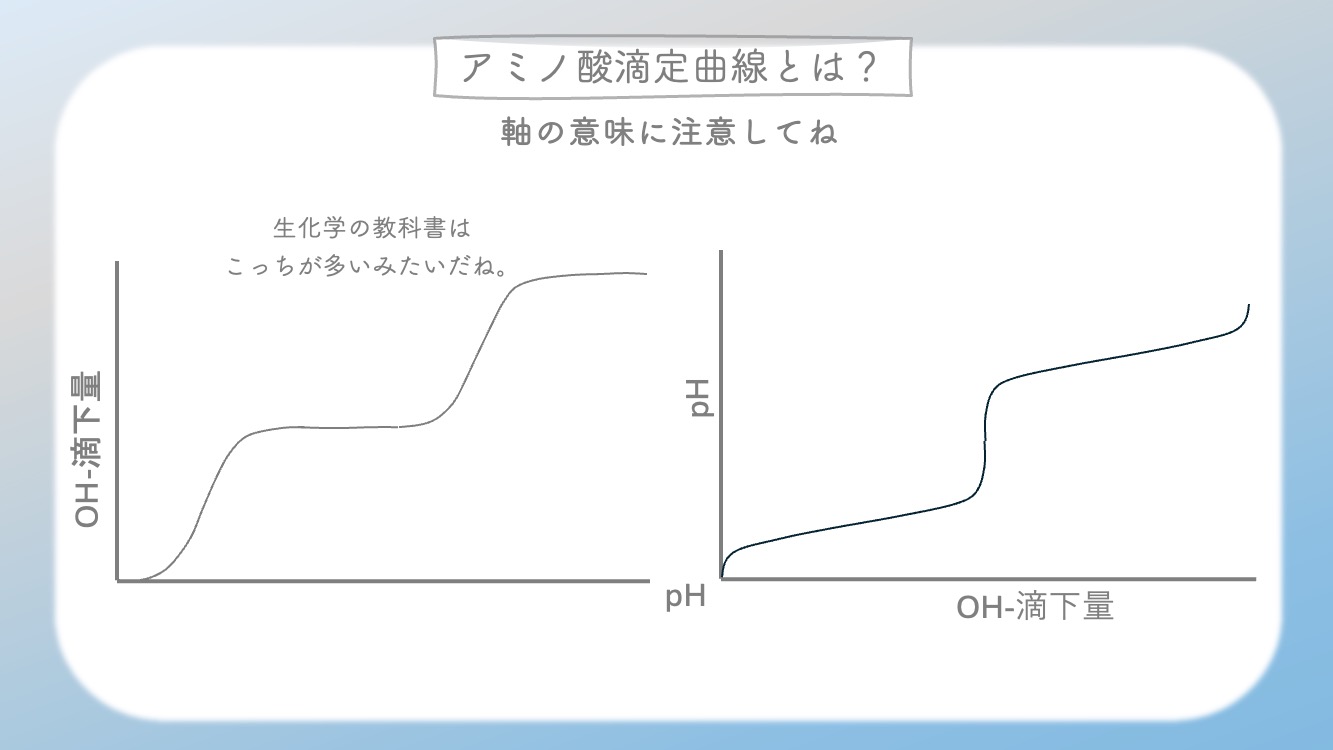
ただし、教科書や問題集では、
横軸が OH⁻ の滴下量、縦軸が pH のグラフも
よく出てくるよ。試験では、軸の意味を取り違えないように
気をつけてね。
同じ滴定曲線でも、軸が逆のことがあるんだ。
そこはちゃんと見ないと危ないね。

3. いちばんシンプルな グリシンで意味をつかむ
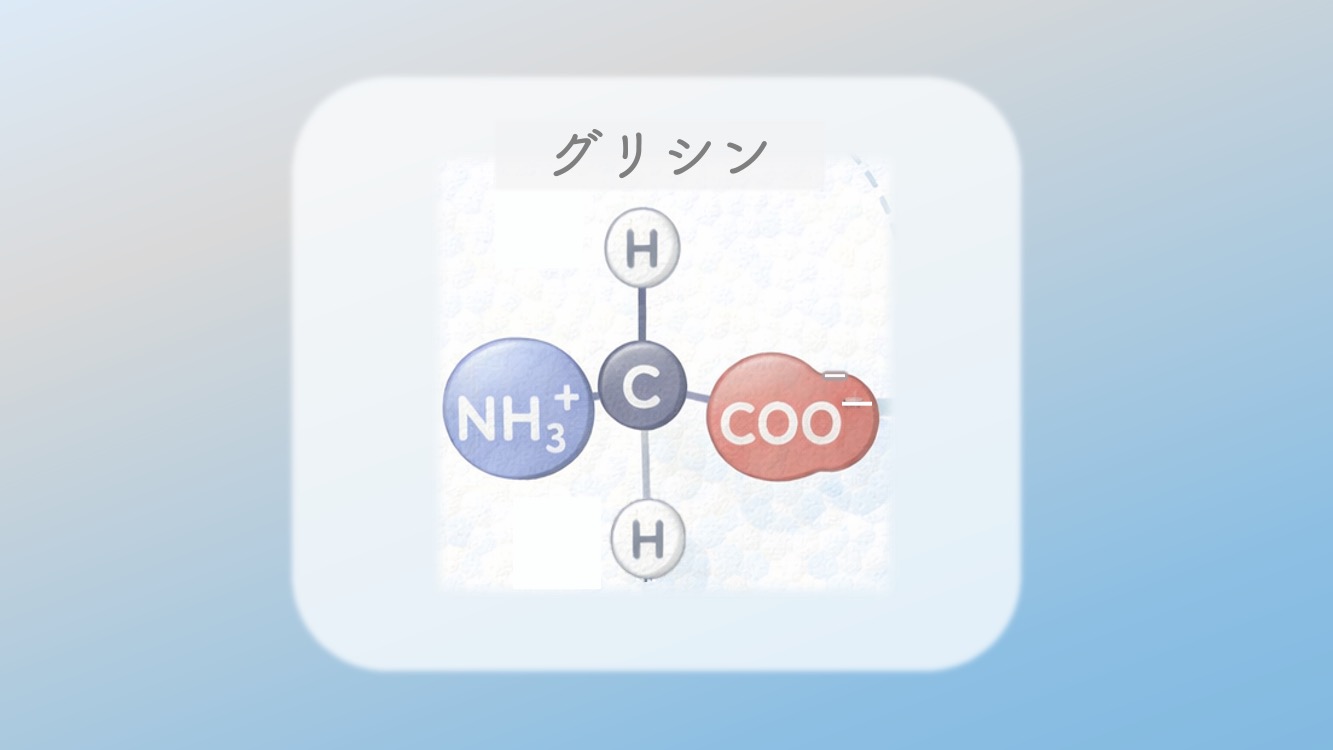
グリシンは、基本のアミノ酸の形に、
側鎖は ”Hだけ” だったよね。


その通り。
グリシンは、側鎖がいちばんシンプルなんだ。
アミノ酸の基本を考えるときの出発点にしやすいんだよ。

グリシンの滴定曲線を読む上で
注目すべき主な場所は2つ。
・COO-
・NH3⁺
まずはその2か所を見ればいいんだね。


うん。ではまず、pH がとても低いときを考えよう。
pH がとても低いというのは、
まわりに H⁺ がたくさんある、ということなんだ。
H+が周りにたくさんあると、
グリシンは H⁺ を取り込みやすいんだね。


その通り。低い pH では、
グリシンは H⁺ をしっかり持った形になりやすい。

つまり、H⁺ を受け取れる側も、
H⁺ を手放せる側も、
どちらも H⁺ を持った形になりやすいんだ。
ということは、
COOH と NH3⁺ の形ということ?


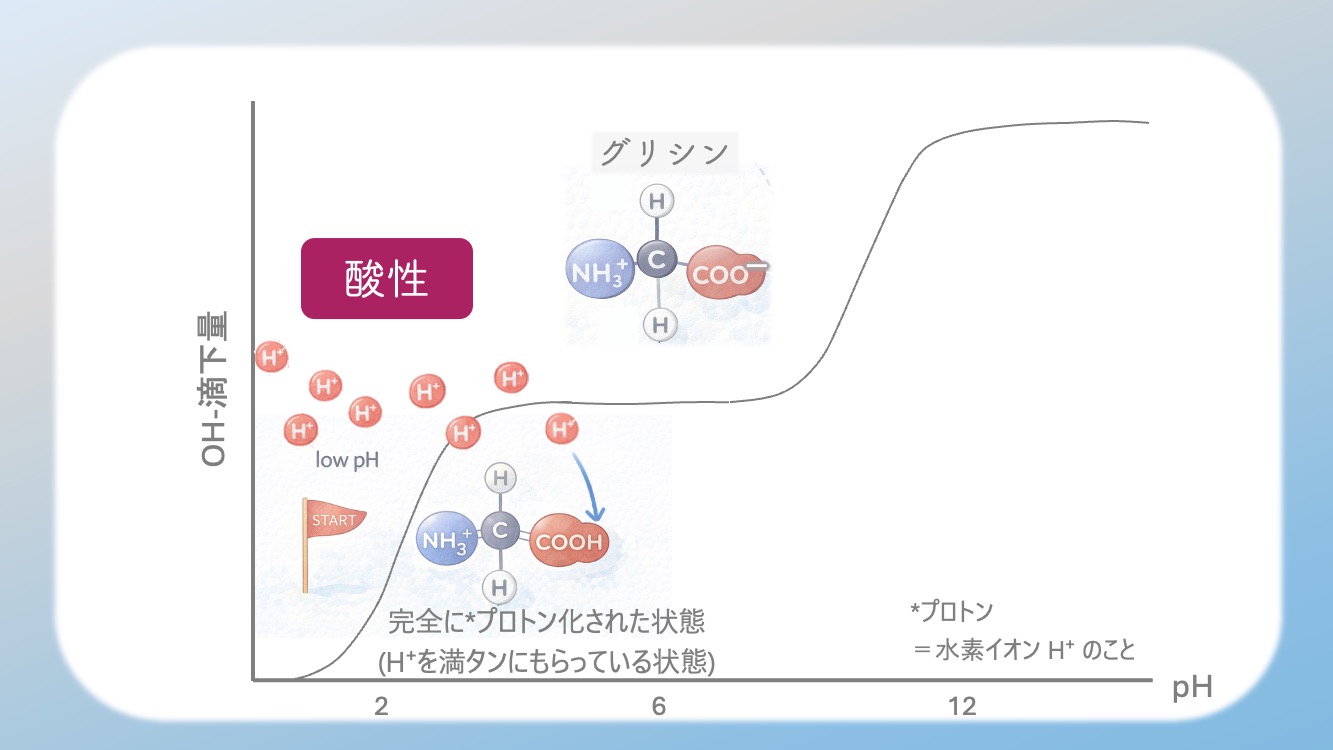
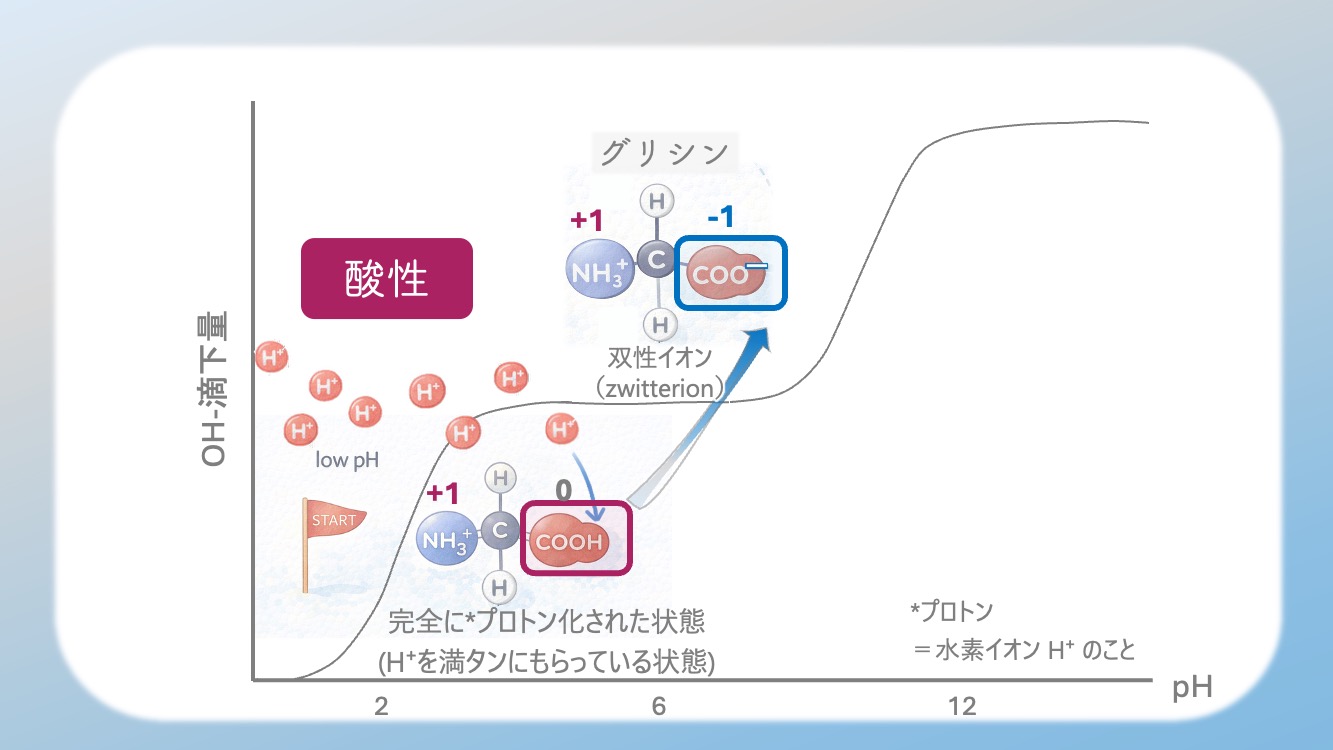
そう。つまり最初は、
完全にプロトン化された状態なんだ。
言いかえると、
受け取れるだけの最多の H⁺ を受け取った状態だよ。

滴定曲線の左端は、
H⁺ をたくさん持ったスタート地点 と考えるといいよ。
なるほど。
左端は、プロトンが多い。
だから最もプロトン化された状態で出発する
んだね。

4.最初に変わるのは COOH。一気に理解が進む

ここから pH を上げていくと、
まず最初に変化しやすいのは
COOH なんだ。
最初は COOH から変わるんだね。


そう。
前のブログ記事
「アミノ酸のイオン性」でも話したけれど、
COOH の H⁺ は、
もともと COO⁻ から離れやすいんだ。

だから、H⁺がたくさんあるときは我慢しているけど、
まわりの H⁺ がだんだん少なくなると、
待ってました!とばかり
H⁺ がCOOH から外れようとするんだ。
へえ。
酸性から塩基性へ向かうとき、
もともと外れやすい
COOH からH+が外れるんだね。


その通り。そしてこのとき、
NH3⁺ はまだ H⁺ を持ったままなんだ。

NH3⁺ は、H⁺ をつけたままのほうが
絶対に安定、という意味ではないよ。

でも、その pH では、
H⁺ をつけたままでいるほうが有利というか、
楽なんだ。
だから、酸性から中性へ向かう途中では、
COO⁻ と NH3⁺ を両方持つ形になるんだ。


そう。これが
両性イオン(双生イオン・zwitterion) だよ。
プラスもある。
マイナスもある。
でも全体としては net charge 0。


言い換えると、
分子全体としては正味電荷は 0。

等電点では、
この両性イオンがいちばん多くなるんだ。
へえ。
プラスもマイナスもあるのに、
全体では 0 なんだ。

5.【最重要】pKa と緩衝域が ここでつながる

ここで、滴定曲線の見方が少し見えてくるよ。
最初の段差は、
COOH から H⁺ が外れていく変化 を
表しているんだ。
そしてその変化の真ん中あたり、
つまり 半分くらい外れたところ が
pKa なんだよ。
なるほど。
pKa って、どの pH で
その H⁺ が半分くらい外れるかを表す数値なんだね。


そう。pKa とは、
H⁺ の外れやすさを表す値だよ。
たとえば、pKa が小さいということは、
低いpHでH+を離すということ。
つまり「H⁺ を持ち続ける」より「H⁺ を放す」ほうに
傾きやすい、ということなんだ。

ブレンステッドの定義では
酸 = H⁺ を与えるものだったよね。
言い換えれば、H⁺ を手放すものと言える。
pKa が小さいとは、
より低いpHでH+を離すということ。
つまり、酸としてふるまいやすい傾向があるとも言えるね。
その結果、マイナス電荷をもつ形が増えやすい。
ただし大事なのは、
必ずしも物質全体がマイナスになるとは限らない、
ということなんだ。
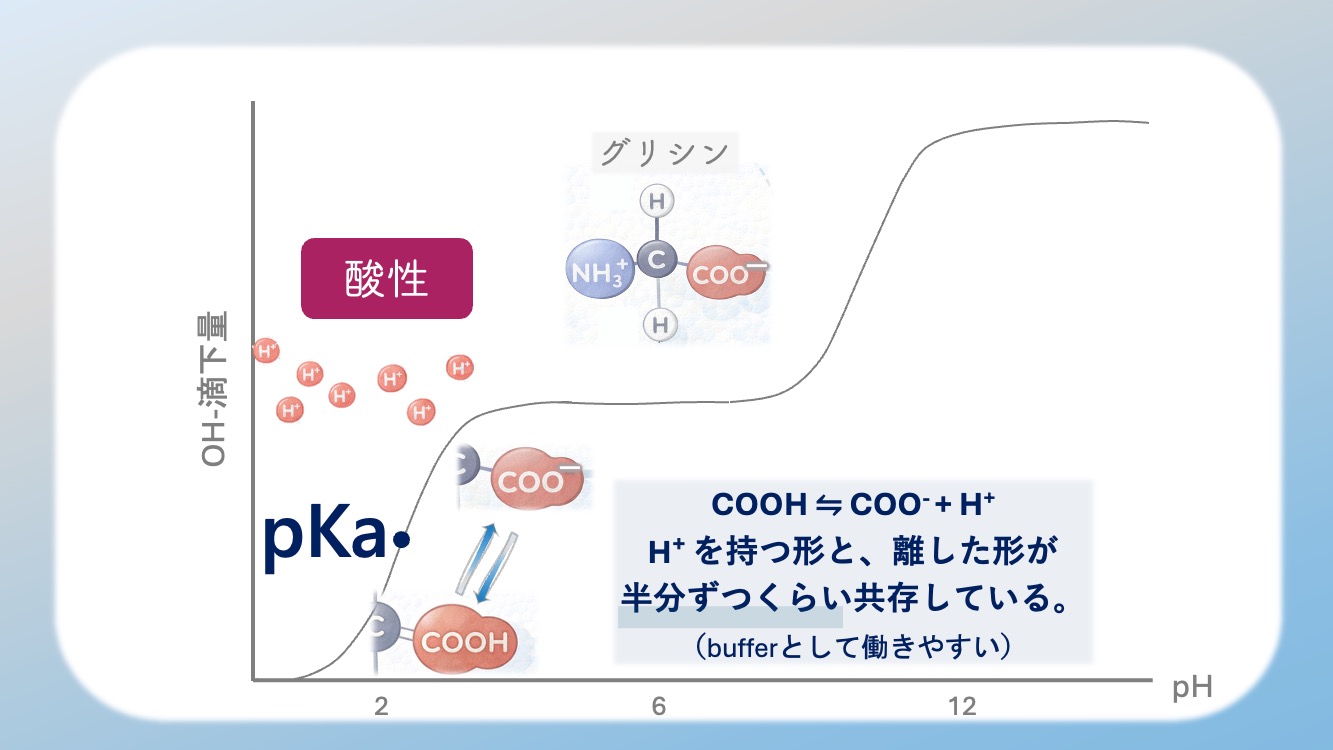
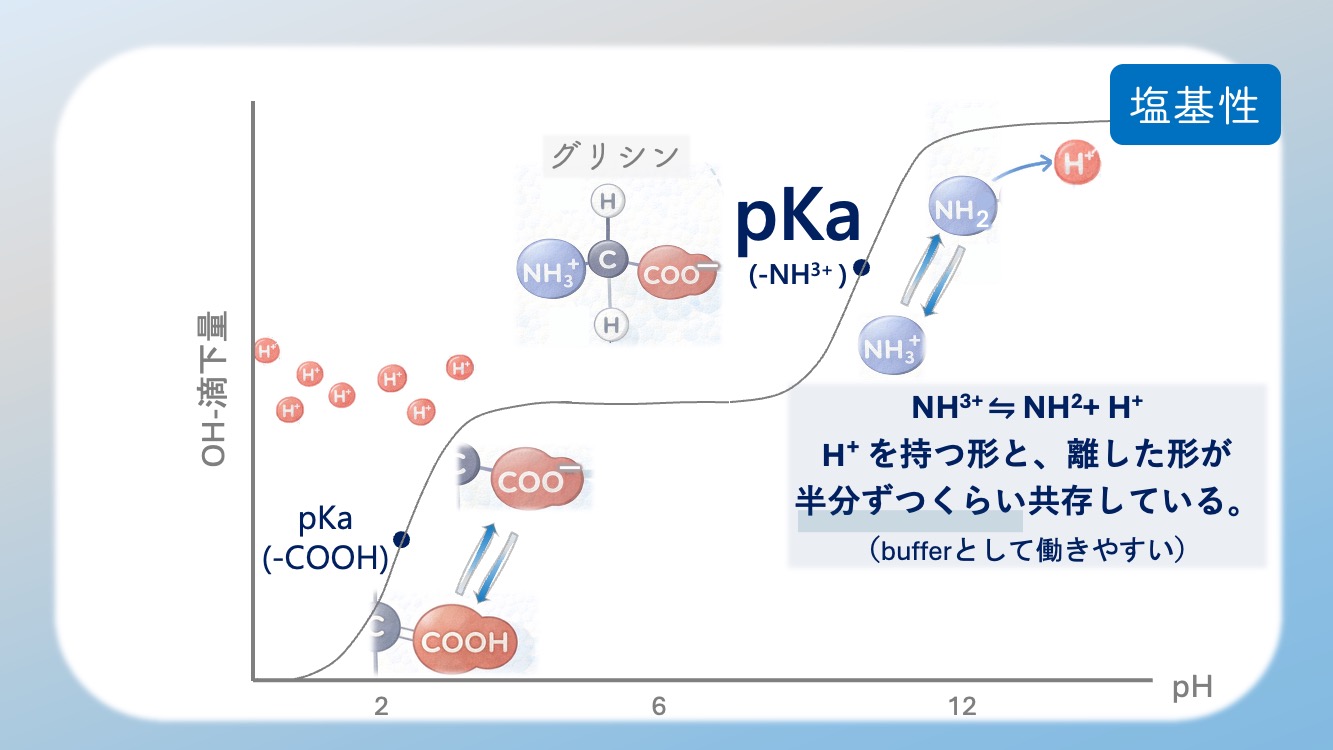
緩衝作用とは?

pKaの付近では
H⁺ を持つ形と、離した形が
半分ずつくらい共存している。

だから buffer として働きやすい、
つまり緩衝作用が大きいんだよ。
緩衝作用が大きいって、どういう意味なの?


酸やアルカリが少し入ってきても、
pHが急に変わりにくい
という意味だよ。
pHが急に変わりにくい?


たとえば、ふつうの水は、
少し酸やアルカリが入ると pH が変わりやすい。

でも 緩衝作用があると、酸が少し入っても、
すぐには強く酸性にならない。アルカリが少し入っても、
すぐには強くアルカリ性にならない。

つまり、緩衝作用は
「pHのゆれを小さくするクッション」
のようなものなんだよ。
ああ。
急に変わりすぎないようにしてくれるんだ。


そう。アミノ酸でいうと、
H⁺を受け取れる形 と H⁺を放せる形 の両方が
ほぼ同じ量でいるとき、
緩衝作用が大きいんだ。
あっ!だから pKa の近くなんだね。


そう。
pKa の近くでは
H⁺ を受け取る
H⁺ を放す
その両方に対応しやすく、
pHを変わりにくくできるんだよ。
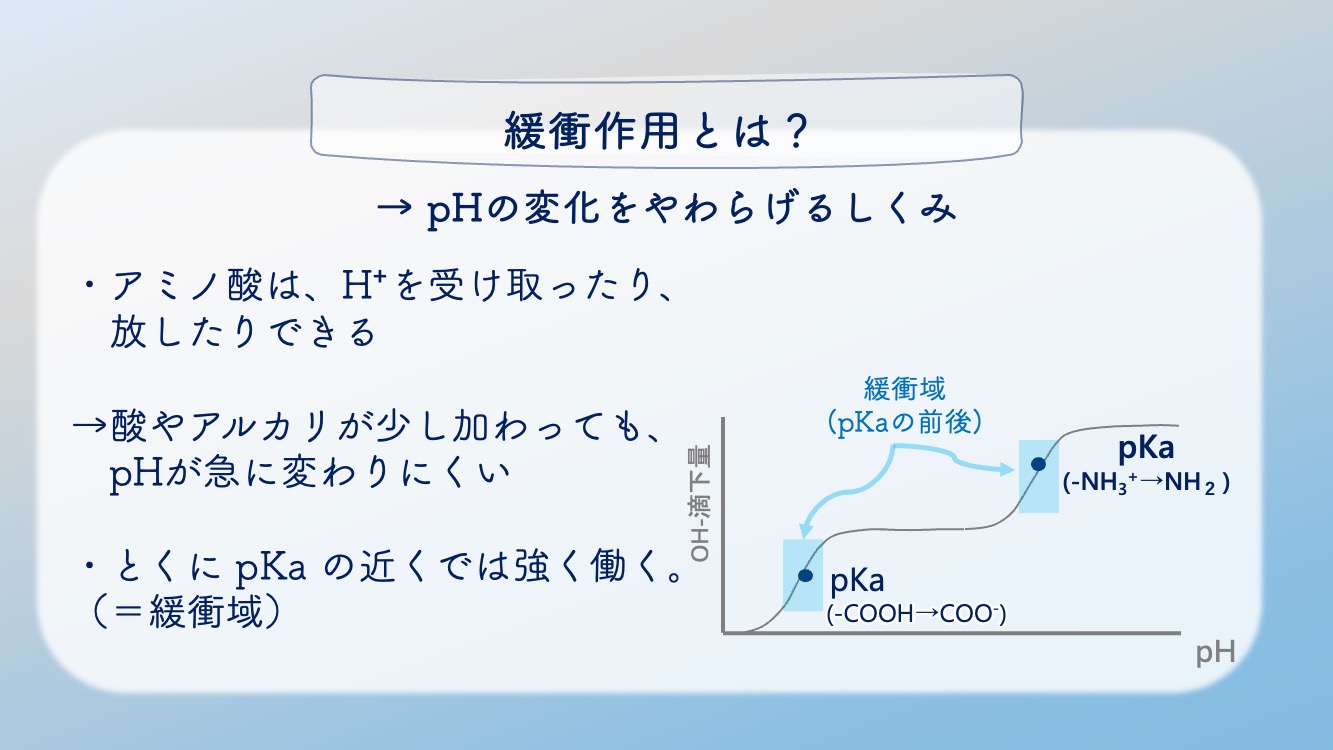

そして、pKa のおよそ ±1 pH のところを、
緩衝域 と呼ぶよ。
なるほど。
pKa の近くで、緩衝作用が大きいところ が、
緩衝域 なんだね。

6.次に動くのは NH3⁺。 2つ目の段差

さらに pH を上げていくと、
今度は NH3⁺ が H⁺ を離すよ。
へえ。
今度は NH3⁺ のほうが変わるんだね。


そう。この時点では、
すでに COO⁻ になっているので、
NH3⁺ が H⁺を手放すと
全体としてはマイナスが強くなる。

つまり、pH が高い側では、
OH⁻ を加えるにつれて、グリシンはしだいに
負に帯電していくんだ。
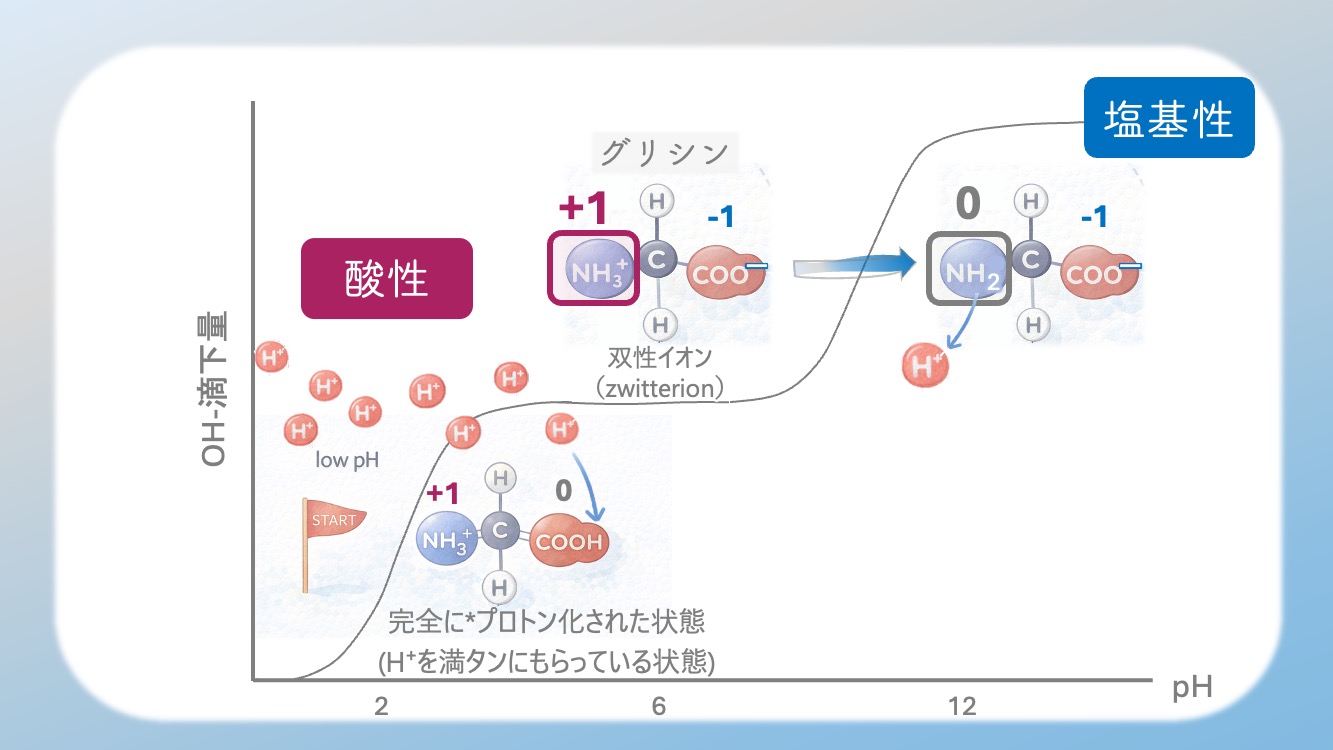

ここで2つ目の段差ができる。
そして、その真ん中あたりに、
もう1つの pKa があるよ。
へえ。
NH3⁺ の pKa は約 9.6 なんだね。
COO-と比べてpKaが高いね。
かなり塩基性に傾かないと、
H⁺ が外れないということだね。

7.なぜ S字なのか。 段階ごとの脱プロトン化で見る

では、なぜ滴定曲線は
あの独特な S字 になると思う?
ゆるやかに変化する理由?


そう。その理由はシンプルだよ。
それは、H⁺ が一気に
全部外れるわけではないからなんだ。

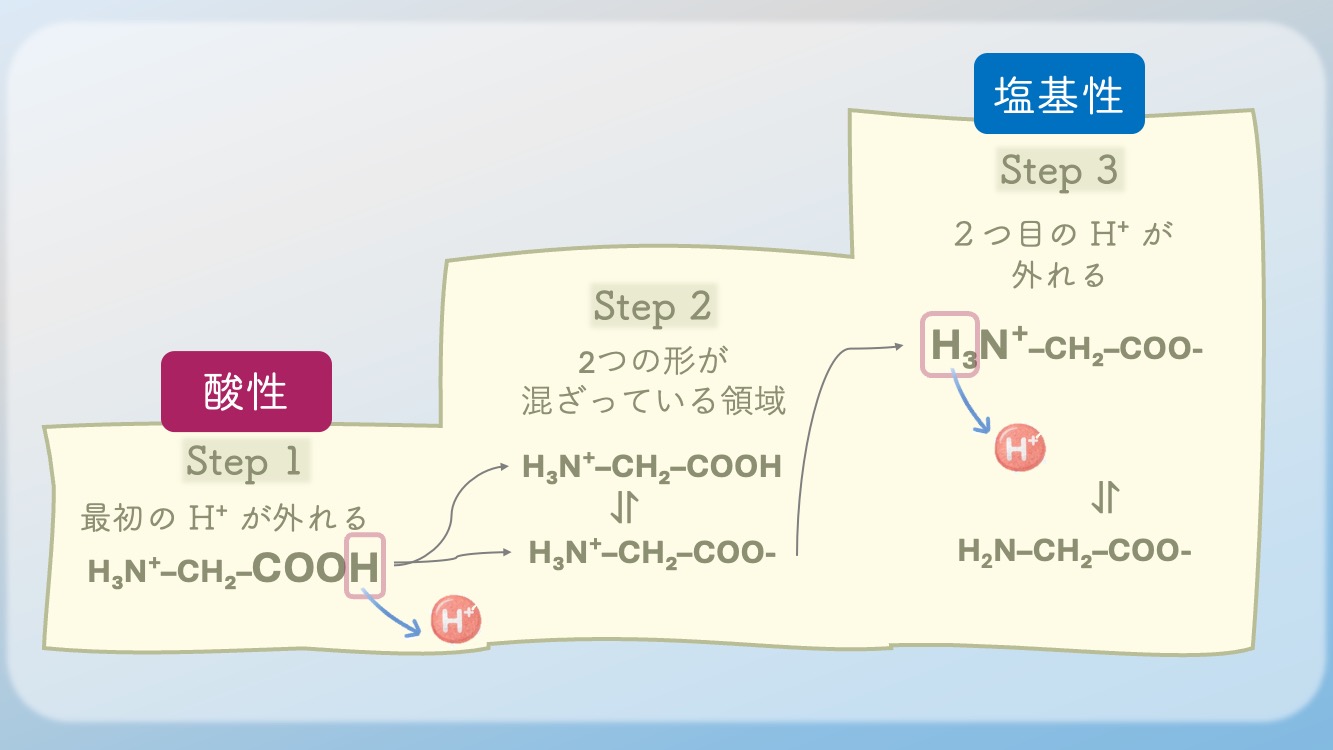
最初に外れやすい場所がある。
次に外れる場所がある。
その途中には、
半分ずつ混ざる領域がある。
この変化が、
なだらかな部分 と
立ち上がる部分 を作るんだよ。

だから滴定曲線は、
段階ごとの脱プロトン化の記録
と言えるね。
一気に全部じゃなくて、
順番に外れていくからなんだね。

8. 等電点は“なんとなく真ん中”ではない

ここで、よく混乱する 等電点 を整理しよう。

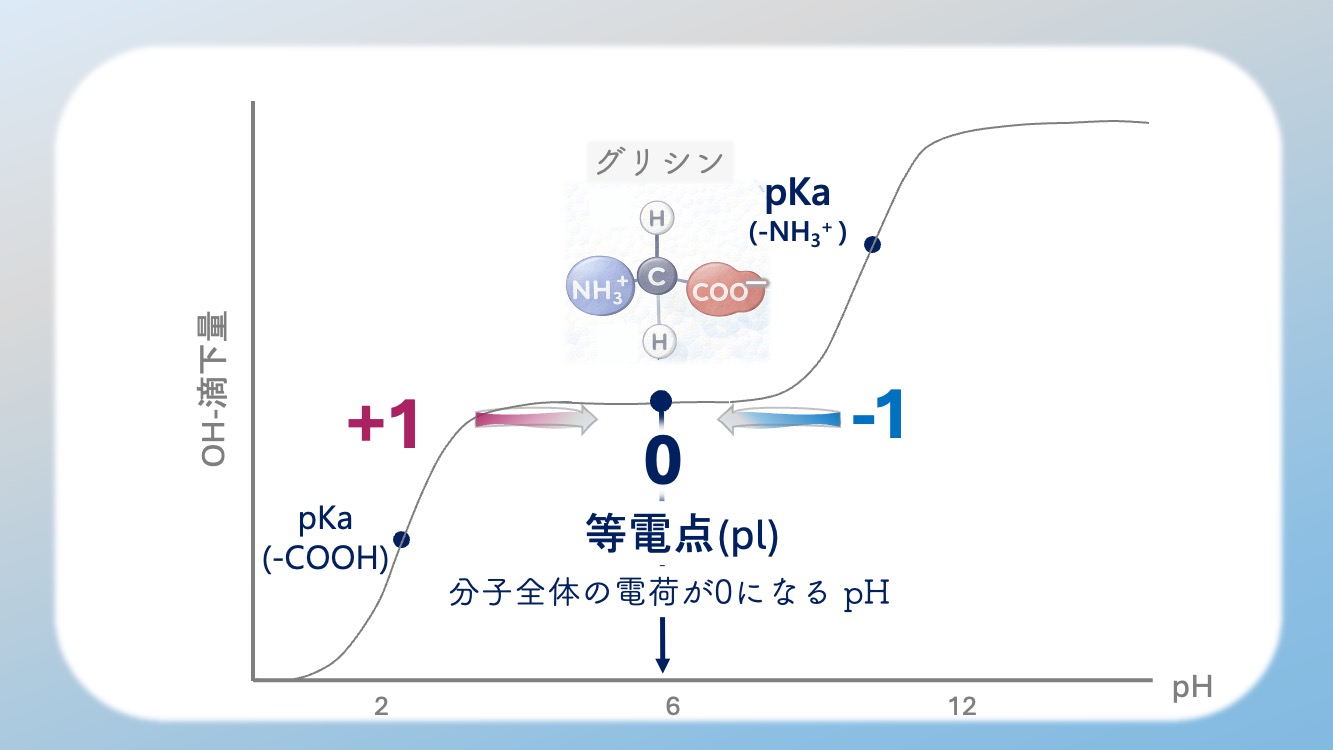
等電点、つまり pI は
分子全体のnet chargeがゼロ、言い換えると
正味電荷が 0 になる pH のことなんだ。

グリシンでは、
それは 両性イオン(双性イオン・zwitterion) が
いちばん多いあたりになるよ。

グリシンで両性イオンが多いあたりが等電点になるのは、
その形が、
分子全体としてちょうど正味電荷 0 だからなんだ。
じゃあ実際に等電点って
計算でも求められるの?


グリシンのように、
正味電荷 0 の形をはさむ pKa が 2つある場合は、
pI = (pKa1 + pKa2) / 2 で求めるよ。
グリシンなら、
pI = (2.34 + 9.60) / 2 = 5.97 だね。
大事なのは、
全部の pKa を足すのではなく、
正味電荷 0 の形をはさむ 2つの pKa を使う
ことだよ。
つまり、最初の pKa と
2つ目の pKa の
ちょうど間くらいに、
pI が来るってこと?


そのとおり。
ここで大事なのは、
等電点は「なんとなく真ん中」ではなく、
電荷が打ち消し合う形が中心になる場所
ということなんだよ。
見た目の真ん中じゃなくて、
電荷が 0 になることが大事なんだね。

9. 試験ではこの3つ。 “どこがいつ変わるか”を見る

では、試験ではどこを見るのか。
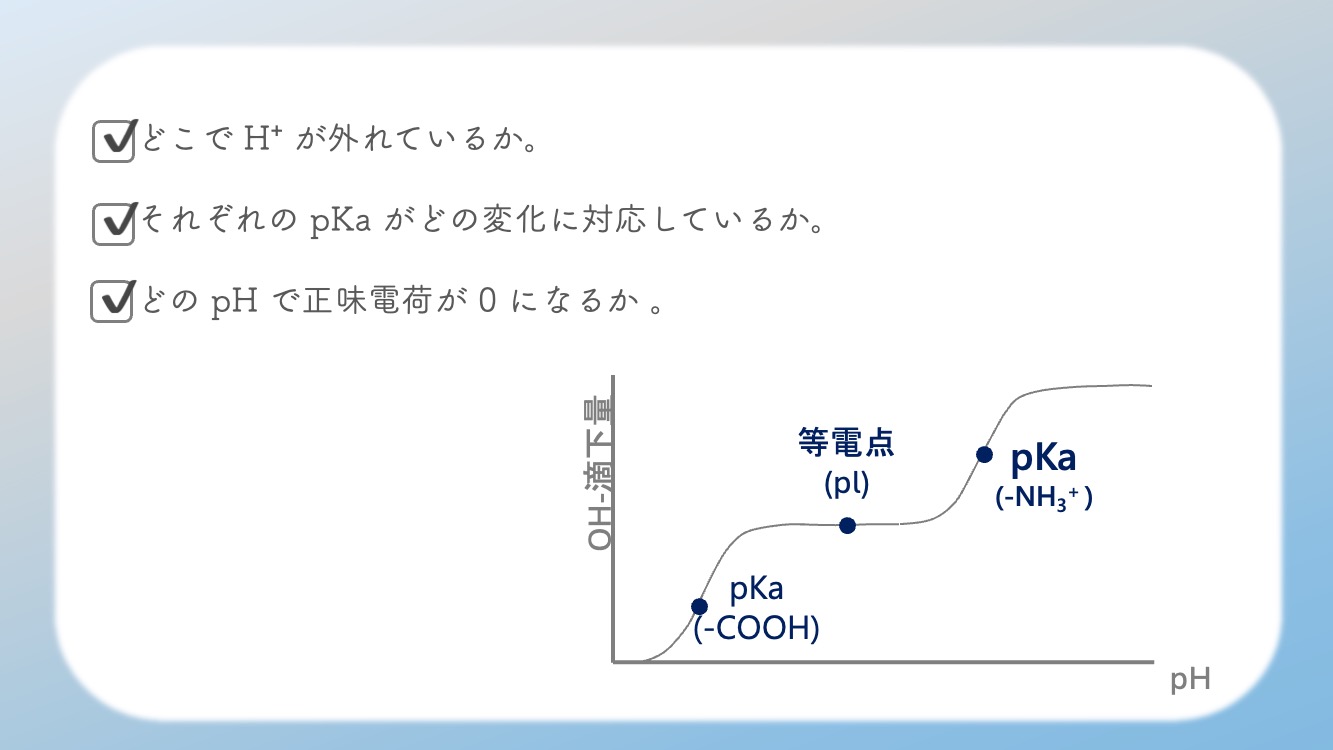
まず見るべきはこの3つだよ。
1つ目:どこで H⁺ が外れているか。
2つ目:それぞれの pKa がどの変化に対応しているか。
3つ目:どの pH で正味電荷が 0 になるか。

つまり、
滴定曲線は「形」を覚えるのではなく
どの部位がいつ脱プロトン化するか
を追うことが、得点につながるんだ。
たしかに。
今日一緒に勉強したことで
その考え方が身についたよ。

10. ここだけ押さえれば大丈夫。 グリシン 滴定曲線の最短ルート

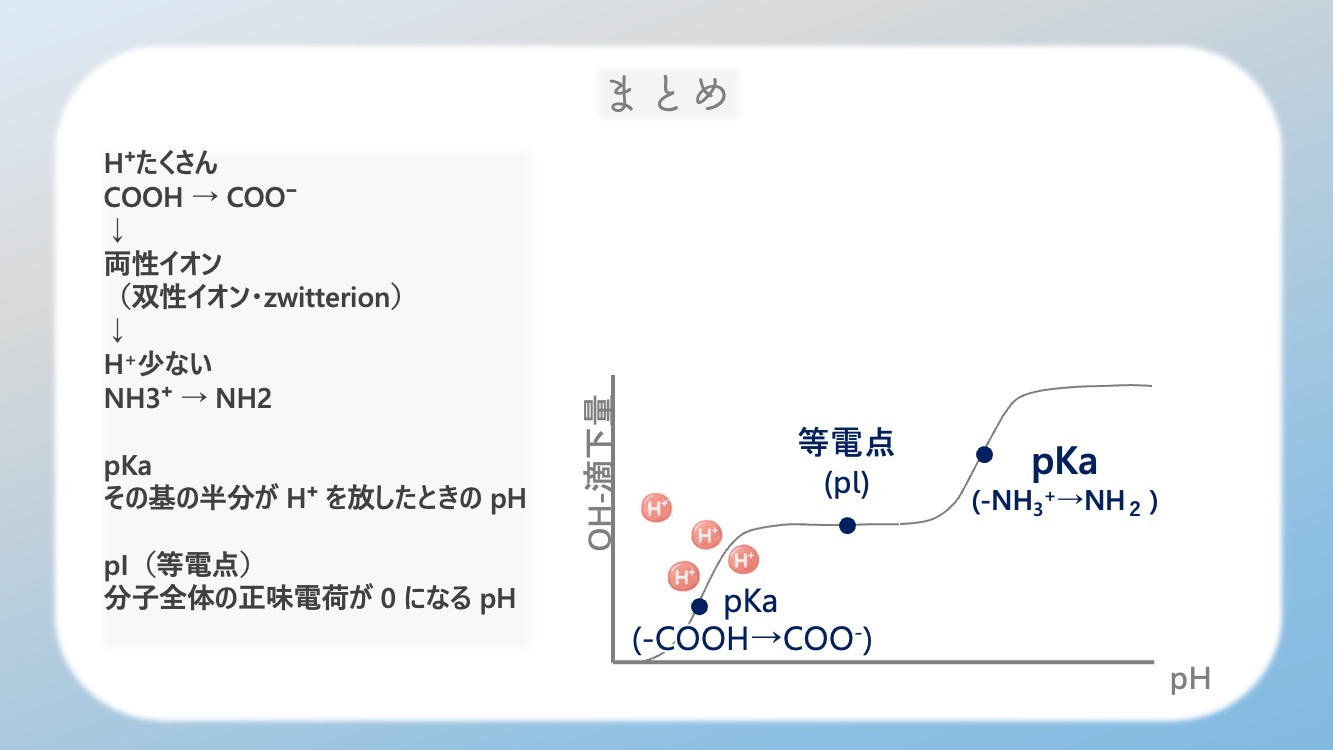
ここまでを、超圧縮するとこうなるよ。
・低い pH では、H⁺ をたくさん持っている。
・最初に COOH から H⁺ が外れる。
・中間で 両性イオン(双性イオン)zwitterion になる。
・次に NH3⁺ から H⁺ が外れる。
・pKa は半分ずつの点。
・pI は net charge 0 の点。
おお。
こう並ぶと、流れがすごく見やすいね。

11. 🍀ブログ特典 豆知識
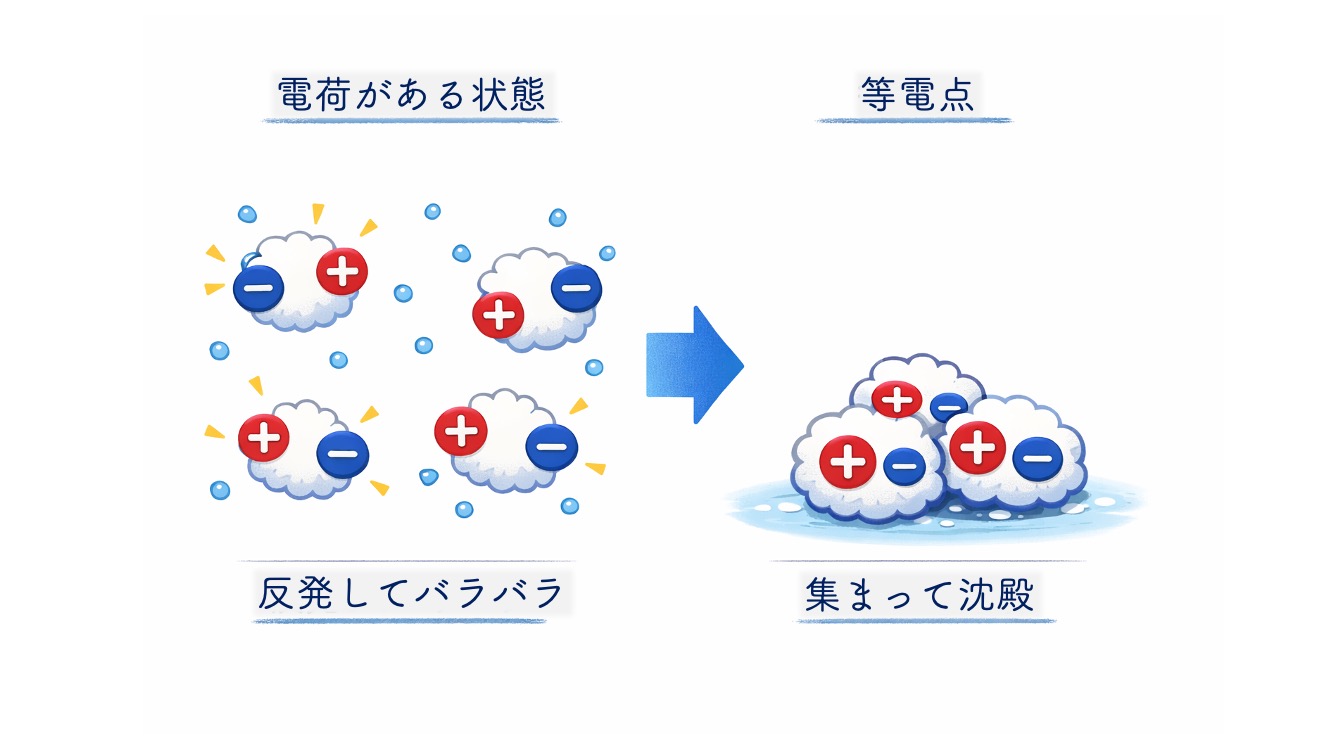
等電点で、なぜタンパク質は集まりやすくなるの?

こはく。
アミノ酸と同じように
タンパク質にも等電点があるんだよ。
タンパク質にも等電点があるの?


そう。
タンパク質の等電点
= たくさんのアミノ酸が集まった
全体の電荷が 0 になる pH
そして等電点の付近では
タンパク質が集まって沈殿しやすい。
えっ?
等電点だと、どうして
タンパク質は集まりやすくなるの?


わかりやすく説明するね。
アミノ酸やタンパク質には、
プラスやマイナスの電荷があるよね。
この電荷があるおかげで、
分子どうしは反発し合い、
水の中でも散らばって存在しやすいんだ。
電荷があると、例えば磁石のプラスとプラスが
反発し合う様に
分子同士が近づきすぎにくくなるんだね。


そう。
ところが、
等電点では話が少し変わるよ。
等電点とは、
分子全体の正味電荷が 0 になる pH のことだったね。
このとき、分子全体としては
プラスでもマイナスでもなくなるため、
分子どうしの電気的な反発が小さくなるんだよ。
反発が弱くなると、どうなるの?


反発が弱くなると、
分子どうしが近づきやすくなるんだ。
その結果、
・水に溶けにくくなる。
・分子どうしが集まりやすくなる。
・沈殿しやすくなる。
ことがあるよ。
つまり、等電点では「ばらばらでいにくくなる」んだ。
なるほど。
だから、集まって沈みやすくなることがあるんだね。


その通り。
これは、タンパク質を取り出したり、
分けたりするときの大事な考え方なんだ。
実験では、pH を等電点に近づけて
タンパク質を沈殿させる ことがあるよ。