7. 滴定曲線の前に知っておきたい: アミノ酸のイオン性

〜カルボキシ基・アミノ基・等電点の基本をやさしく整理
※本記事にはアフィリエイトリンクが含まれる可能性があります。
📚目次
(3)カルボキシ基とは? なぜH⁺をはなしてCOO⁻になるのか
(4)アミノ基とは? NH₂はなぜH⁺を受け取ってNH₃⁺になるのか
スマホを置き、誘惑を断つ。
時間を支配し、自分を最適化する。
その瞬間、あなたの脳は
「深い集中」へと研ぎ澄まされていく。
必要な通知は手首で一瞬、不必要なノイズはすべて遮断。
臨床で、ラボで、デスクで、カフェで。
Apple Watch SE
余計なものを削ぎ落とす。
その腕に、合格への最短ルートを。
1. 滴定曲線の前に知っておきたい アミノ酸のイオン性▲ 目次へ

プラス➕にもマイナス➖にも傾くことができるんだ。
条件しだいで電気のバランスが動くってこと?


だからアミノ酸の滴定曲線を見るときも、
「どっちに傾いているか」を見ると
流れがつかみやすいんだよ。

アミノ酸のイオン性について確認しておこうか。

滴定曲線をただ暗記する📚のではなく、
変化の流れとして読めるようになるよ。
2. イオンとは? 中学生のおさらい▲ 目次へ

思い出してみようか。
ちょっとあやふやかも…。


大丈夫。一緒に復習しよう。
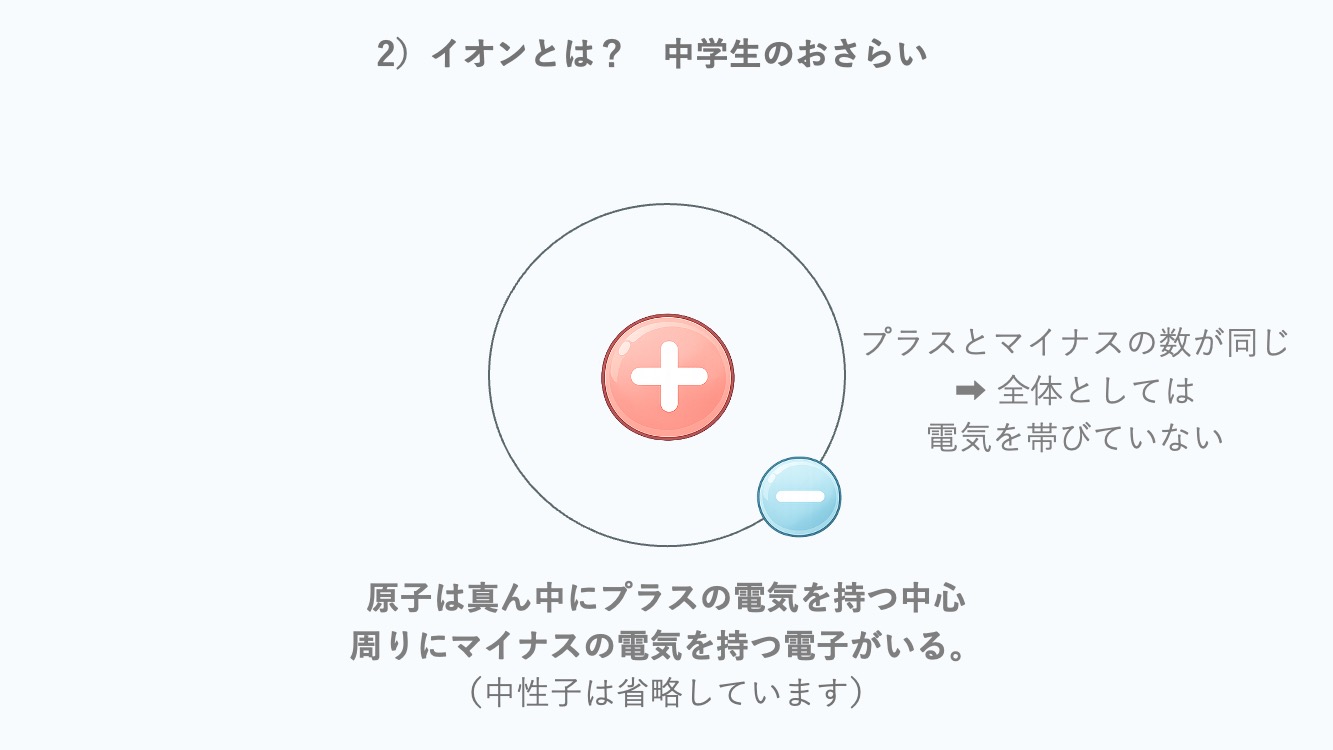
まず、原子は真ん中にプラスの電気を持った中心があって、
そのまわりにマイナスの電気を持つ電子がいるんだ。

全体としては電気を帯びていないんだよ。
ふつうは電気を帯びていないんだ。


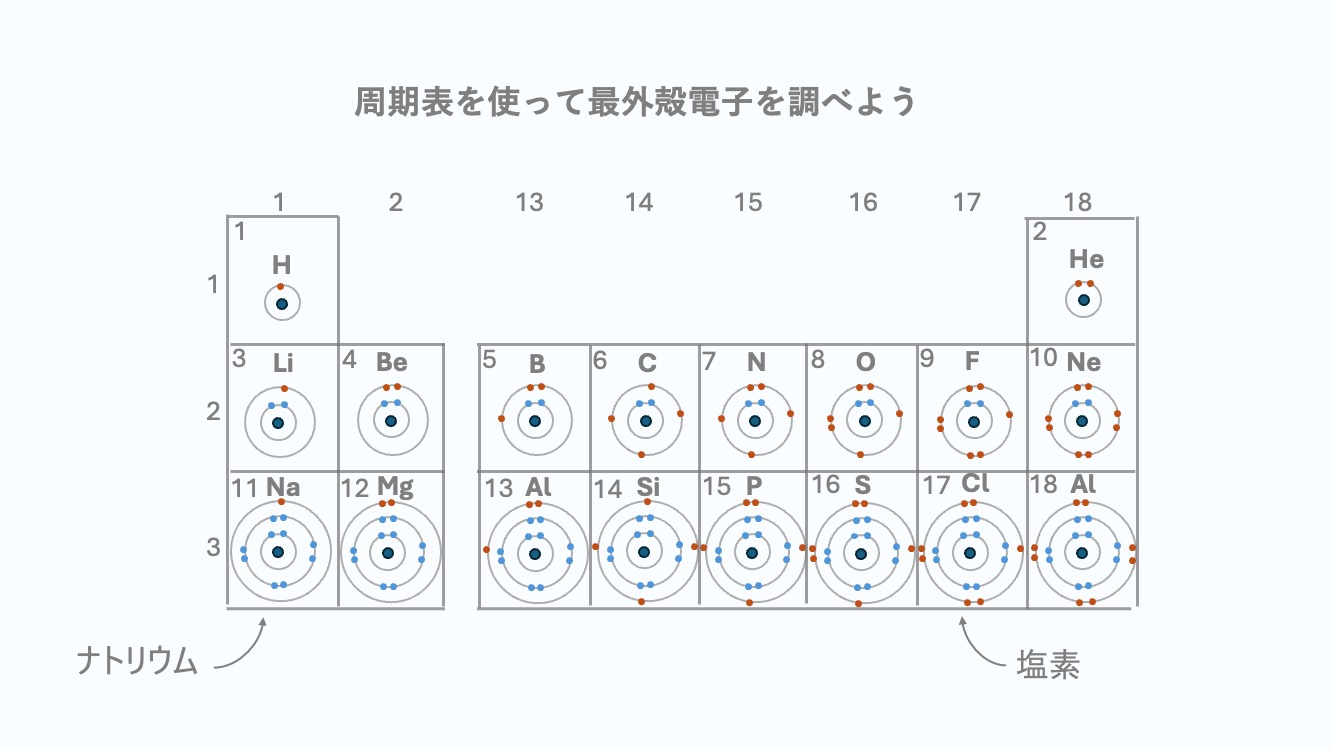
たとえばナトリウムを見てみよう。

そのまわりに11個の電子がいる。
だからふつうはつり合っているんだね。


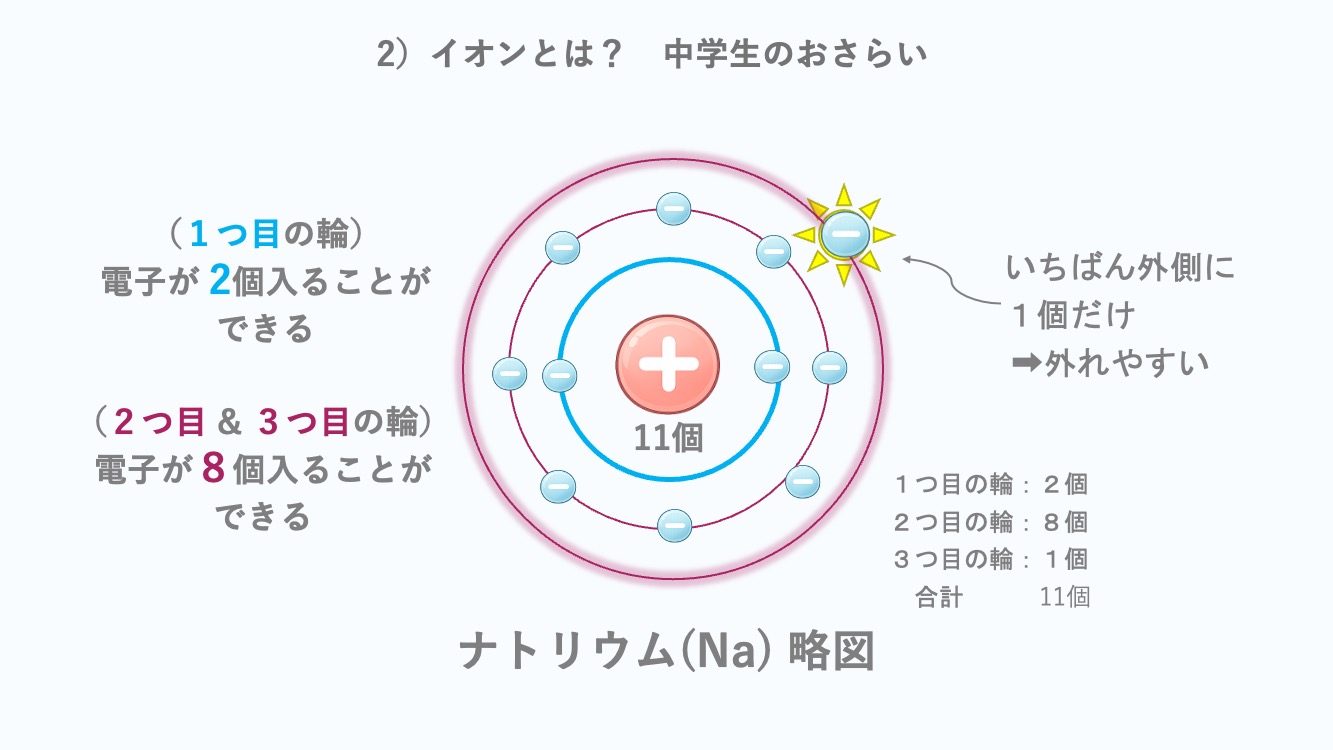
電子は、🪐惑星がまわるみたいに
外側へ広がって並んでいる。

2つ目の輪には8個入る。
3つ目の輪にも8個入ることができるんだ。


2つ目の輪に8個入るから、
最後の3つ目の輪にはたった1個だけ残るんだ。


いちばん外側でふらふらしていて😵💫、はずれやすい。

手放しやすいんだよ。

安定しやすいんだ。
塩素は1個ほしい。
なんだか相性ぴったり。



ナトリウムがその1個を差し出し、
塩素が受け取ることで、
両方が安定した状態になっているんだ。
落ち着いているんだ。

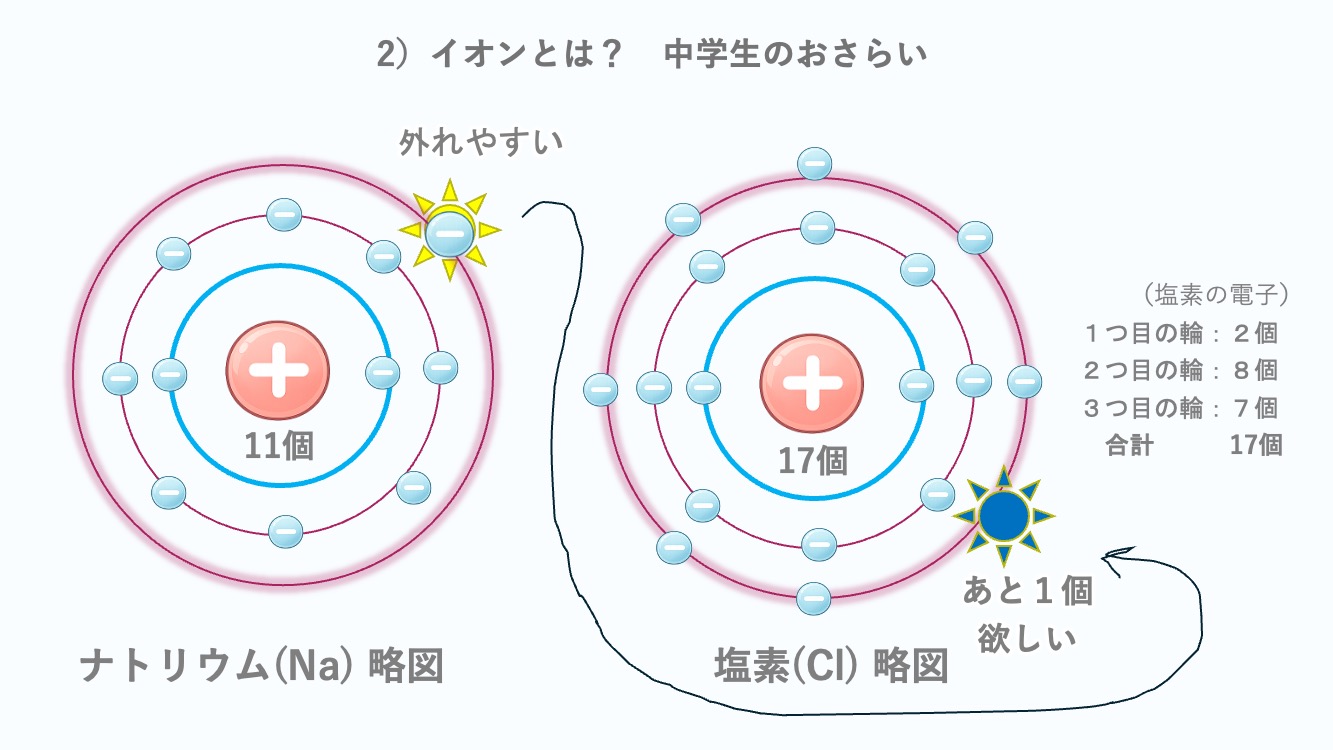




塩素は電子を1個多く持った状態で安定しているから
Cl⁻ になる。


イオンとは、このように、
原子が電子を失ったり 受け取ったりすることで、
⚡️電気を帯びた粒子になったもののことなんだ。
Na はプラスだから陽イオン、
Cl はマイナスだから陰イオンなんだね。



Na はプラスの電気を帯びた陽イオン、Cl はマイナスの電気を帯びた陰イオンになる、
ということだね。

3. カルボキシ基とは? なぜH⁺をはなしてCOO⁻になるのか▲ 目次へ

これは中学ではあまり習っていない気がする。


これについては中学ではあまり習わないので、
少し新しい見方✨になる。

基本的にCOOHは、水の中で
COOH ⇄ COO⁻ + H⁺
のように、H⁺をはなして COO⁻ になることがあるんだ。
少し似ているね。



イオンになった。でもCOOHでは、そういう❌単純な受け渡しではないんだ。
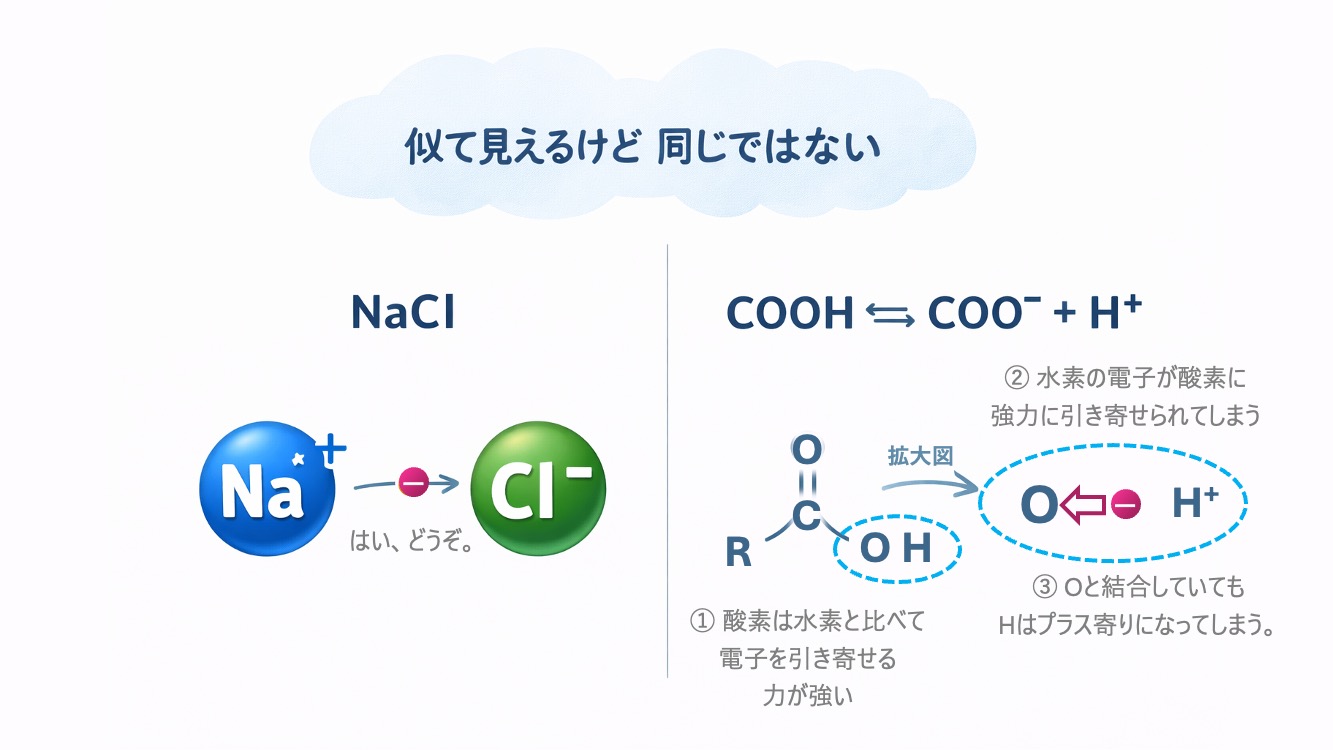

ここで大事なのが、O(酸素)とH(水素)の関係。
酸素は電子を引っぱる力が強く💪
水素はそれが弱い。

電子は酸素のほうへぐっと
引っぱられているんだ。
電子は酸素のほうに引っぱられているんだね。


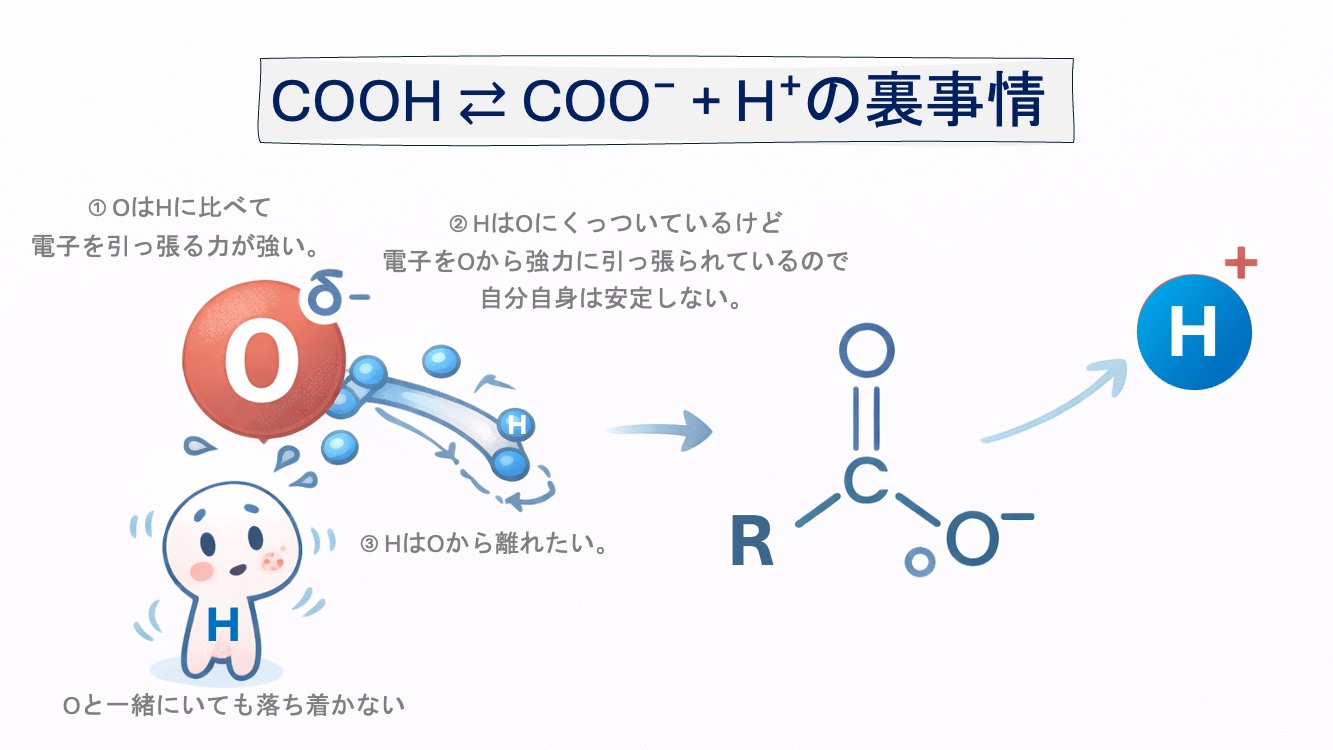
だからもし自分がCOOHの中のHだったら…

なんだか少し居心地が悪いな🌀」「このままずっとここにいるより、
出ていったほうが楽かもしれない😆」



このHがH⁺として離れやすい。

マイナスの電気を帯びる。

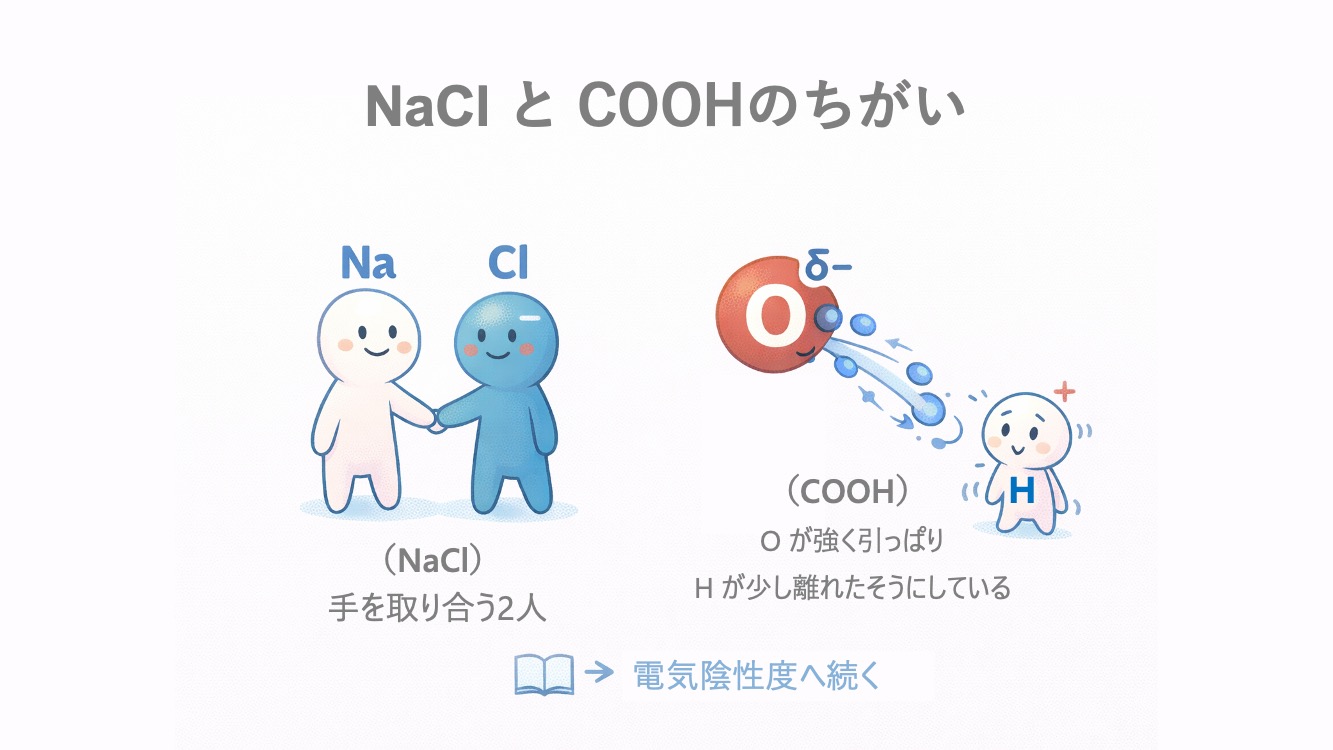
NaCl:おたがい助け合うカップル
COOH:片方が強くて💪、
Hが離れやすいカップル
みたいだね。
NaCl は助け合っている感じで🫶、
COOH は力の差💪がある感じ。


「酸素はなぜそんなに電子を強く引っぱるの?」
という話は、電気陰性度という考え方に
つながってくる。

別の動画でわかりやすく説明するね。
H⁺が多いと、なぜCOOHのままでいるの?

いつも同じだけ COOH と COO⁻ + H⁺ が
あるわけではないということなんだ。


まわりの水のようす💧で、COOHが多くなったり、
COO⁻ + H⁺が多くなったりするんだ。

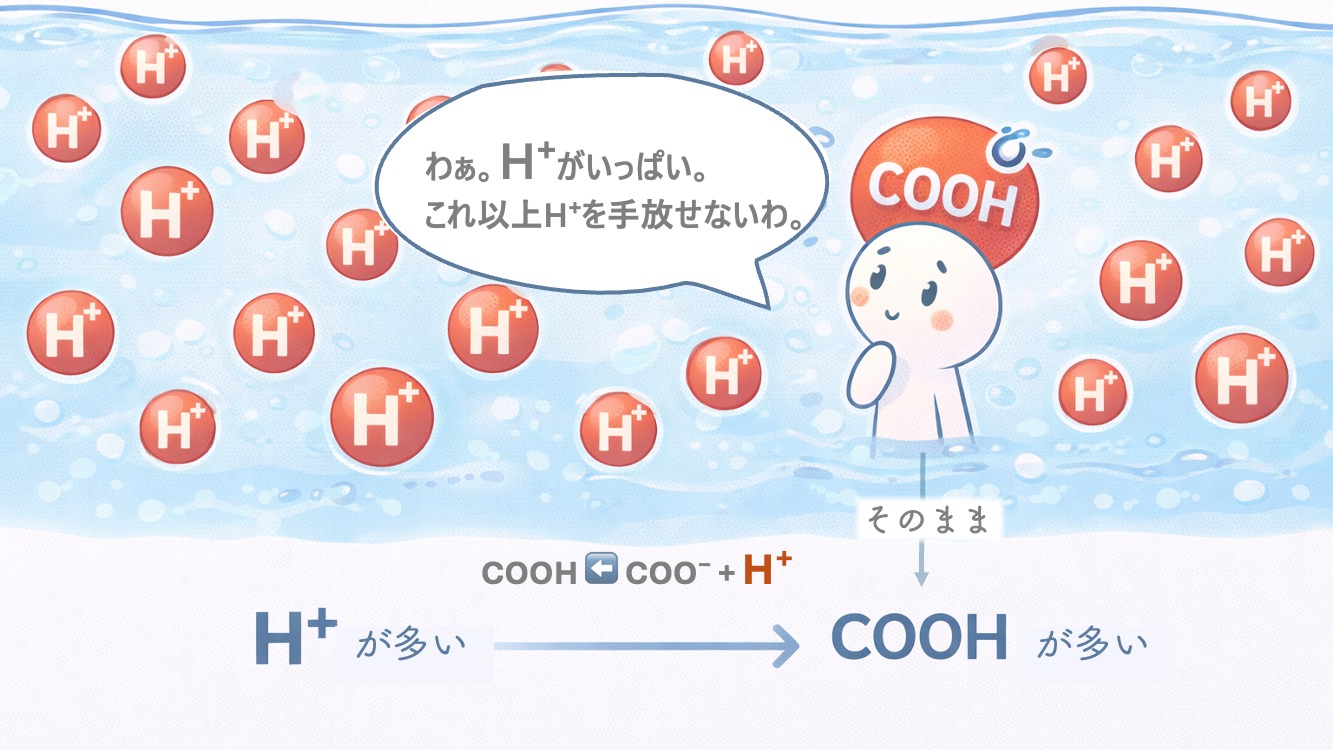
たとえば、まわりに H⁺ がたくさんある とする。
するとCOOHは、こう感じる。
「えっ、まわりはもうH⁺でいっぱいじゃないか!」
「今ここで、私までH⁺を外に出したら、
もう入り込むすき間がない」
「今はこのまま、COOHの形で静かにしておこうかな」

多くなる。
そのままでいるほうが多くなるんだね。


H⁺が少ないと、なぜCOO-が増えるの?

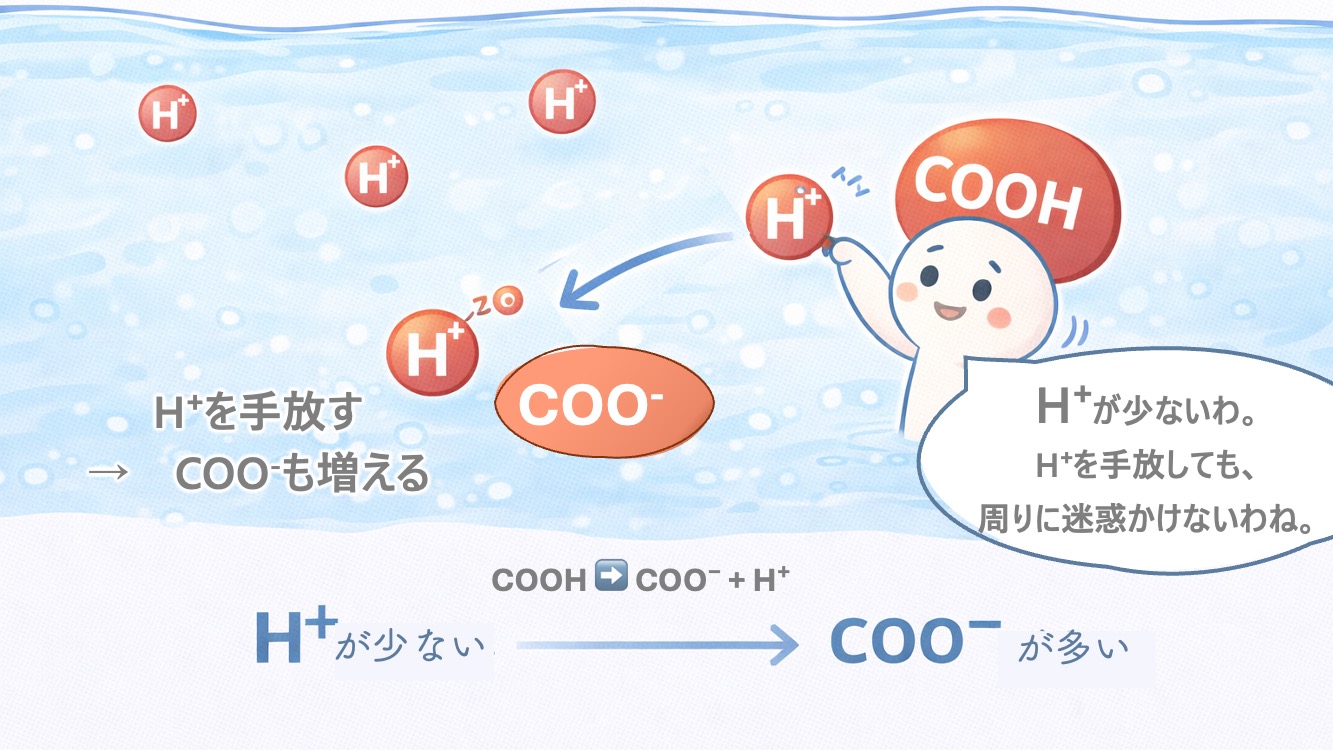
反対に、まわりに H⁺ が少ない とする。
そんなときCOOHは、こう感じる。
「あれ、まわりにはH⁺があまりいない」
「それなら、私が1つ出ても大丈夫そうだ」
「じゃあ、ここからH⁺をはなしてみようか」

すると、COOHは H+をはなして COO-になりやすい。
つまり、H⁺が少ない環境では、COO- のほうが
多くなりやすい。
COOH から H⁺ がはなれやすいんだね。


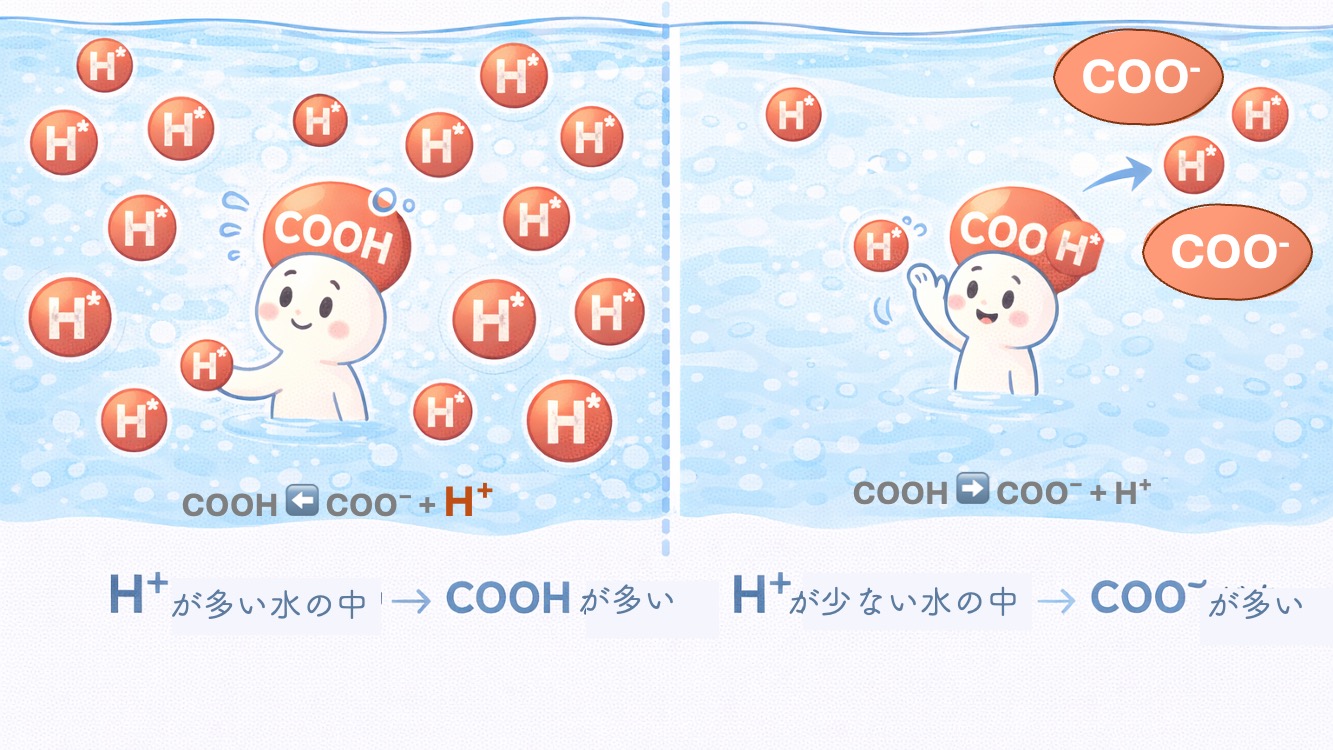
H⁺が多いと → COOH が多い
H⁺が少ないと → COO- が多い
どちらの形が多いかが変わるんだね。

4. アミノ基とは? NH₂はなぜH⁺を受け取ってNH₃⁺になるのか▲ 目次へ



そして、まわりに 8個 そろうと安定しやすい。




窒素は 1個の炭素 と 2個の水素 とつながっていて、
それぞれと電子を共有している (NH2-C-)。これで、窒素のまわりには8個の電子がそろって、
まず安定しているんだ。
(まずは下の図を見てみてね。)
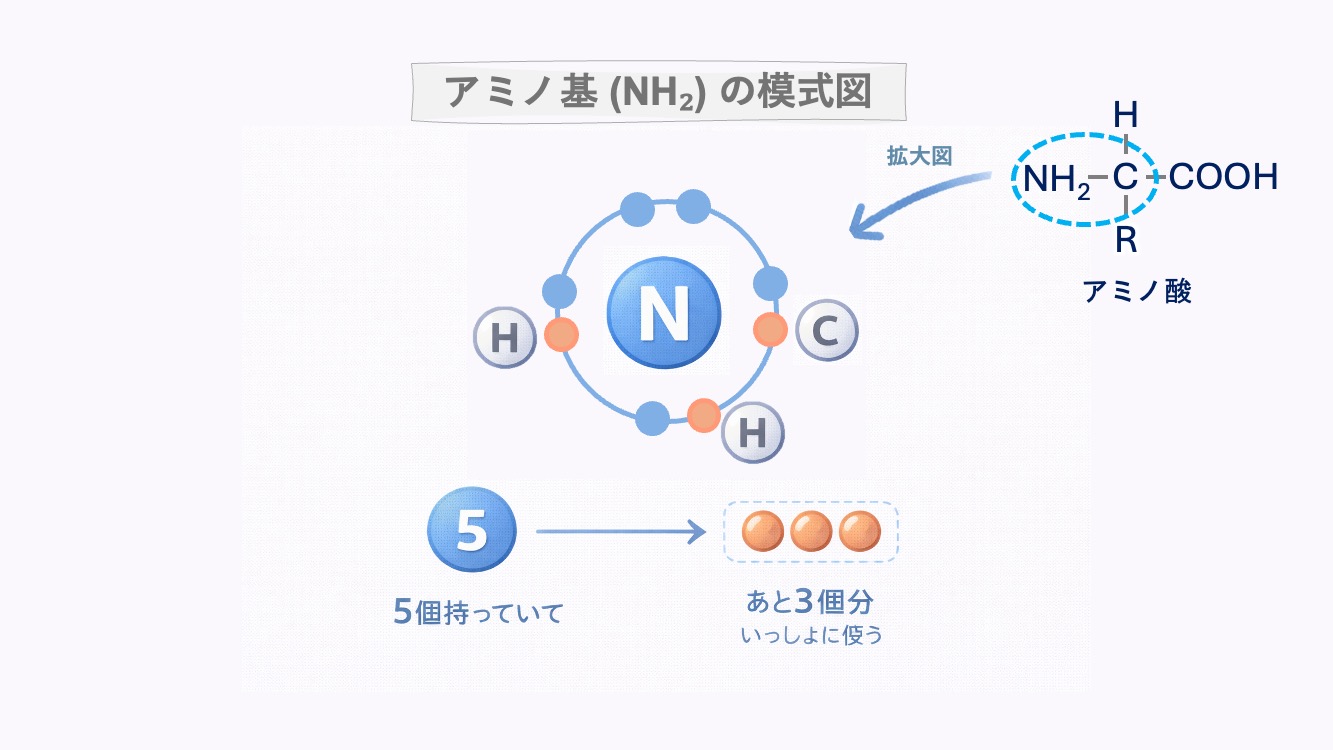

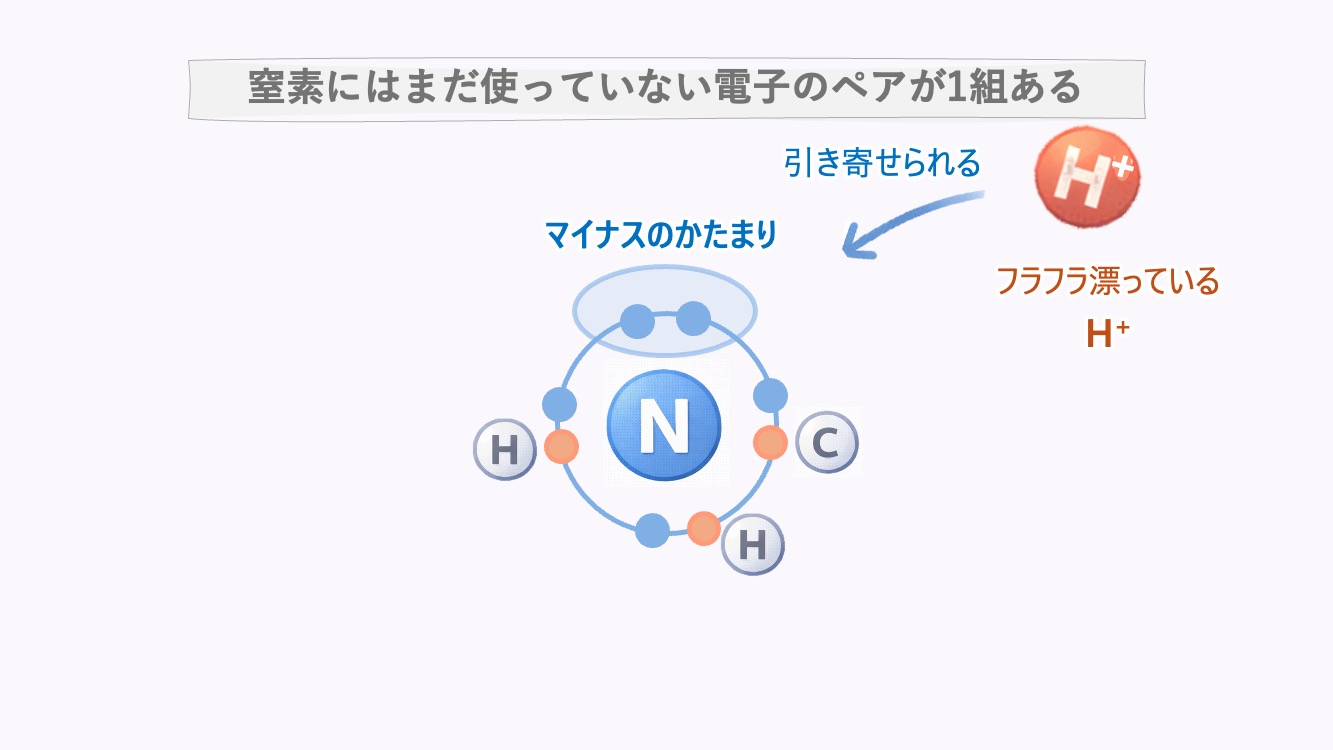
窒素にはまだ使っていない電子のペアが1組あること。電子ペアはたしかに、窒素の近くにあるだけでも
安定している。


どうかな?


H⁺ はプラスの電気だけを持っていて、電子を強く求めている。

つまりマイナスのかたまりがあるわけ。



「ただ窒素のそばにある」より、「H⁺と結合を作って落ち着く」
ほうが有利な場合があるんだよ。

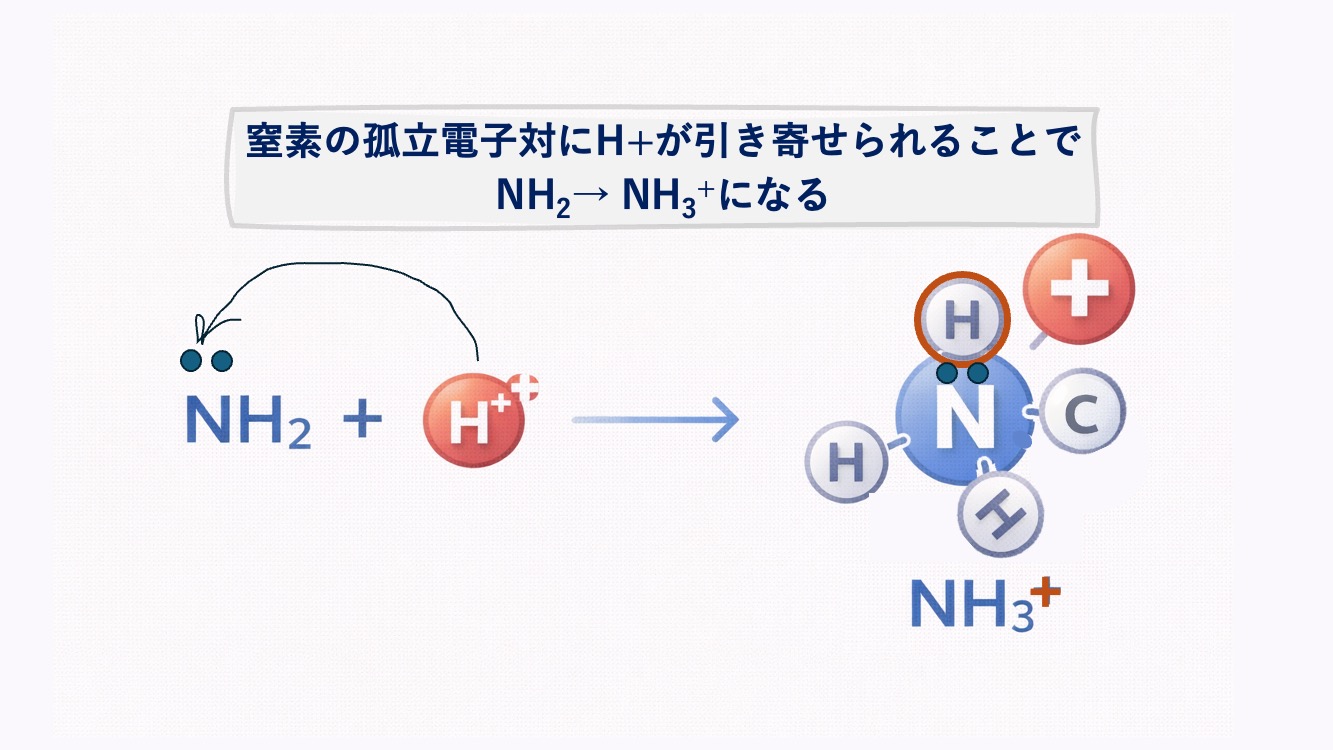
NH₂ + H⁺ ⇄ NH₃⁺
となる。

なれるんだね。


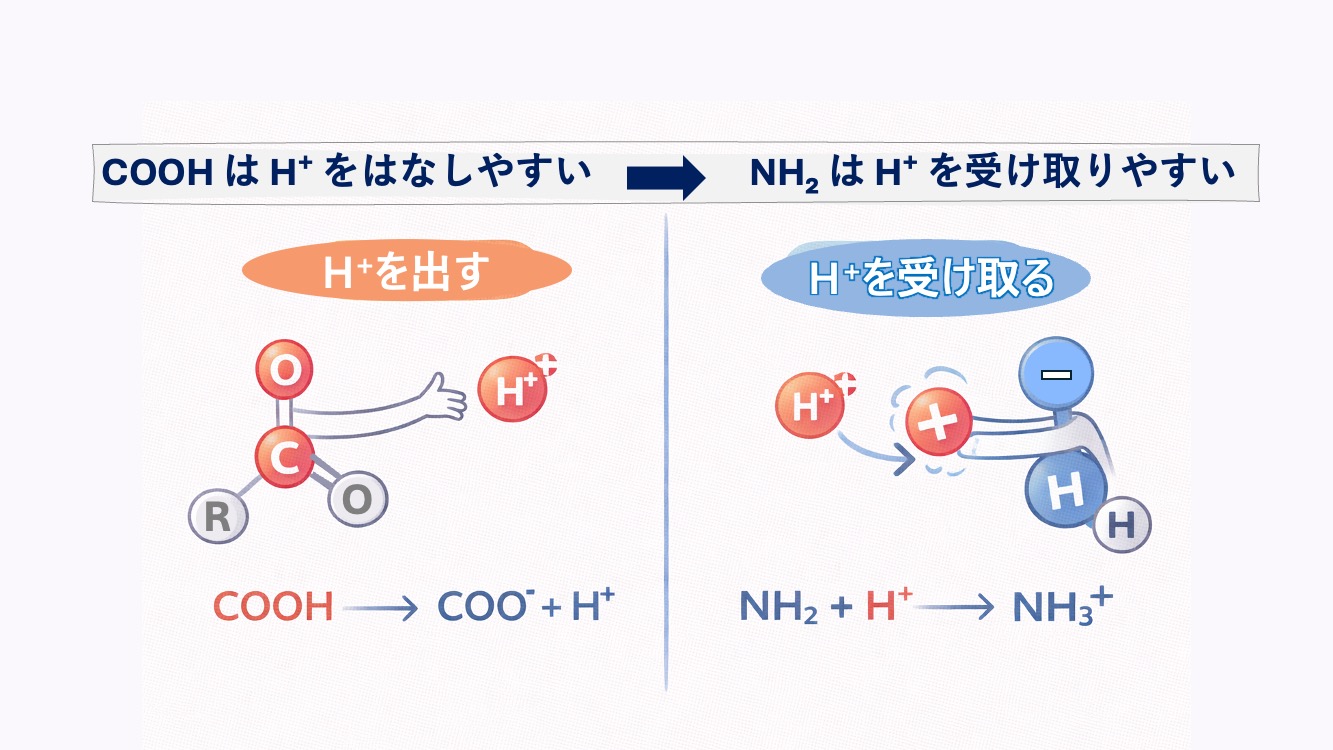
わかりやすい。COOH は H⁺ をはなしやすい
NH₂ は H⁺ を受け取りやすい
という違いがある。



すると NH₂ は H⁺ を受け取りやすくなって、
NH3+ が多くなる。


すると NH₃⁺ は H⁺ 受け取りにくくなって、
NH₂ が多くなる。

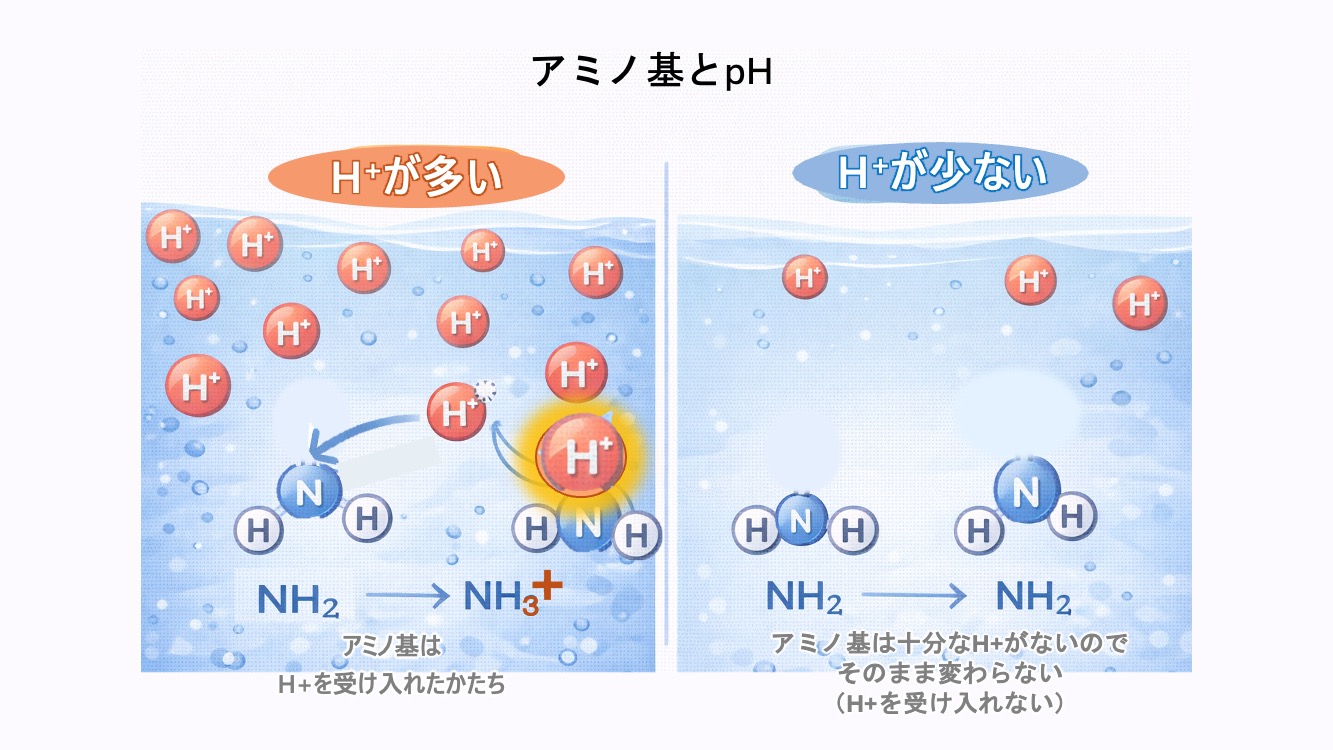

H⁺ が多いと → NH₃⁺ が多い
H⁺ が少ないと → NH₂ が多い
ということなんだ。
NH₃⁺ になったり NH₂ のままだったりするんだね。

5. 両性電解質・両性イオンとは? 定義の確認▲ 目次へ
(定義の確認:両性電解質・両性イオン)



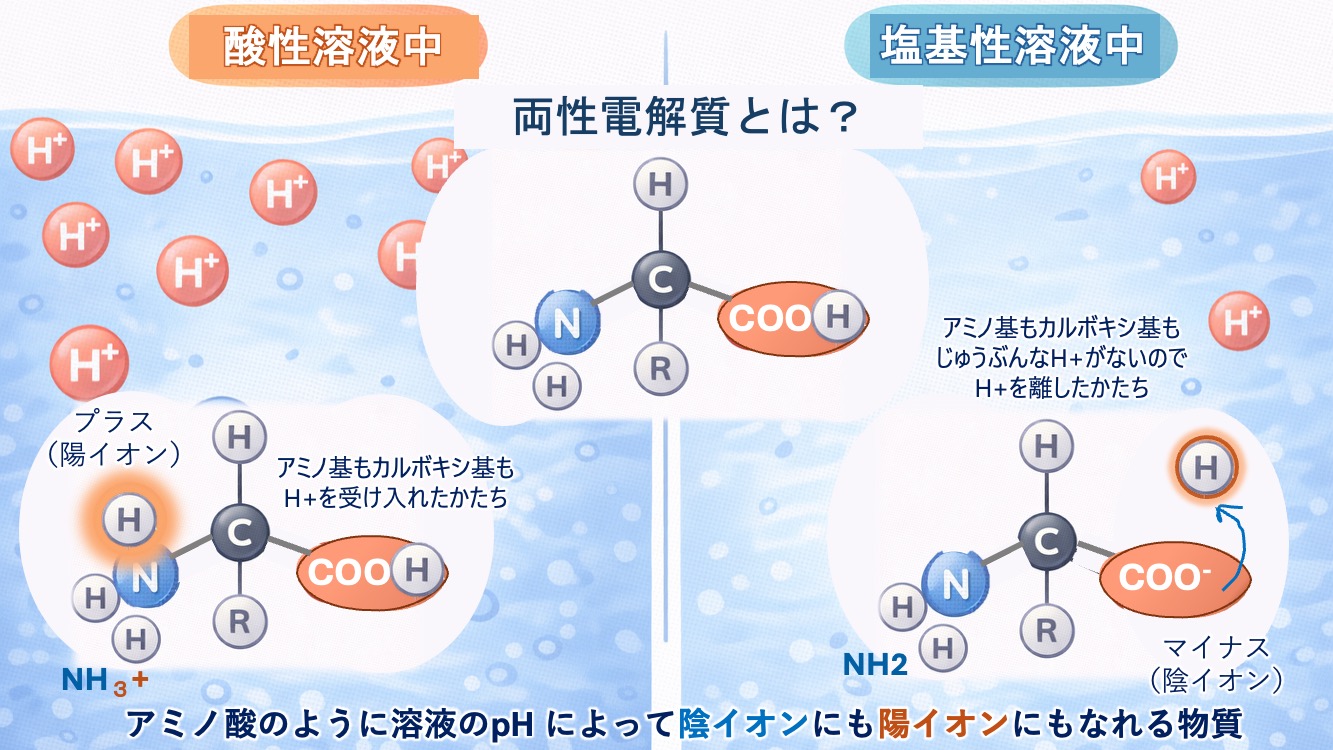
アミノ基もカルボキシ基も、
まわりにたくさんある H+ を受け入れた形になる。

H+ を離した形になっているんだ。
酸性溶液中では H+ を受け入れた形、
塩基性溶液中では H+ を離した形になるんだね。


溶液のpH によって陰イオンにも陽イオンにもなれる物質を、
両性電解質というよ。
同じ意味なの?



カルボキシ基は水素イオンを遊離して COOー になる。

アミノ基は NH3+陽イオン になるんだね。


両性イオン というよ。

この両性イオンになるんだね。
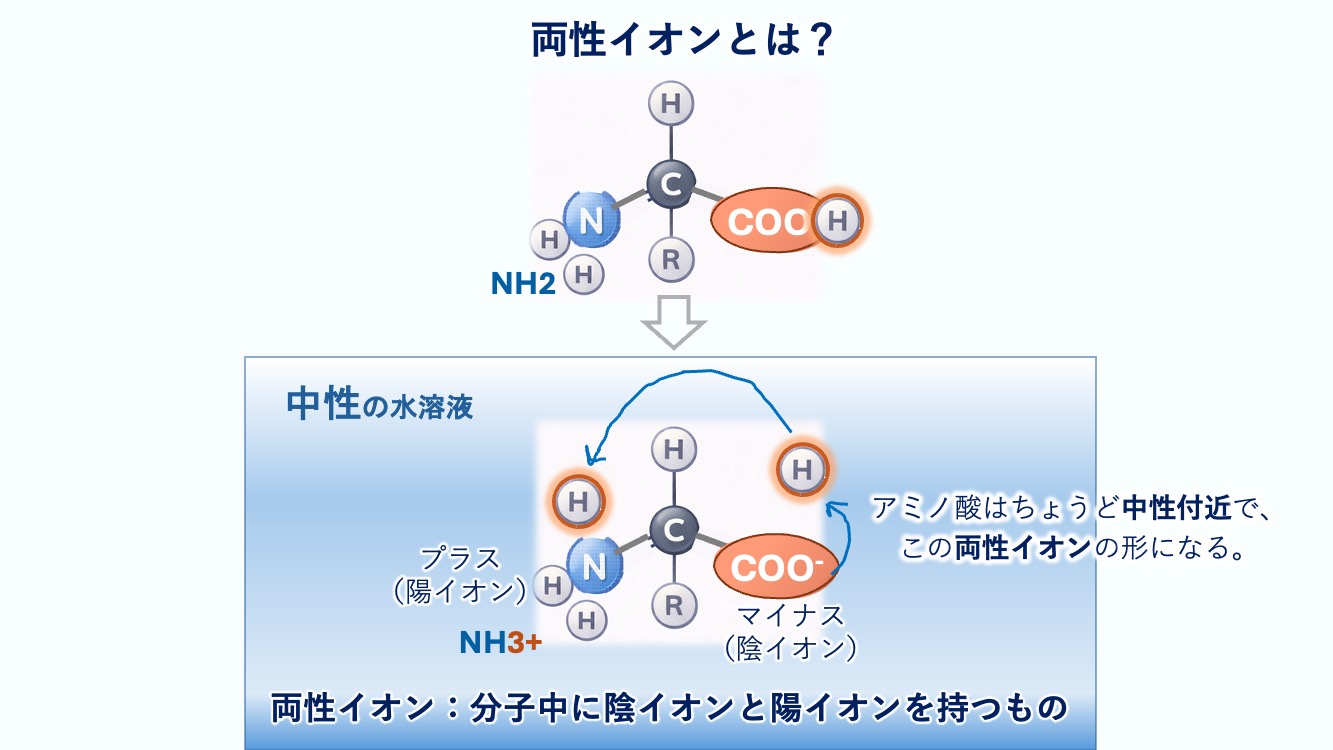

陰イオンにも陽イオンにもなれる物質のこと。

アミノ酸はちょうど中性付近で、
この両性イオンの形になるね。
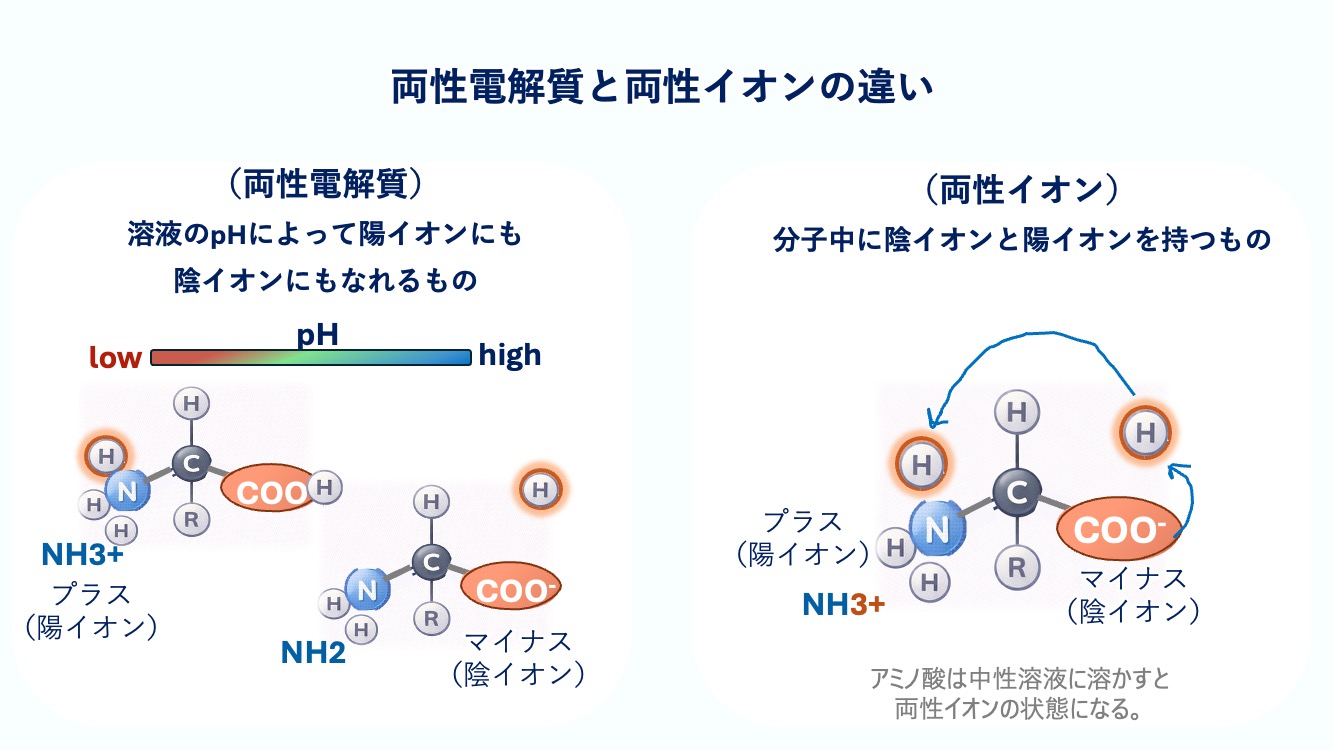
両性電解質は「pHによって変われる物質」
という意味で、両性イオンは「1つの分子の中にプラスとマイナスを
両方持っている形」という意味なんだね。

6. アミノ酸と等電点(pI)をわかりやすく解説▲ 目次へ

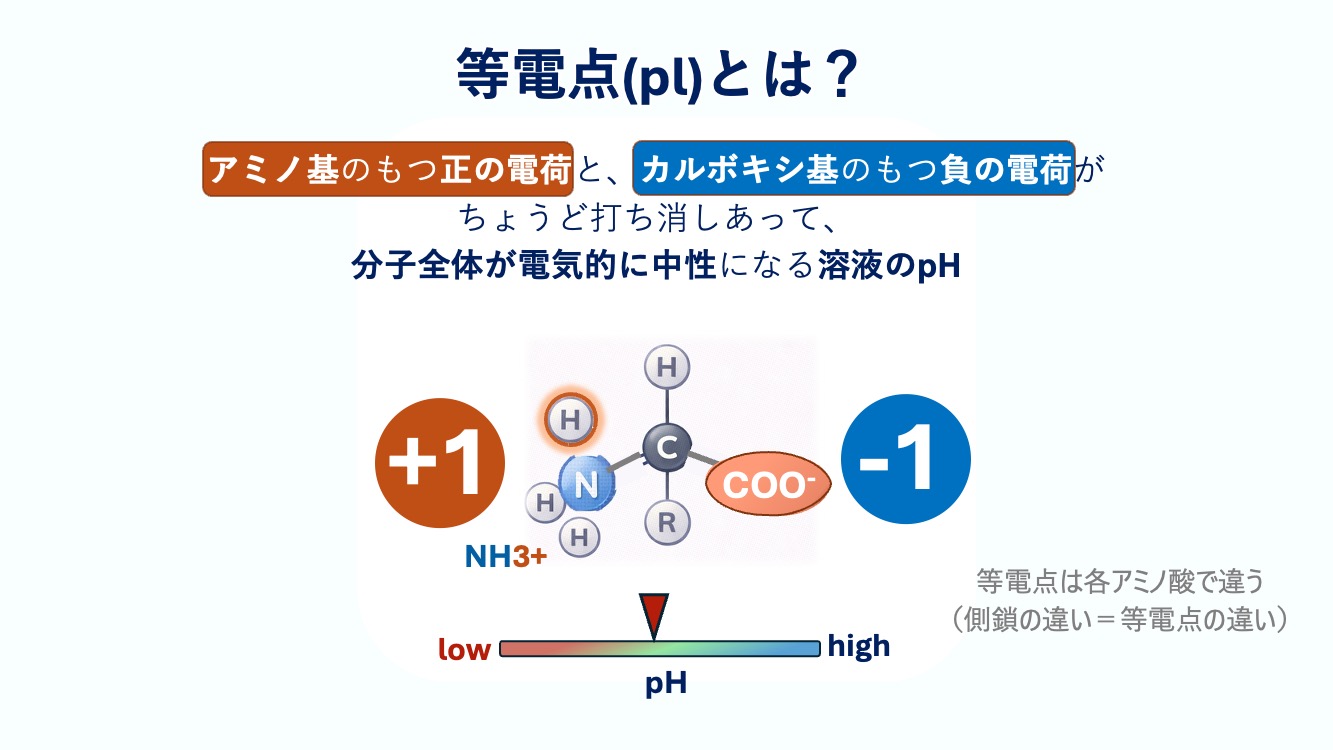
カルボキシ基のもつ負の電荷がちょうど打ち消しあって、
分子全体が電気的に中性になる溶液のpHを、
等電点(pI)というよ。
全体ではちょうど中性になる pH があるんだね。


すべてのアミノ酸は、側鎖の構造の違いによって、
それぞれ異なった等電点を持っているよ。
等電点もそれぞれ違うんだね。

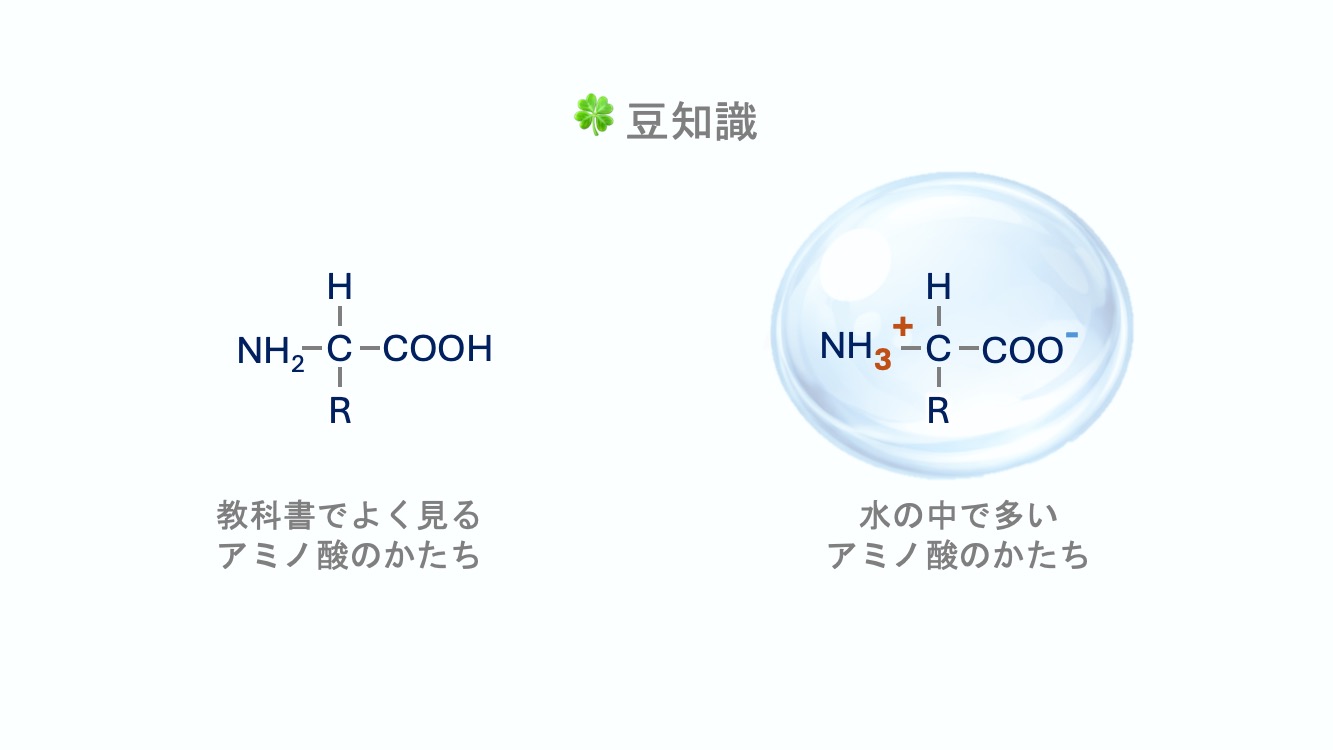
🍀ブログ特典:豆知識 教科書で見る形と、水の中でよくいる形は少し違う

NH₂–CHR–COOH
の形かな? 教科書でよく見る形。



いるわけではないんだ。


アミノ基は NH₃+カルボキシ基は COOー
になっていて、プラスとマイナスを同時に持つ形で
存在しているんだよ。
NH₂–CHR–COOH のままというより、
NH₃⁺ と COO⁻ を持った形のほうが多いんだ。


つまり、教科書で最初に見る
NH₂–CHR–COOH
は「基本の形」としては大事なんだけれど、水の中でいちばんよくいる姿とは少し違うんだ。
最初に覚える形と、水の中でよくいる形は、
少しズレがあるんだね。


このことを知っておくと、
「どうしてアミノ酸は電気を帯びるの?」「どうして等電点があるの?」が、ぐっと自然に見えてくるよ。
🐾 Dr.シロネコの応援メモ
使い終わった教科書📚はどうしていますか?
医学書・薬学書・看護書は価値が高いうちに整理するのが賢い方法です。
次のステップへ進むための軍資金にするのも手です。👍
【アウトプット重視】アミノ酸のイオン性・10題クイズ
▲ 目次へ
【復習】アミノ酸のイオン性・10題クイズ
参考文献/References
▲ 目次へ
① 世界的に有名な生化学の「三大教科書」
01
Lehninger Principles of Biochemistry
英語: Nelson DL, Cox MM. (2021). Lehninger Principles of Biochemistry, 8th Edition.
日本語: デービッド・ネルソン、マイケル・コックス(著)中山和久 他(監訳) (2023年). レ-ニンジャーの新生化学: 生化学と分子生物学の基本原理 (上)
今日のブログ記事に関する特徴: 原子構造や電子配置の基礎から説き起こし、なぜアミノ酸が水溶液中で「両性イオン」として存在するのかを熱力学的な安定性の観点から精密に記述しています。特に、結晶状態と水溶液中での構造の違いについて厳密に区別して解説している点が特徴です。
02
Biochemistry (Stryer)
英語: Berg JM, Tymoczko JL, Gatto Jr. GJ, Stryer L. (2019). Biochemistry, 9th Edition.
日本語: 入村達郎 他(監訳) (2021年). ストライヤー生化学 第10版.
今日のブログ記事に関する特徴:「アミノ酸は常にイオン化している」という前提を強調しており、生理的pH(約7.4)においてアミノ基とカルボキシ基がそれぞれどのような荷電状態にあるかを、タンパク質の機能と結びつけて簡潔に解説しています。
03
Harper’s Illustrated Biochemistry
英語: Victor WR, Anthony PW, Peter JK, David AB. (2022). Harper’s Illustrated Biochemistry, 32nd Edition.
日本語: 上代淑人(監訳) (2023年). イラストレイテッド ハーパー・生化学 原書32版
今日のブログ記事に関する特徴: アミノ酸を「多塩基酸」の一種として捉え、H+の濃度変化に応じて分子の正味電荷がプラスからマイナスへと段階的に変化していく様子を、医学的な酸塩基平衡の理解に繋がるよう構成しています。
② 初心者でも読みやすい・人気のテキスト 3選
01
Lippincott’s Illustrated Reviews: Biochemistry
英語: Abali EE, Cline SD, Franklin DS, Viselli SM. (2021). Lippincott Illustrated Reviews: Biochemistry, 8th Edition.
日本語: 石崎泰樹 他(監訳) (2022年). リッピンコット イラストレイテッド 生化学 原書8版.
今日のブログ記事に関する特徴: 「アミノ酸の化学的性質」の章で、カルボキシ基とアミノ基の電離状態を色分けされた図で示しています。特に等電点において、なぜ「正味電荷が0」と言えるのかを、1分子内のプラスとマイナスの相殺として視覚的に説明しています。
02
はじめの一歩の生化学・分子生物学
石浦章一(著) (2013年). はじめの一歩の生化学・分子生物学 第3版.
今日のブログ記事に関する特徴: 化学が苦手な学生が躓きやすい「イオン結合」と「共有結合」の違いや、H+が動く物理的なイメージを、身近な比喩を使って丁寧に解説しており、今回のブログの「カップルの比喩」に近い感覚で読み進めることができます。
03
マンガでわかる生化学
武蔵野公嗣(著) (2005年).
今日のブログ記事に関する特徴: 目に見えない電子のやり取りや、H+が窒素原子の電子ペアに吸い寄せられる現象を、擬人化されたキャラクターの動きとして描いています。等電点の概念を「電気的なバランスが取れて動けなくなる状態」として直感的に理解させてくれます。






