17.【生化学】アミノ酸の立体構造を「混成軌道」で解く:sp3・sp2・1.5重結合が作る生命の設計図

アミノ酸は「電子」で動く:
sp3と1.5重結合が解き明かす、生命の美しき設計ルール
※本記事にはアフィリエイトリンクが含まれる可能性があります。
丸暗記を卒業し、薬理や代謝を「論理」で支配する。
その本質である電子の動きを掴むことが、
あなたを市場価値の高い専門家へと押し上げます。
「不斉炭素だから立体構造をとる」
―その説明だけで、本当に納得できていますか?
医学部・薬学部の試験やCBT、さらに過酷な院試。
そこでは「アミノ酸の構造」という基本中の基本が、
形を変えて何度も襲いかかってきます。
「とりあえず暗記して乗り切る」ことはできるかもしれません。
でも、それではペプチド結合の回転制限も、αヘリックスの安定性も、
結局はバラバラの知識のままで終わってしまいます。
▼ なぜ? を放置していませんか?
この問いに、電子の動き(混成軌道)から答えを出せるようになれば、
生化学の景色は一変します。
sp3、sp2、そして1.5重結合。
ただの暗記から抜け出し、タンパク質の高次構造を
「物理的な必然」として読み解くための最強の武器。
手に入れてみませんか?
国試や院試で問われる本質を、
どこよりも深く、どこよりも「腑に落ちる」形で整理しましょう。
📚 目次:アミノ酸の「構造」を混成軌道で完全攻略
1. 【立体構造の土台】sp3混成軌道がアミノ酸に「3Dの個性」を与える理由
▲ 目次へ
実はもっと立体的なものなのかな…?


その鍵を握る「sp3混成軌道」について解説していくよ。
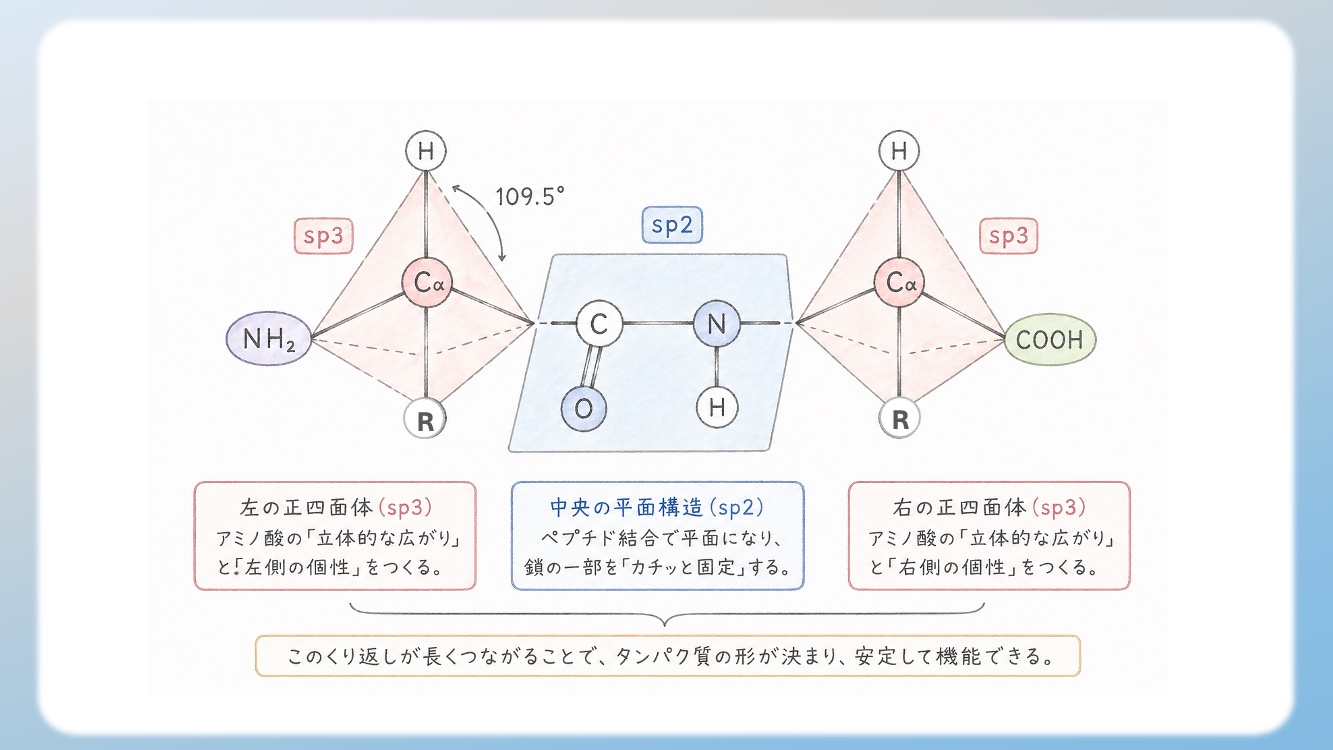
アミノ酸の真ん中にある炭素(α炭素)は、
「sp3混成軌道」で作られています。
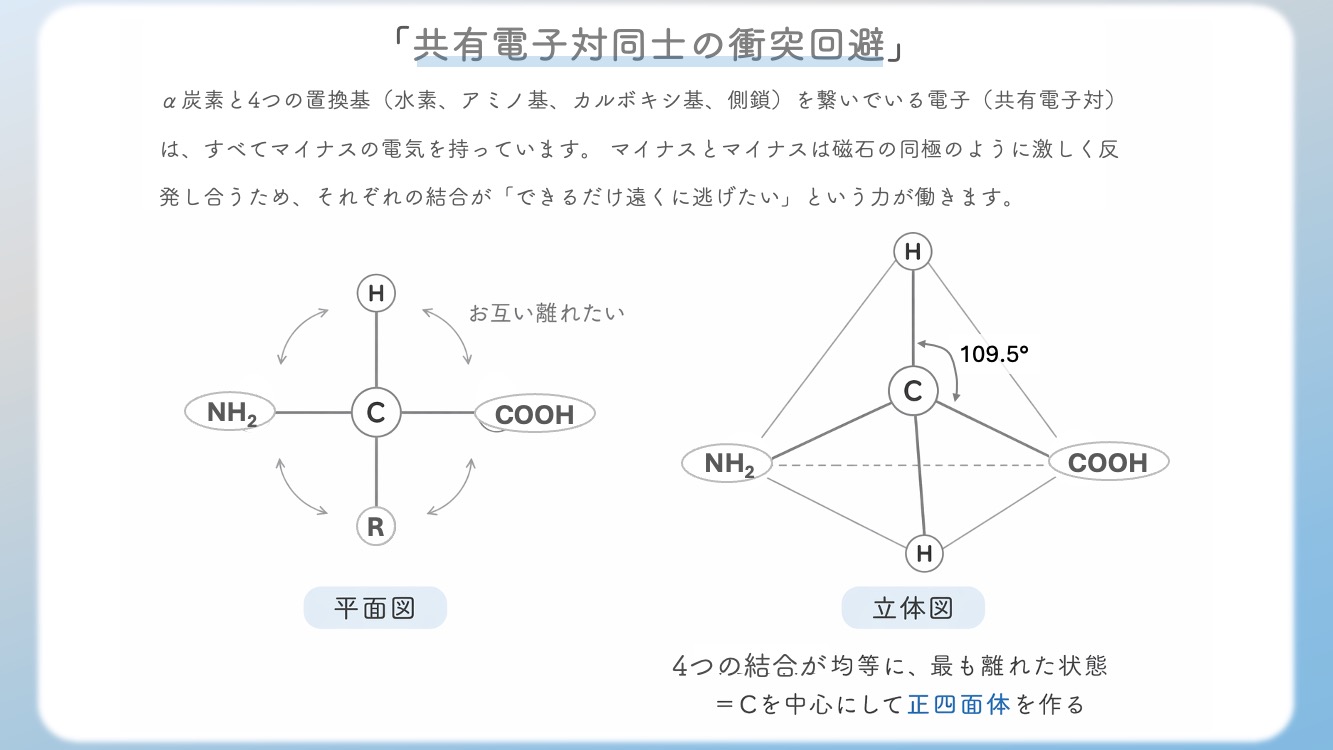
正四面体の中心から4つの角に向かって伸びる形(結合角 約109.5度)をしています。
これにより、アミノ酸は平面ではなく、しっかりとした3D構造を持ち、光学異性体(L型とD型)の違いを生み出します。
💡 機能への影響:
私たちの体のタンパク質は、ほぼすべて「L型」です。sp3による3D構造があるからこそ、精密な「鍵と鍵穴」の関係が成立し、生命活動が維持できるのです。

2. 【強固なジョイント】sp2混成軌道がタンパク質の「カタチ」を決定づける
▲ 目次へ


アミノ酸がつながった「ペプチド結合」は、
実質的に「sp2混成軌道」として振る舞います。
💡 酸素(O)の sp² 混成と電子配置
ペプチド結合の炭素(C)がsp²混成になることはすでに勉強しましたね。
実は酸素(O)も同じようにsp²混成軌道を作ることで、二重結合という「ガチッと固まった構造」を作ります。
酸素(O)原子番号8 の変化
【基底状態】
2p軌道: [↑↓] [↑ ] [↑ ] (ペア1、不対電子2)
2s軌道: [↑↓]
【励起状態】 ※2sの電子が2pへ移動
2p軌道: [↑↓] [↑↓] [↑ ] (ペア2、不対電子1)
2s軌道: [↑ ]
【sp² 混成状態】s-1個+p-2個→sp²-3個
2p軌道(残): [↑ ] ← π結合用
sp²軌道(混成): [↑↓] [↑↓] [↑ ]
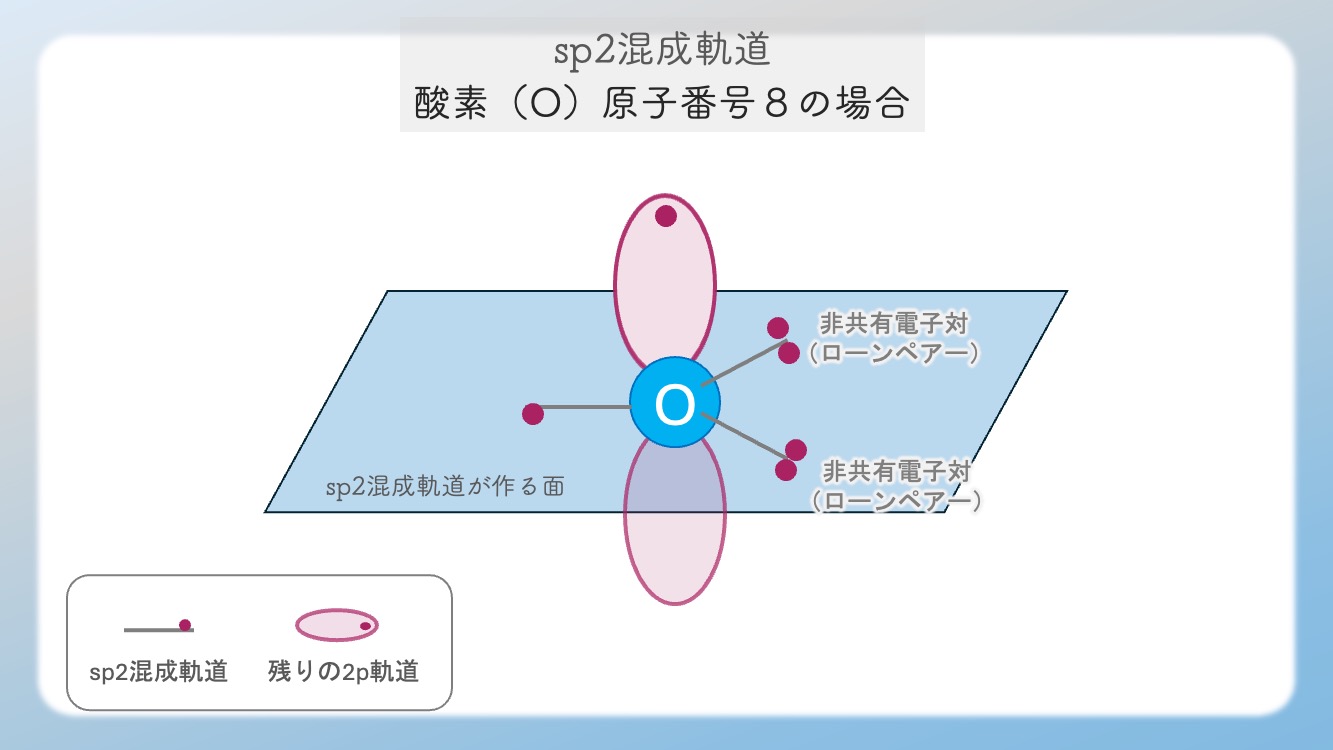
酸素の「腕」と「部屋」の使い道:
-
-
- 🔹 sp²軌道(1番目): [↑↓] ローンペアー(非共有電子対)
- 🔹 sp²軌道(2番目): [↑↓] ローンペアー(非共有電子対)
- 🔹 sp²軌道(3番目): [↑ ] σ(シグマ)結合用(炭素と正面で握手)
- 🔹 残った p軌道: [↑ ] π(パイ)結合用(炭素と横から握手!)
-
画像の通り、酸素には「すでにペアになっている電子」が2組あるため、結合の腕として使えるのは炭素と同じく「正面(σ)」と「横(π)」の2本だけになるのです。
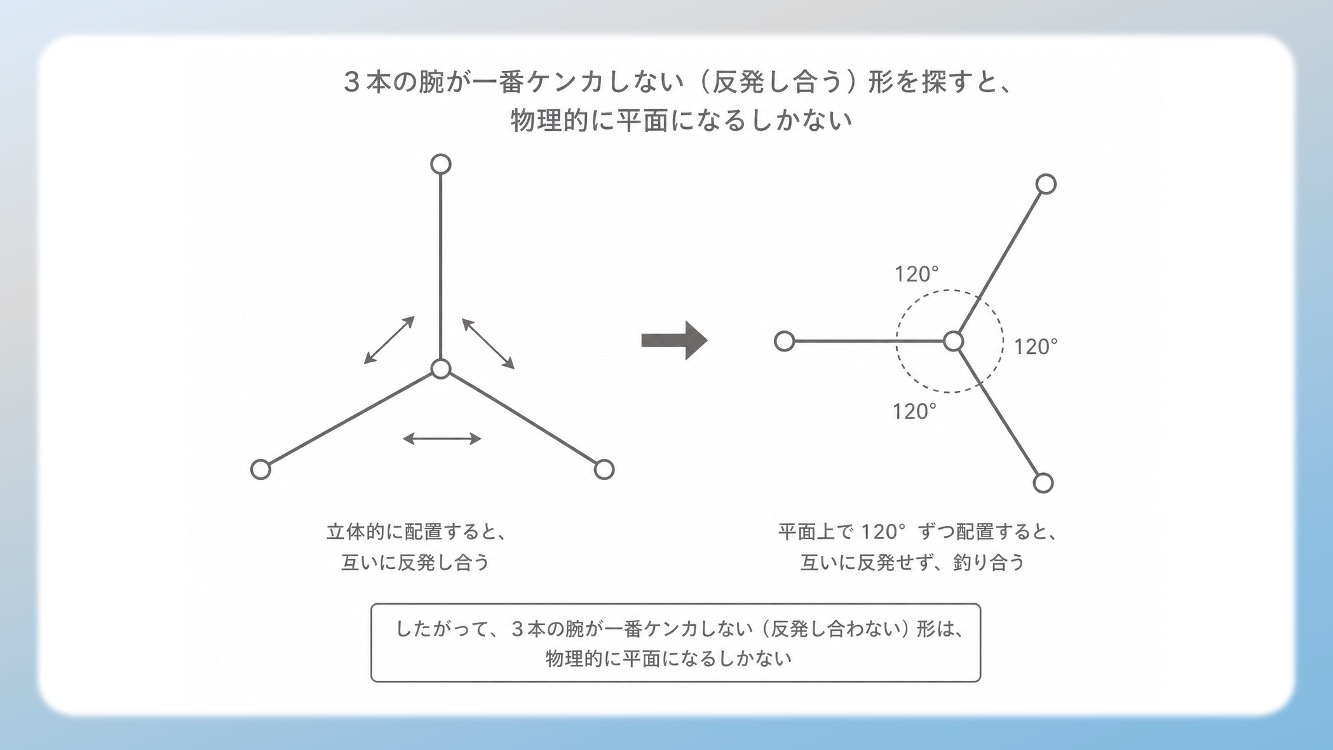
sp2混成による平面構造(結合角 120度)を作るため、結合の周りは「板のように硬く、回転できない」状態になります。
💡 機能への影響:
もし鎖が自由に動けたら、タンパク質は形を維持できません。sp2混成が生む「動かない板」が節々にあるおかげで、筋肉や酵素などの複雑で強固な立体構造を保てるのです。

3. 【生命の設計ルール】2つの軌道が「暗記量」を最小化する
▲ 目次へ
sp3/sp2混成軌道は、アミノ酸の構造構築に大きく寄与し、
その性質まで大きな影響を与えているのですね。
最後にもう一度整理しましょう。
アミノ酸がタンパク質として働くとき、
この 2つの軌道 は以下のような役割分担をしています。
| 軌道 | 構造の特徴 | 役割 |
|---|---|---|
| sp³ | 正四面体(3D) | アミノ酸に立体的な広がりと「右・左」の個性を与える |
| sp² | 平面(2D) | 鎖の一部をカチッと固めて、タンパク質の形を安定させる |
※表がはみ出す場合は横にスクロールして確認できます。
🐾 Dr.シロネコの応援メモ
使い終わった教科書📚はどうしていますか?医学書は価値が高いうちに整理するのが賢い方法です。次のステップへ進むための軍資金にするのも手ですよ。👍
ここからはさらに深く掘り下げていきます。
それ、当たり前だとおもっていませんか?
4. 不斉炭素のその先へ。sp3 という「物理的構造」が鏡像を生み出す真実
▲ 目次へ
ではさらに深く、その本質を理解しましょう。
なぜアミノ酸はL体・D体などの光学異性体を持つのでしょうか?
αアミノ酸が不斉炭素だから、それは当然のこと?
まさに!「α 炭素が不斉炭素であること」が光学異性体を生む直接の理由です。
ただ、化学の視点で見ると、「なぜ不斉炭素というものが成立するのか?」という根本的な理由が、実は sp3 混成軌道にあるんです。
1. 「sp3 混成軌道」が「不斉炭素」を可能にする
もし炭素の結合が「平面(sp2 や sp 混成軌道)」だったら、不斉炭素は存在できません。
- 📍 平面の世界: 仮に炭素に 4 つの異なるグループがついていても、それらがすべて同じ平面上に並んでしまったら、ひっくり返せば重なってしまいます。これでは「右と左」の区別がつきません。
- 📍 立体の世界(sp3): sp3 混成軌道によって、炭素は 正四面体(立体) の形をとります。この「立体的な広がり」があるからこそ、4 つの異なる手が伸びたときに、どうしても鏡合わせにしないと一致しない「右と左(不斉)」という関係が生まれるのです。
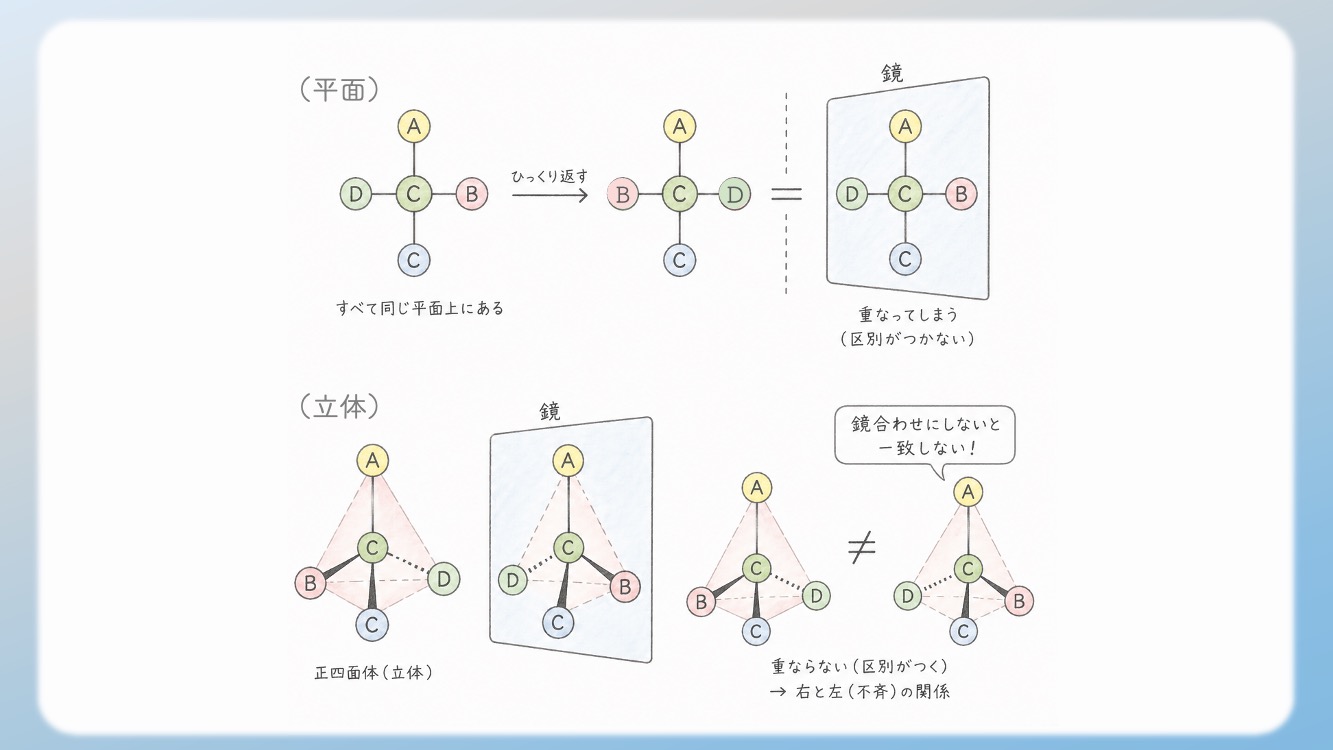
「不斉炭素だから光学異性体ができる」というのは現象としての正解ですが、その現象が起きるための物理的な舞台(形)を用意しているのが sp3 混成軌道 なのです。
2. 立体構造が「機能」にどう寄与するか?
では、この sp3 による立体(不斉炭素)が、具体的にどう機能に結びつくのでしょうか?
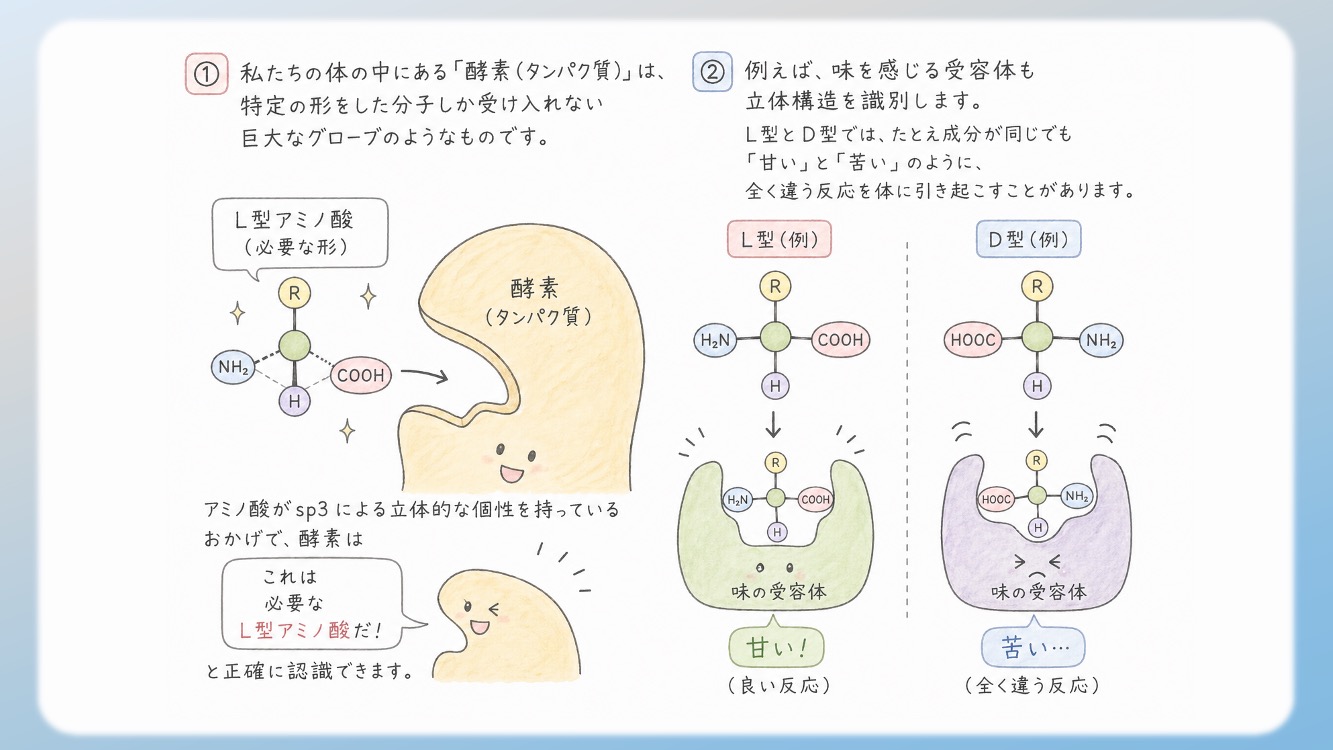
私たちの体の中にある「酵素(タンパク質)」は、特定の形をした分子しか受け入れない巨大なグローブのようなものです。アミノ酸が sp3 による立体的な個性を持っているおかげで、酵素は「これは必要なL型アミノ酸だ!」と正確に認識できます。
例えば、味を感じる受容体も立体構造を識別します。L型とD型では、たとえ成分が同じでも「甘い」と「苦い」のように全く違う反応を体に引き起こすことがあります。
5. 創薬・薬理学の基礎:sp2 混成軌道による「平面固定」が生体機能に及ぼす影響
▲ 目次へ
さて次はsp2について。
「ガチガチに平面を作って動かない。」
こう聞くとマイナスのイメージをもつ人も多いと思います。
しかしこれこそが、タンパク質を構築する上で非常に欠かせない構造であり、
創薬や薬理学に深く関係するのです。
「なぜアミノ酸の結合が平面であることが、創薬や薬理学に関係するのか?」
それは、薬が効く仕組みの根本が「鍵と鍵穴」の関係にあるからです。
💡 なぜ「平面固定」が薬理学の基礎なのか?
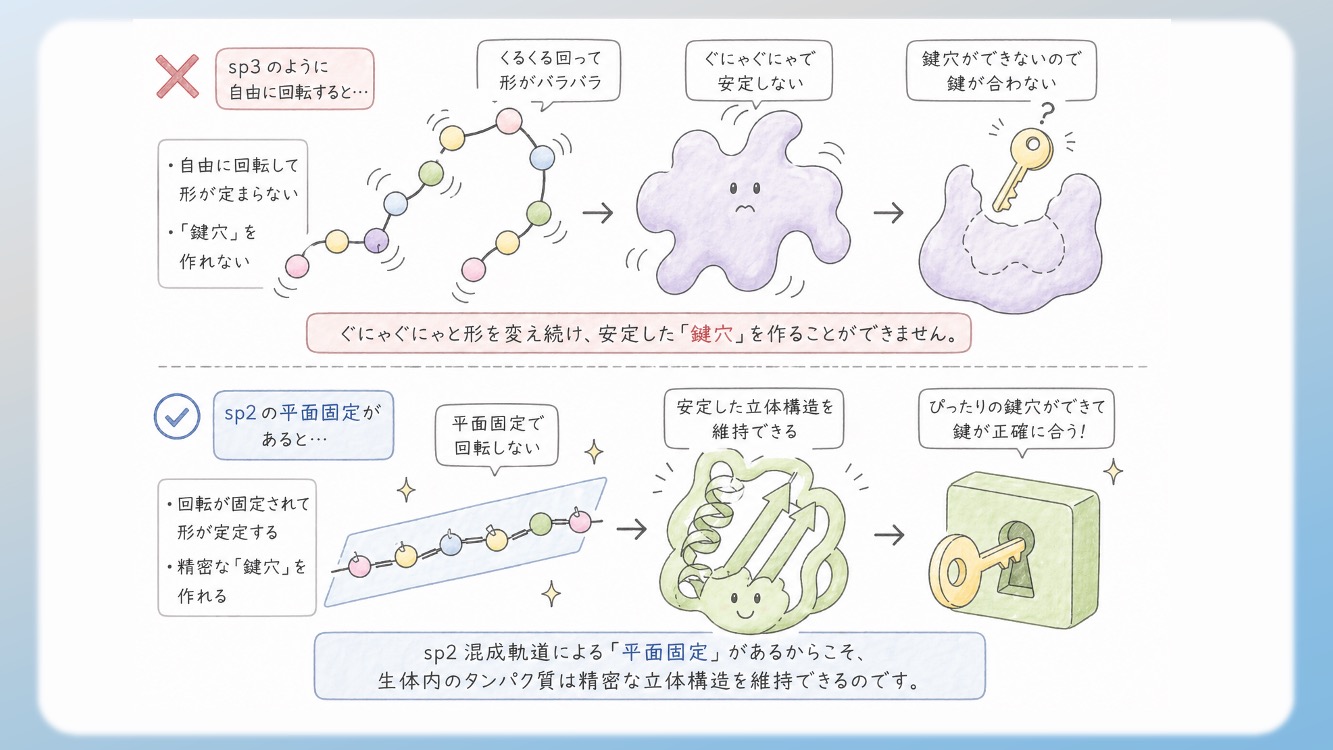
もしペプチド結合が sp3 のように自由に回転してしまったら、タンパク質はぐにゃぐにゃと形を変え続け、安定した「鍵穴」を作ることができません。
sp2 混成軌道による「平面固定」があるからこそ、生体内のタンパク質は精密な立体構造を維持できるのです。
✅ 「折れ曲がる場所」の限定:
sp3 の部分は自由に回転できる「関節」のような役割をしますが、sp2 の平面部分は「動かない板」のようになります。
✅ 機能的な折りたたみ:
どこでも自由に動けるクネクネの紐ではなく、要所要所が sp2 で固定されているからこそ、タンパク質は「いつも同じ形」に折りたたまれ、特定の仕事(酸素を運ぶ、消化するなど)ができるようになります。
✅ 創薬への応用:
多くの医薬品は、この sp2 によって固定された「特定の隙間(ポケット)」にスポッとはまるように設計されています。この構造の頑丈さこそが、薬が特定のタンパク質だけを狙い撃ちできる理由なのです。


6. 【最速マスター】アミノ酸の立体と機能——混成軌道で紐解く本質まとめ
▲ 目次へ
「3Dの舞台」を作る
炭素を正四面体に配置し、「不斉炭素」という舞台を作ります。これにより、生命に不可欠な「L型」の選択性が生まれます。
「形を固定する」
ペプチド結合を平面に固定し、「タンパク質の形」を安定させます。これにより、タンパク質が精密なマシーンとして動けるようになります。
「不斉炭素」という言葉の裏側にある
「電子の形のルール(混成軌道)」まで見えてくると、
生命現象がより物理的に、美しく見えてきませんか?


第二部:連結の魔法
—— 「回らない結合」が生命を作る ——
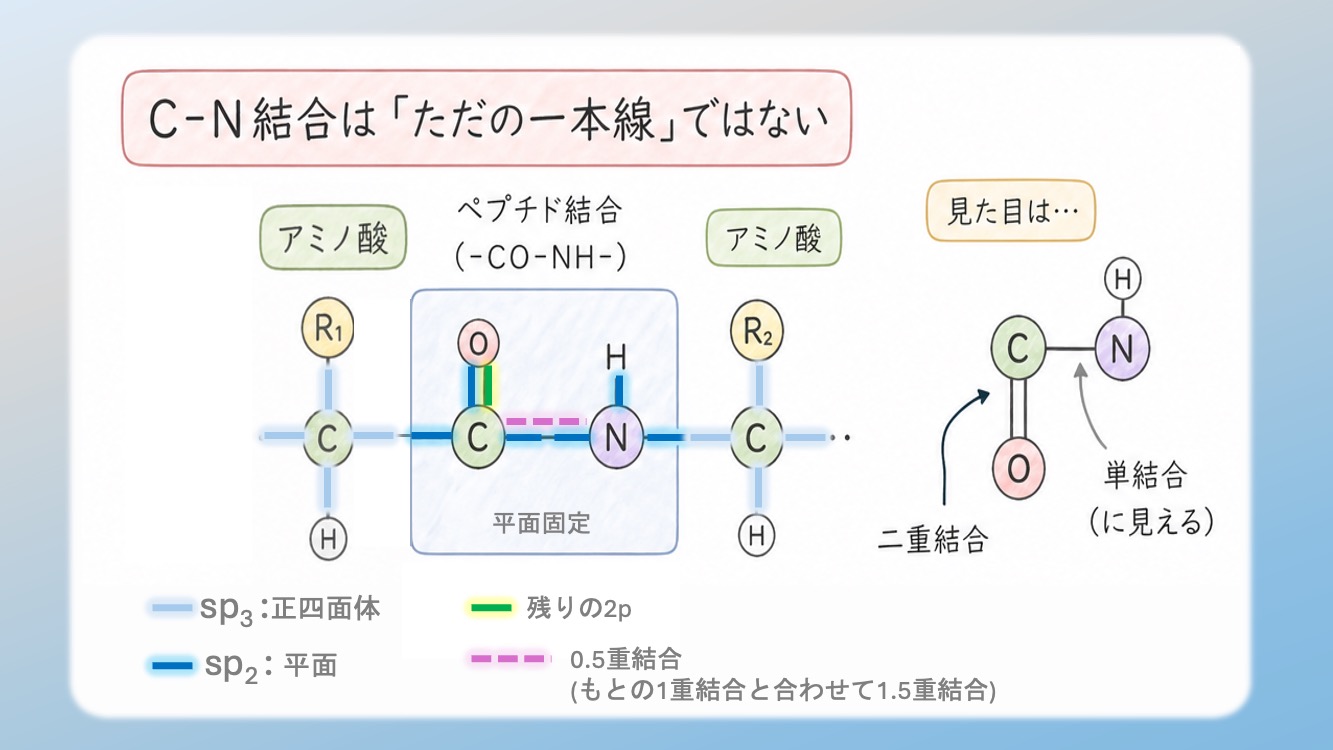
第1章:【衝撃の事実】C-N結合は「ただの一本線」ではない
▲ 目次へ
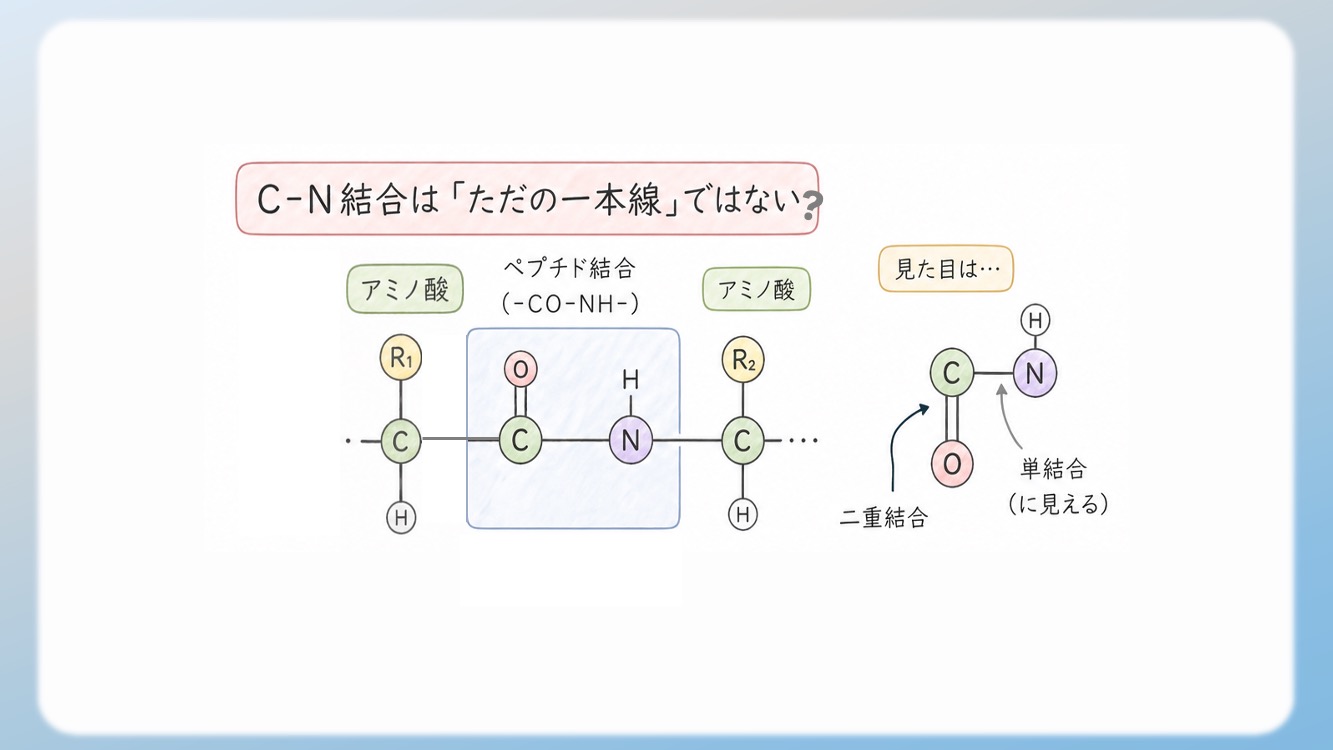
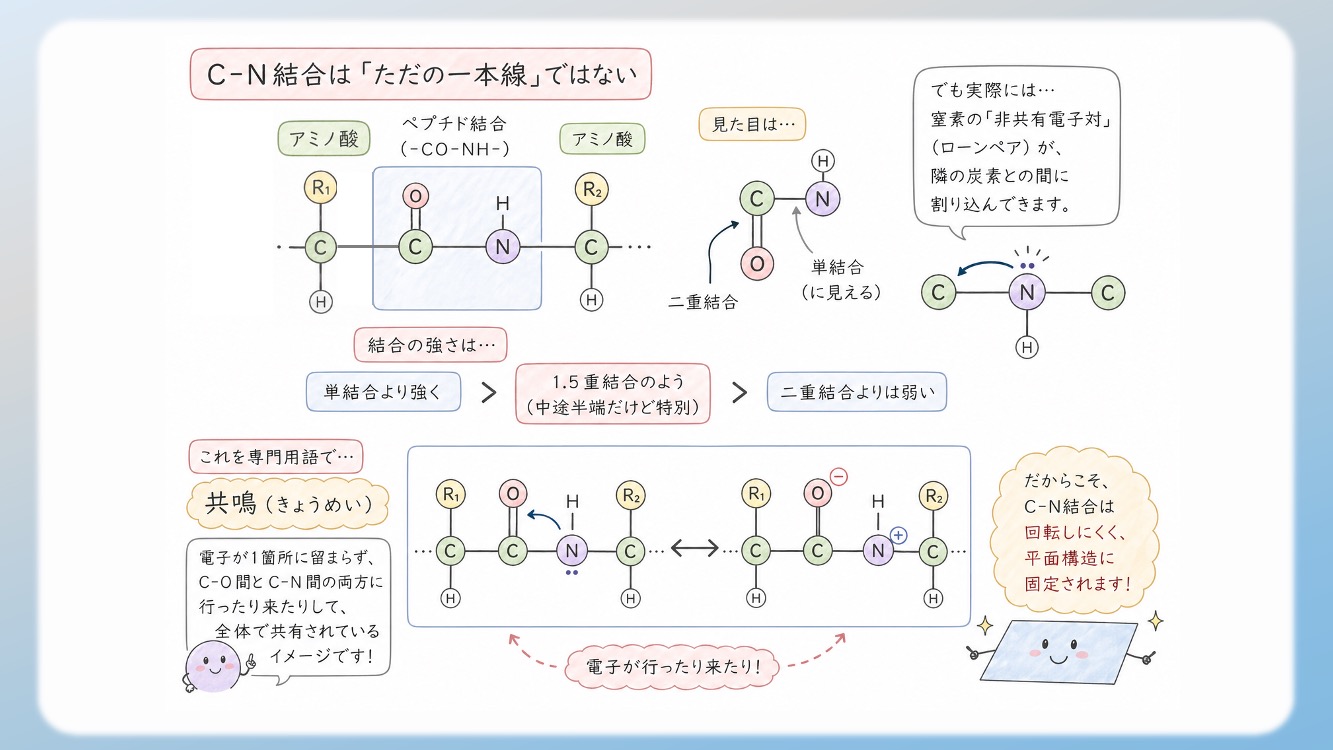
アミノ酸のペプチド結合(-CO-NH-)を詳しく見ると、炭素(C)と酸素(O)の間には二重結合があります。一方、炭素(C)と窒素(N)の間は単結合に見えます。

🤔 実際には何が起きているのか?
しかし実際には、窒素が持っている「非共有電子対(ローンペア)」が、隣の炭素との間に割り込んできます。その結果、結合の強さは以下のようになっています。
いわば「1.5重結合」のような中途半端で、でも特別な状態になっているのです。
これを専門用語で「共鳴(きょうめい)」と呼びます。
【共鳴のイメージ】
電子が1箇所に留まらず、C-O間とC-N間の両方に行ったり来たりして、全体で共有されている状態です。


第2章:【伏線回収】アミノ酸が「板」になる瞬間——ローンペアが起こす奇跡
▲ 目次へ
1. 化学の鉄則:電子は「ペア」で動く——窒素が仕掛けるC-N結合のアップデート
さらに詳しく電子の動きをみてみましょう。
化学の世界では、結合を作ったり壊したりするとき、電子は基本的に2個1組で動きます。
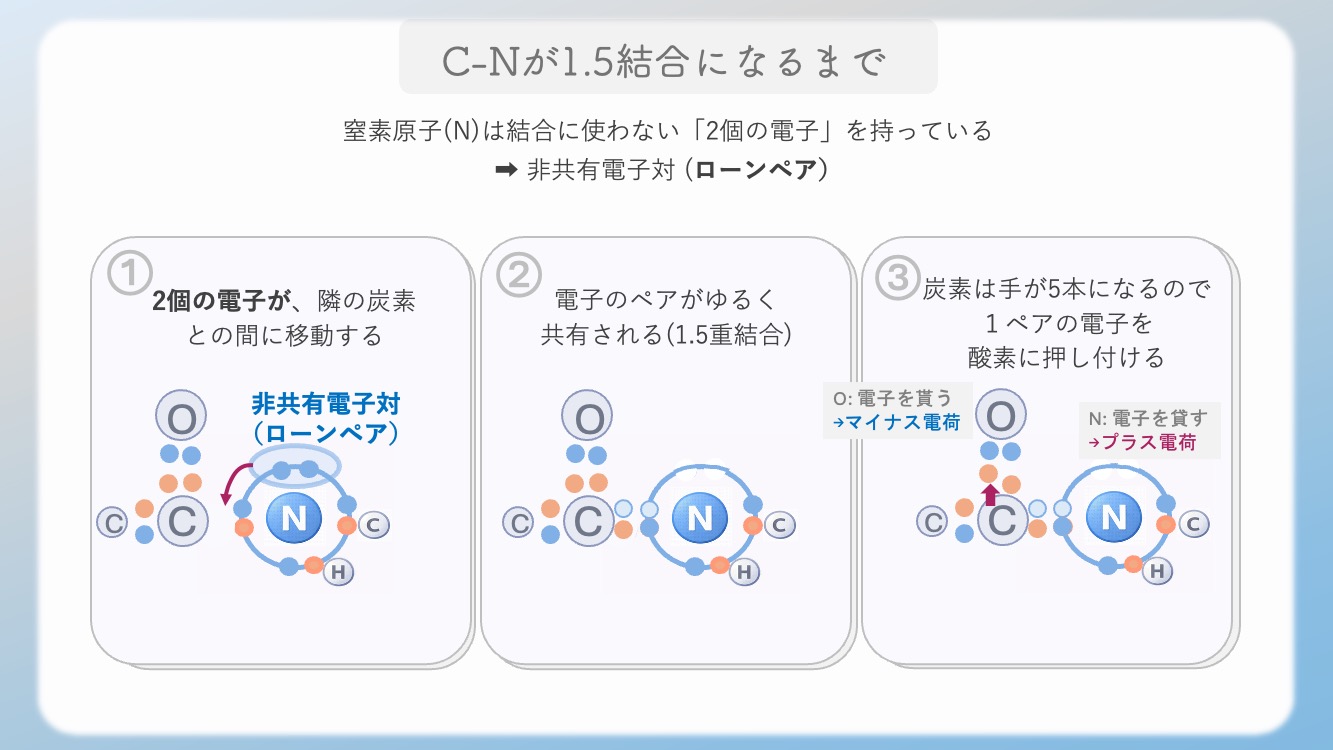
- 🔵 窒素のローンペア: 窒素原子(N)が結合に使わずに持っている「2個の電子」のことです。
- 🌊 流れ込み: この2個の電子が同時に、隣の炭素(C)との間のスペースに移動します。
これによって、もともと「一本線(単結合)」だった炭素と窒素の間に、もう一本の結合の「もと」が供給され、二重結合のような性質が生まれます。
2. 炭素の「パンク」を回避せよ!——押し出される電子と電荷のバランス
窒素から2個の電子が流れ込んでくると、炭素(C)は「手が5本」になってしまい、パンクしてしまいます。そのため、炭素はもともと酸素(O)との間に持っていた二重結合のうち、1ペア(2個)の電子を酸素の方へ押し出します。
結果: 酸素側は電子をもらって「マイナス」の性質を帯び、
電子を貸し出した窒素側は「プラス」の性質を帯びます。
このように、電子のペアが「流れる」と「押し出される」が同時に起こることで、全体のバランスが保たれています。
3. 【本質理解】1.5重結合という「曖昧さ」の正体——「ふわっと共有」が生命を支える
電子のペアが完全にあっちに行ったりこっちに来たりするのではなく、「両方の原子の間で、電子のペアがふわっと共有されている」状態だと考えてください。
C-N 間に電子2個
C=N 間に電子4個
ペプチド結合はこの中間なので、「常に電子が3個くらいの間にあるような状態」、
つまり 1.5重結合 というイメージになります。
第3章:1.5重結合の代償 —— 「回れない」からこそ、タンパク質は美しい
▲ 目次へ
この「1.5重結合」が、私たちの体の中でとんでもなく重要な役割を果たしています。
普通の単結合(一本線)であれば、そこを軸にして分子はコマのようにクルクル自由に回転できます。しかし、二重結合の性質が混ざったペプチド結合は、「硬くて回転できない」という性質を持ちます。
回転できないため、ペプチド結合に関わる炭素、酸素、窒素、水素の原子たちは、すべて同じ一枚の板(平面)の上にピタッと固定されます。
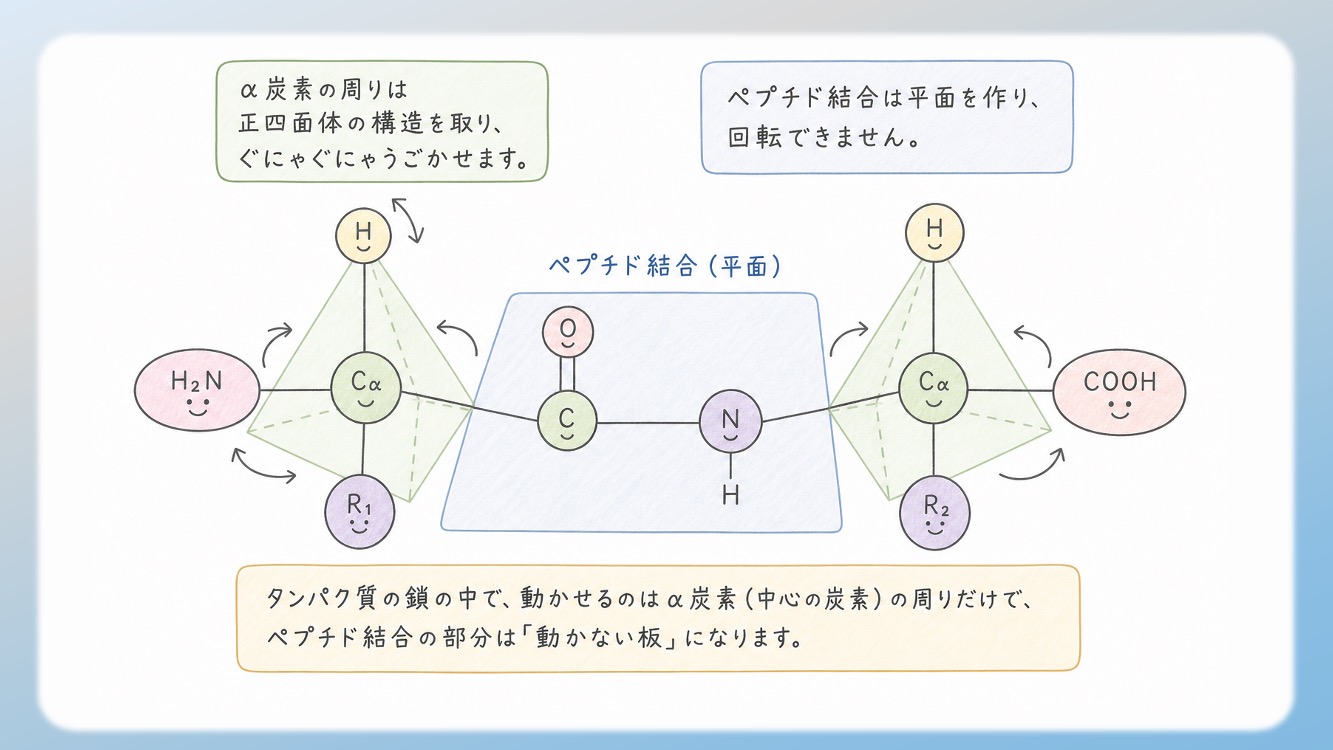
タンパク質の鎖の中で、動かせるのはα炭素(中心の炭素)の周りだけで、ペプチド結合の部分は「動かない板」になります。
この「不自由さ」が生命を支えている
もし、窒素と炭素の結合が単純な単結合で、どこでも自由にクルクル回ってしまったらどうなるでしょうか?
タンパク質の長い鎖は、決まった形を保てず、まるで茹でたてのスパゲッティのようにクネクネと形を変え続けてしまいます。そうなると、特定の形が必要な「酵素」や「筋肉」として働くことができません。
「窒素と炭素が簡単には回らない」というルールがあるおかげで、
タンパク質は複雑で精密な立体構造(αヘリックスやβシート)をカチッと作ることができるのです。
第4章:【まとめ】なぜ生命は「1.5重結合」を選んだのか?
▲ 目次へ
教科書の化学式に書かれた一本の線。
その裏側では、電子が絶え間なく共有され、
強固な「1.5重結合」が形作られています。
● アミノ酸同士のC-N結合は、電子が共有されることで「1.5重結合」になる。
● そのため、単結合のように自由に回転できず、「平面構造」を作って固定される。
● この「硬さ」があるからこそ、タンパク質は決まった形(立体構造)を維持し、生命としての機能を果たすことができる。
「不自由さ」という名の恩恵:平面構造がタンパク質に命を吹き込む
自由な回転を捨て、あえて「平面」として固定されること。この一見不自由なルールこそが、複雑な立体構造(αヘリックスやβシート)を可能にし、私たちの体を動かす「機能」を生み出しています。


この「固い板」の繋がりこそが、精密なタンパク質を作るための秘策なのよ!
【エピローグ】化学式を「立体」で読み解く知性を手に入れたあなたへ
▲ 目次へ
暗記に頼らず、sp3 や sp2、そして電子の動きからアミノ酸を捉えた今、
あなたの生化学の視界は劇的に変わりました。
この「理詰めの思考」は、今後のCBTや国試、
そして臨床の現場でも、あなたを助ける最強の武器になります。
8. 【実力判定】CBT・国試レベルを突破する「混成軌道」攻略テスト
▲ 目次へ
【問題1】
アミノ酸の基本骨格において、アルファ炭素(中心の炭素)がとる混成軌道と、それによって形成される立体構造の組み合わせとして正しいのはどれか?
b) sp2 混成軌道 ―― 正三角形構造
c) sp3 混成軌道 ―― 正四面体構造
d) sp3 混成軌道 ―― 平面四角形構造
▶ 解答・解説を確認する
正解:c
中心のアルファ炭素は、4つの異なるグループと単結合(シグマ結合)で繋がっています。このとき炭素は sp3 混成軌道 をとり、結合角は約 109.5度の 正四面体構造 になります。
【問題2】
タンパク質のペプチド結合(-CO-NH-)に関する記述のうち、正しいのはどれか?
b) C-N結合は単結合として自由に回転できる。
c) 電子の共鳴により、結合は「1.5重結合」のような性質をもつ。
d) 酸素、炭素、窒素、水素の4原子はすべて異なる平面上に位置する。
▶ 解答・解説を確認する
正解:c
窒素(N)上のローンペア(非共有電子対)が、隣の炭素(C)と共鳴することで、ペプチド結合は 1.5重結合 の性質を持ちます。このため結合の回転が制限され、原子は同一の 平面構造 上に固定されます。
【問題3】
ペプチド結合が「回転できない(平面構造である)」ことによって生じる、タンパク質の構造上のメリットとして最も適切なものはどれか?
b) 特定の立体構造(二次構造など)を安定して維持できる。
c) 他のアミノ酸と結合しやすくなる。
d) 熱に強くなり、100度でも変性しなくなる。
▶ 解答・解説を確認する
正解:b
もし結合が自由に回ってしまうと、タンパク質は決まった形を保てません。「1.5重結合」による不自由さ(平面構造)というルールがあるからこそ、アルファヘリックスやベータシートといった精密な立体構造を安定して作ることができるのです。





