8. アミノ酸滴定曲線がついに読める

〜pKa・等電点・緩衝域を一気につなぐ〜
※本記事にはアフィリエイトリンクが含まれる可能性があります。
2.H⁺ がつく場所と外れる場所。 まず基本をおさえよう▲ 目次へ

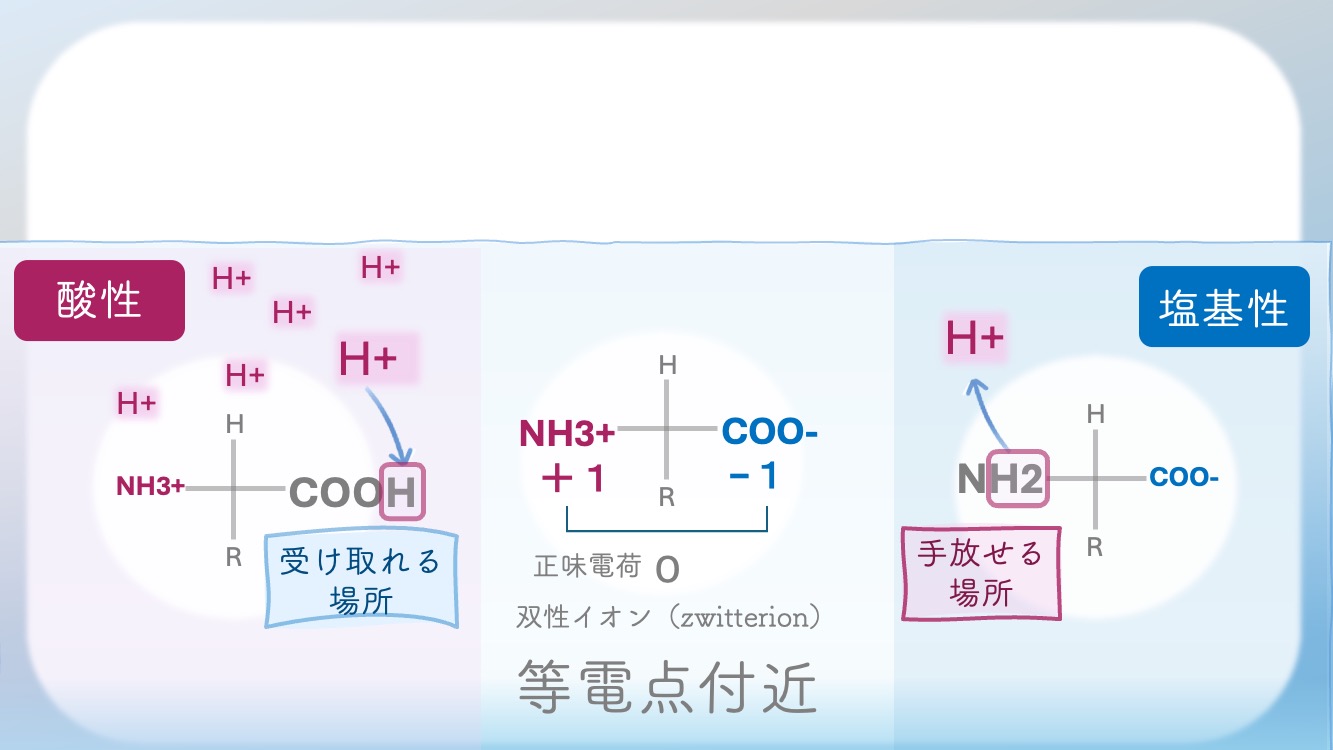
アミノ酸には、H⁺ を受け取れる場所 と、
H⁺ を手放せる場所 があるよ。

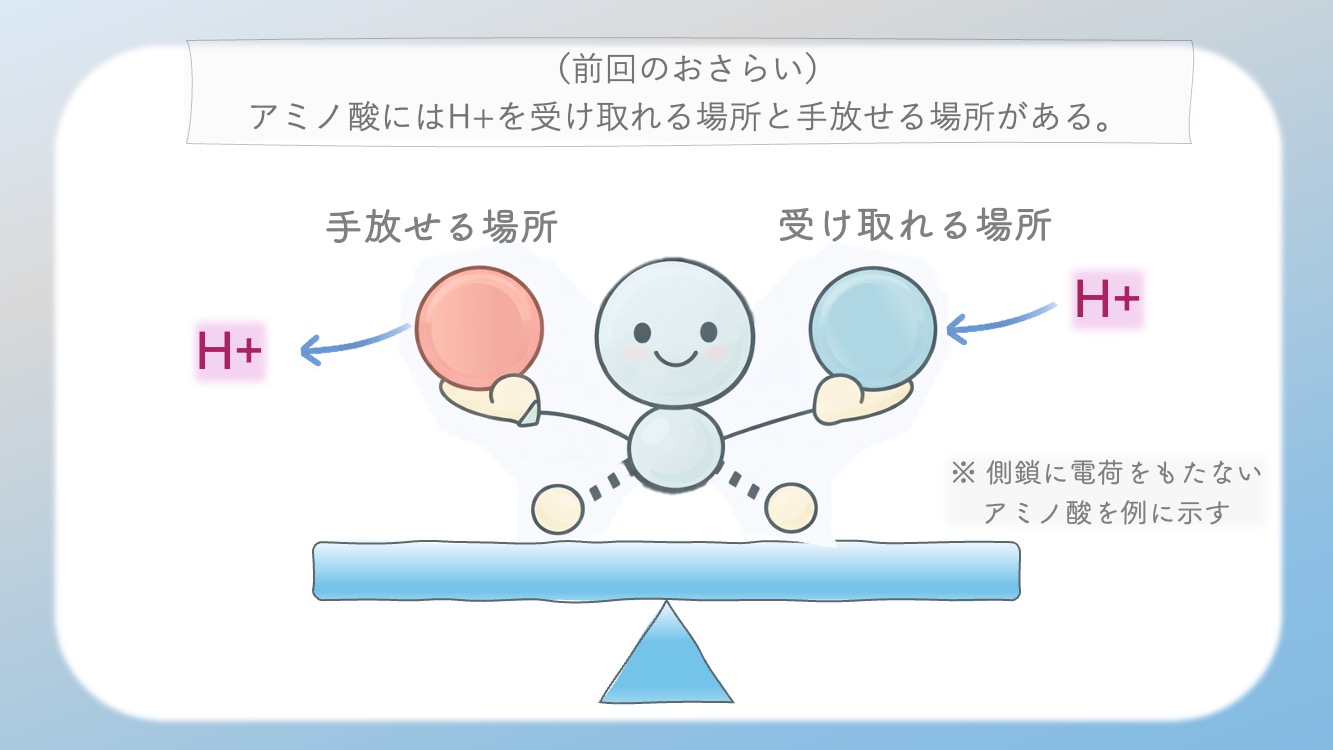

そう。
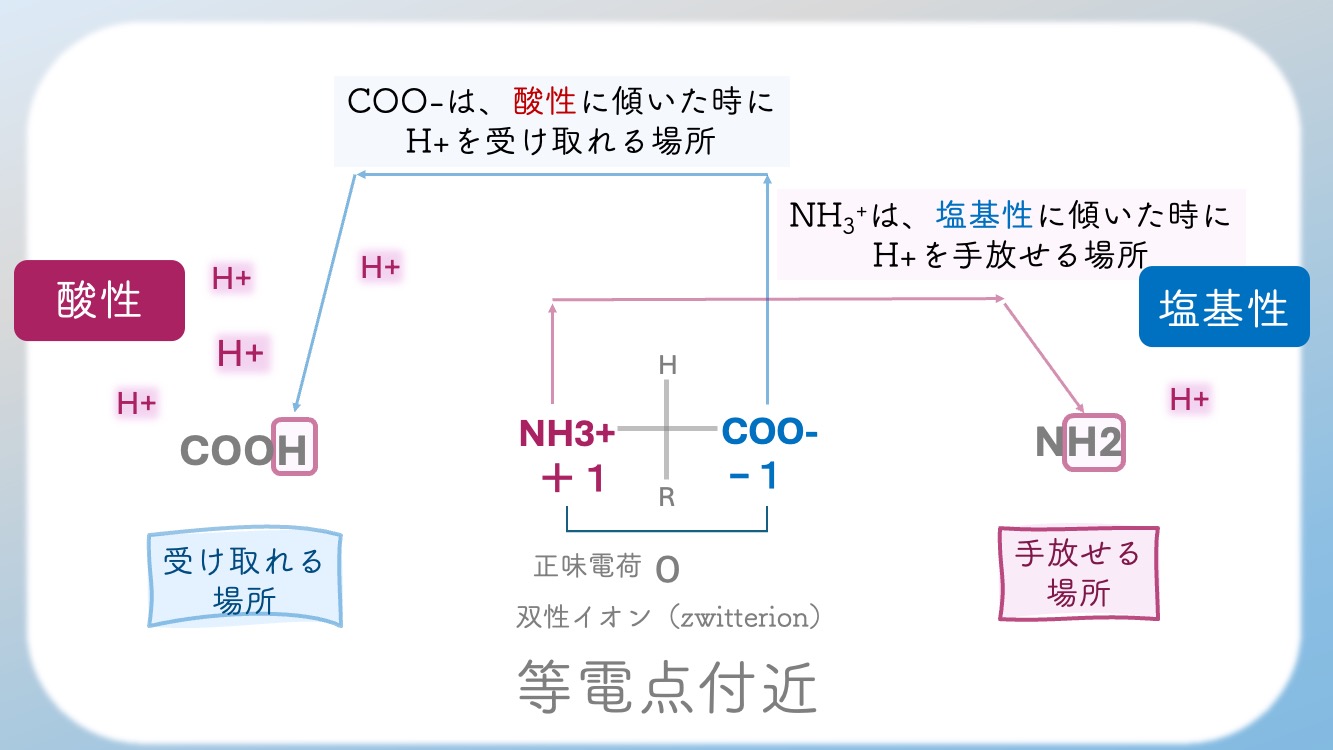
・マイナスの場所は、
プラスを受け取れる。
・H+を持っているからプラスの状態である場合、
H+を手放すことができるんだ。
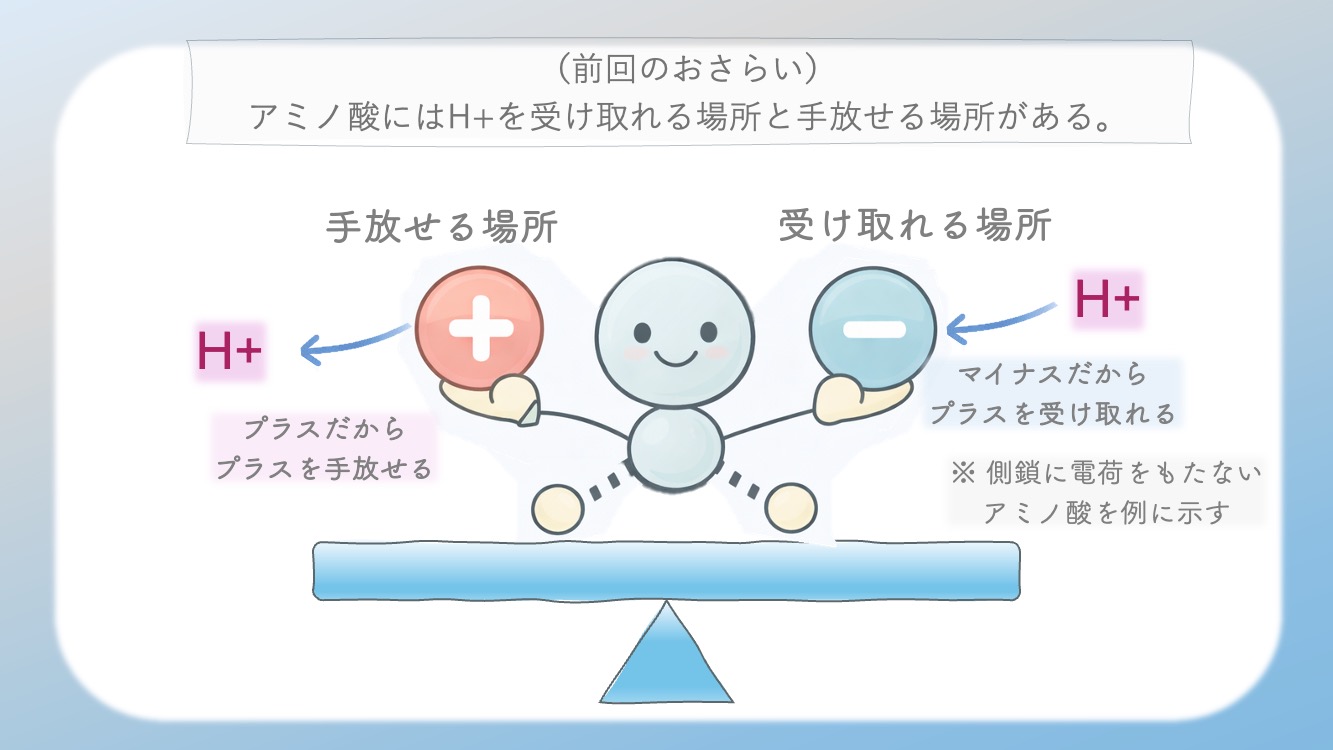

どこが手放す場所なのか?
常に意識しておくと、今何がおこっているのか
わかりやすくなるよ。

水の中では、その形が多いんだよね。


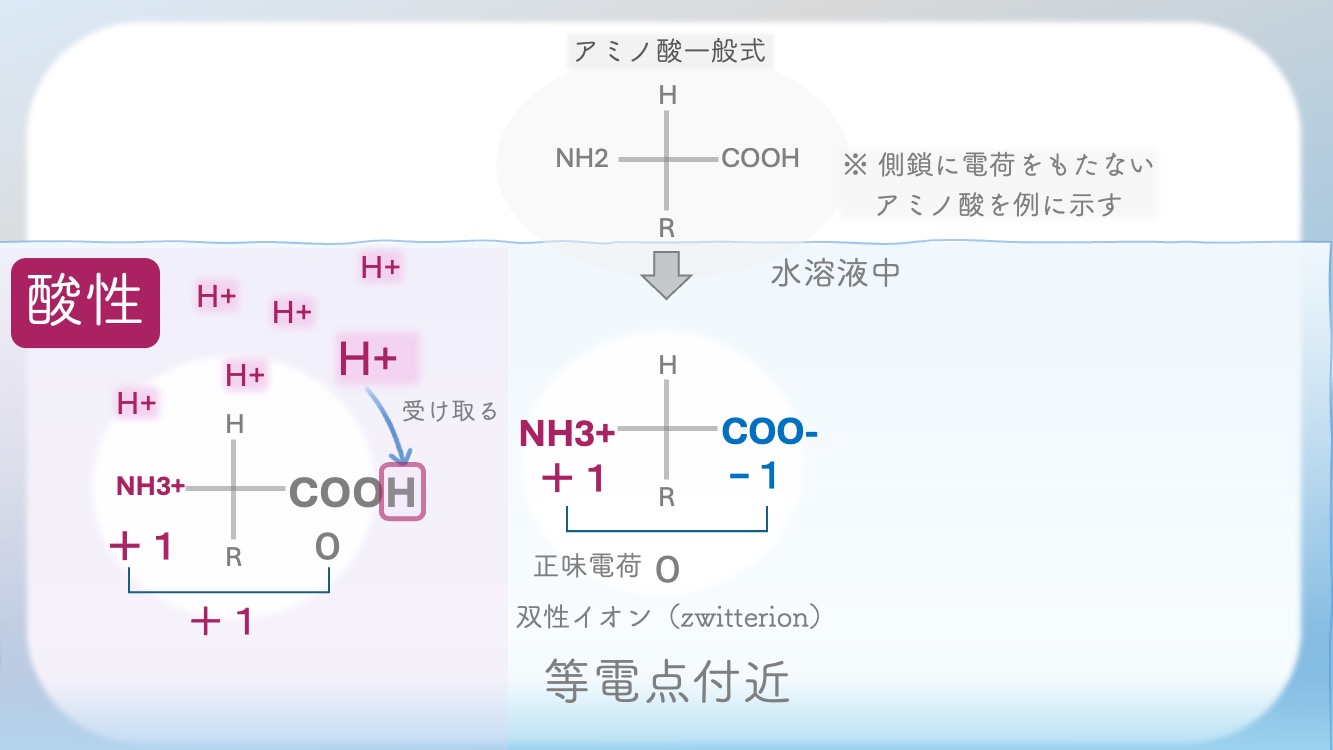
酸性、つまり pH が低いと、H⁺ が多い。
だからアミノ酸は、H⁺ を受け取った形に
なりやすいんだ。
受け取るほうに傾くのか。


逆に、pH が上がると、H⁺ は少なくなる。
だからアミノ酸は、
少しずつ H⁺ を手放していくよ。
今度は持っている H⁺ を手放していくんだね。

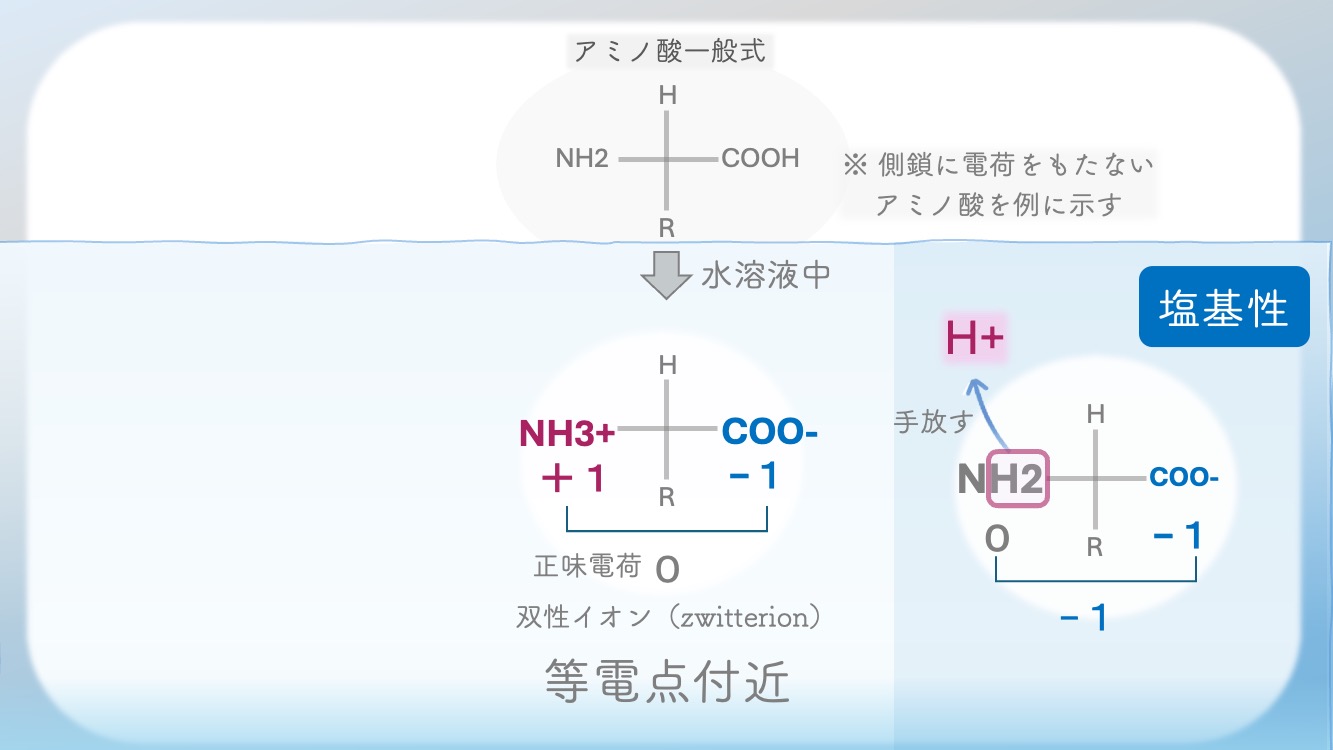

NH3+はH+を手放せる場所。
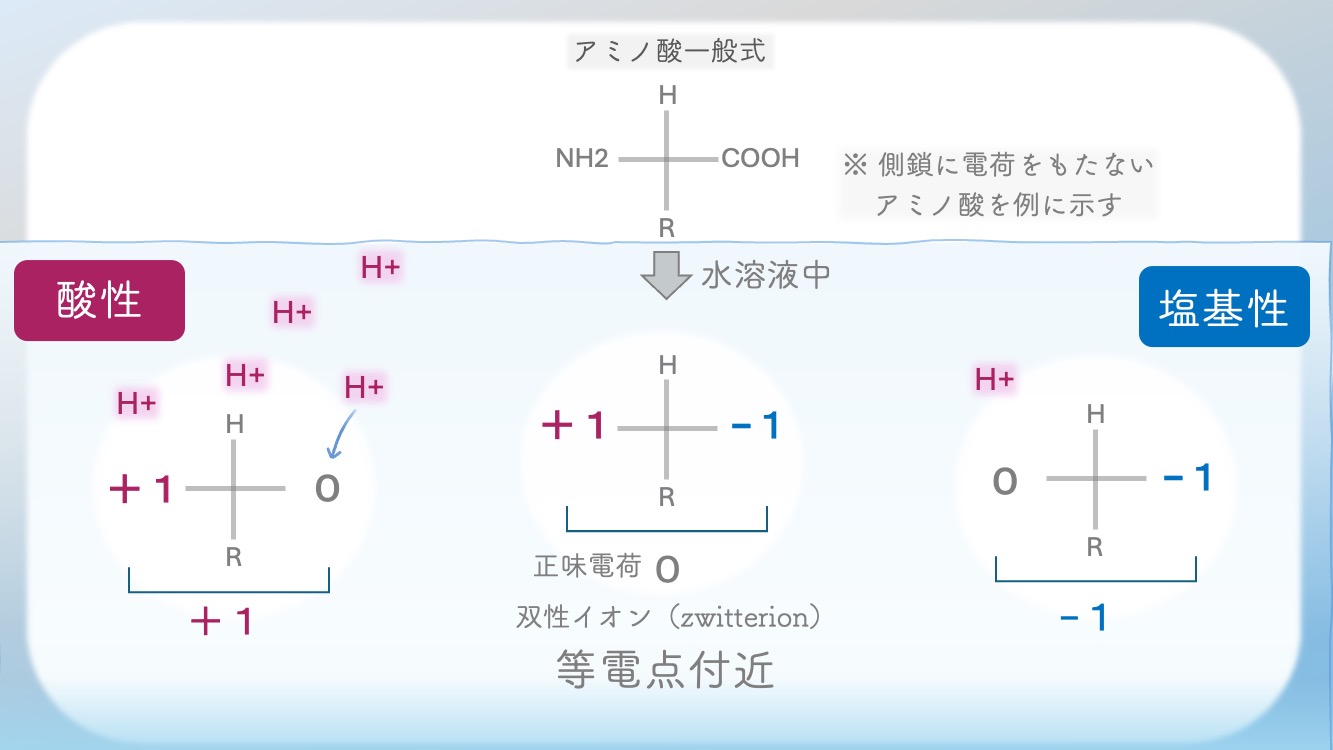
それぞれの”場所”の意味を
ここでしっかり確認しよう!


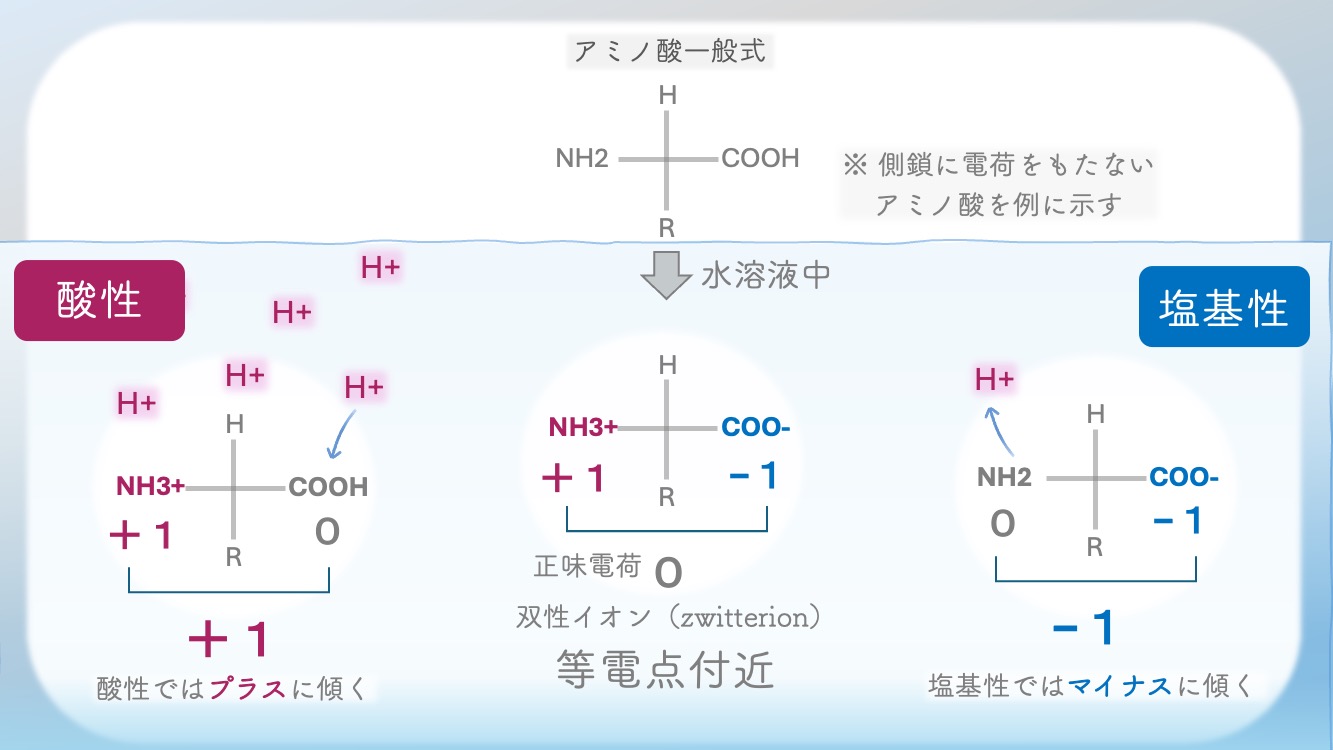

・H+がたくさんあると、
H+を受け取るからプラスに傾く。
・H+が少ししかないと、
持っているH+を手放すからマイナスに傾く。
マイナス寄りになるかが変わるんだ。


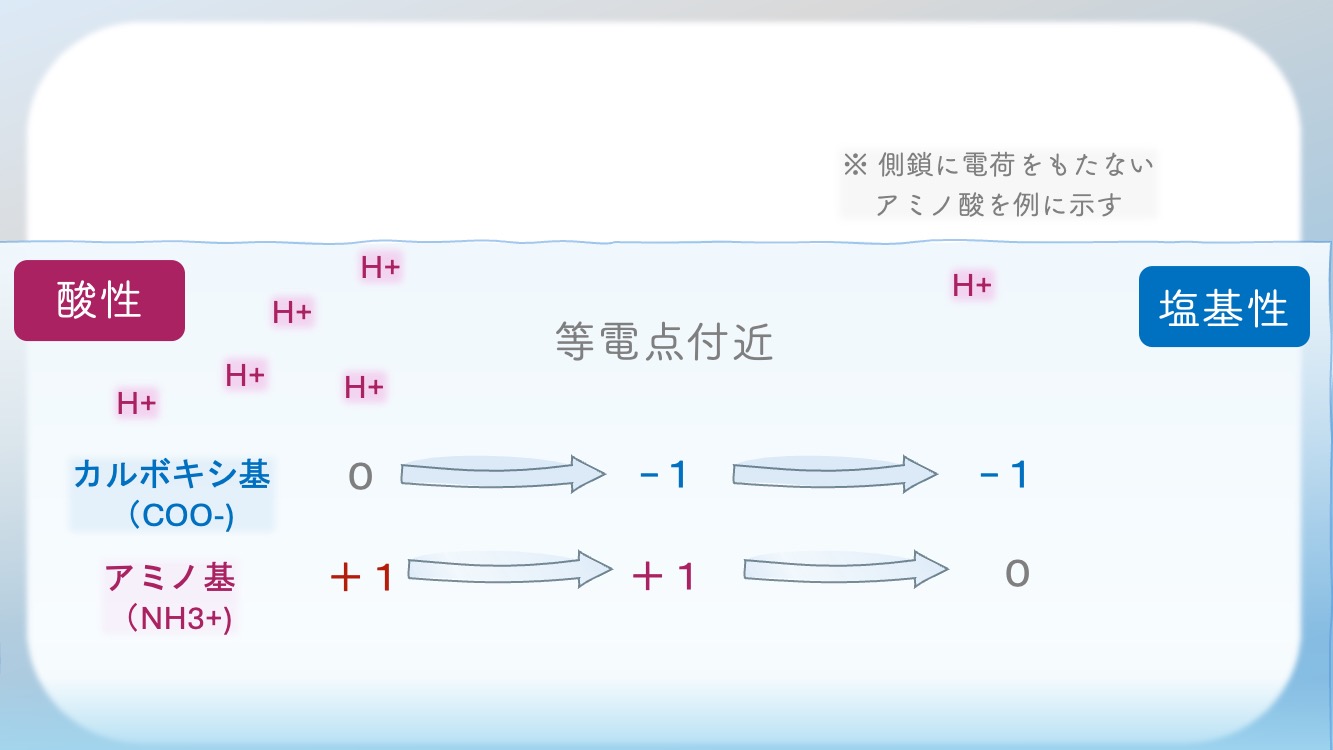

この H⁺ の出入り を線で見せている図なんだ。
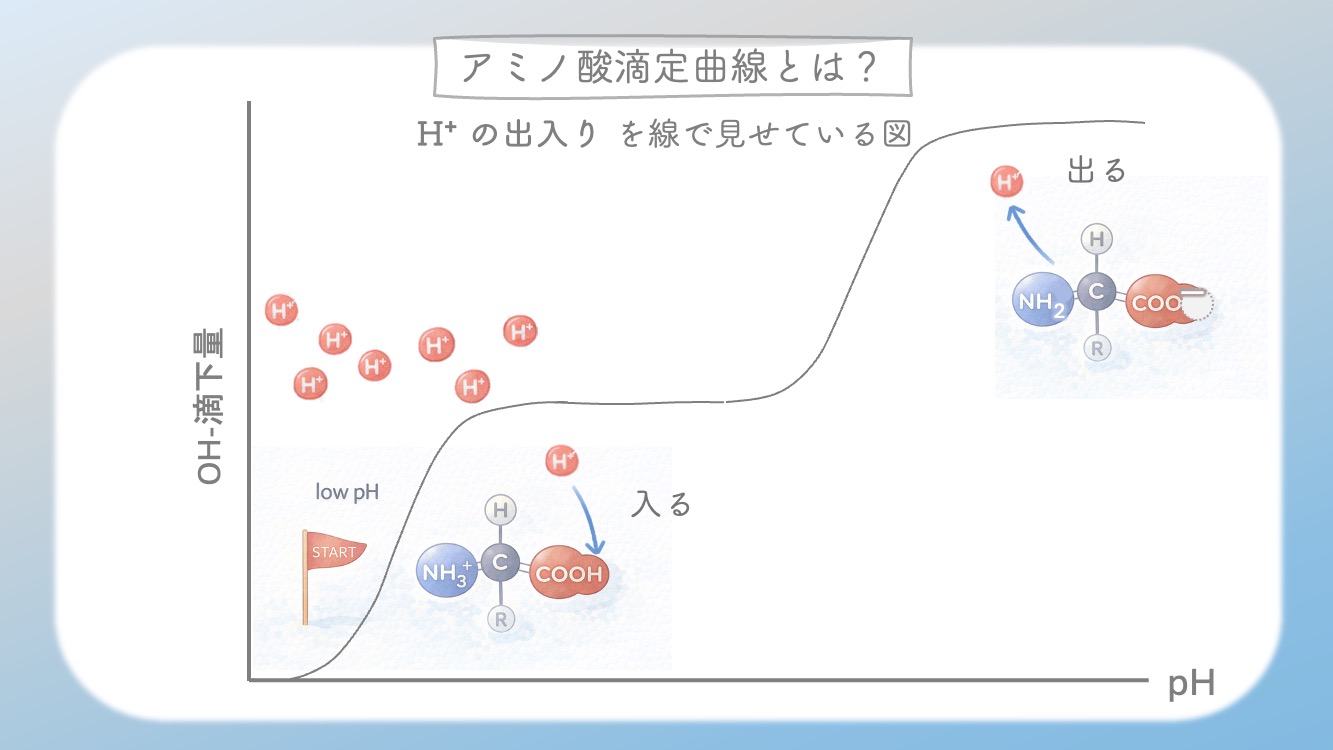

しているよ。
酸性の溶液からスタートして、
それにOH⁻を少しずつ加えると、H+が中和されるから
溶液は酸性からだんだん中性→アルカリ性に変わっていく。
そのとき、アミノ酸のイオン性がどう変化するのかを
見ているよ。

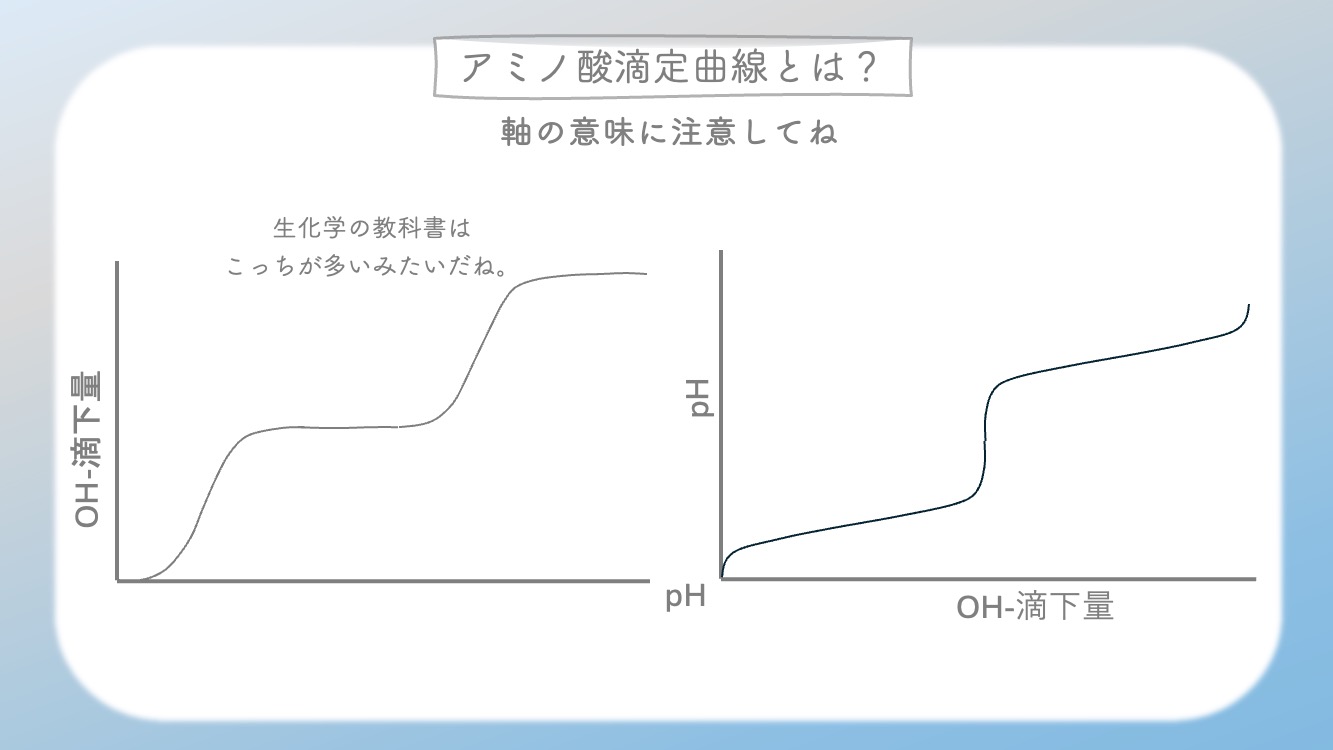
横軸が OH⁻ の滴下量、縦軸が pH のグラフも
よく出てくるよ。試験では、軸の意味を取り違えないように
気をつけてね。
そこはちゃんと見ないと危ないね。

3. いちばんシンプルな グリシンで意味をつかむ▲ 目次へ
側鎖は ”Hだけ” だったよね。


グリシンは、側鎖がいちばんシンプルなんだ。
アミノ酸の基本を考えるときの出発点にしやすいんだよ。

注目すべき主な場所は2つ。
・COO-
・NH3⁺


pH がとても低いというのは、
まわりに H⁺ がたくさんある、ということなんだ。
グリシンは H⁺ を取り込みやすいんだね。

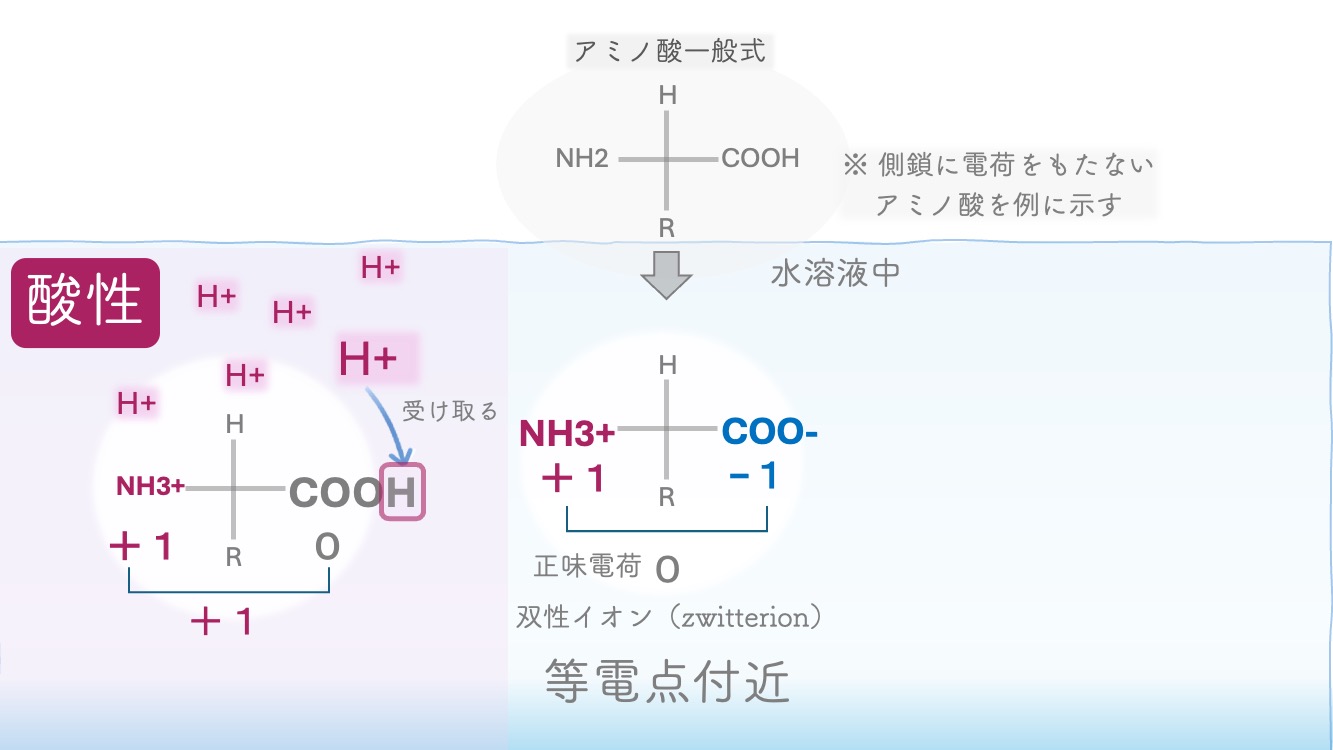

グリシンは H⁺ をしっかり持った形になりやすい。

H⁺ を手放せる側も、
どちらも H⁺ を持った形になりやすいんだ。
COOH と NH3⁺ の形ということ?


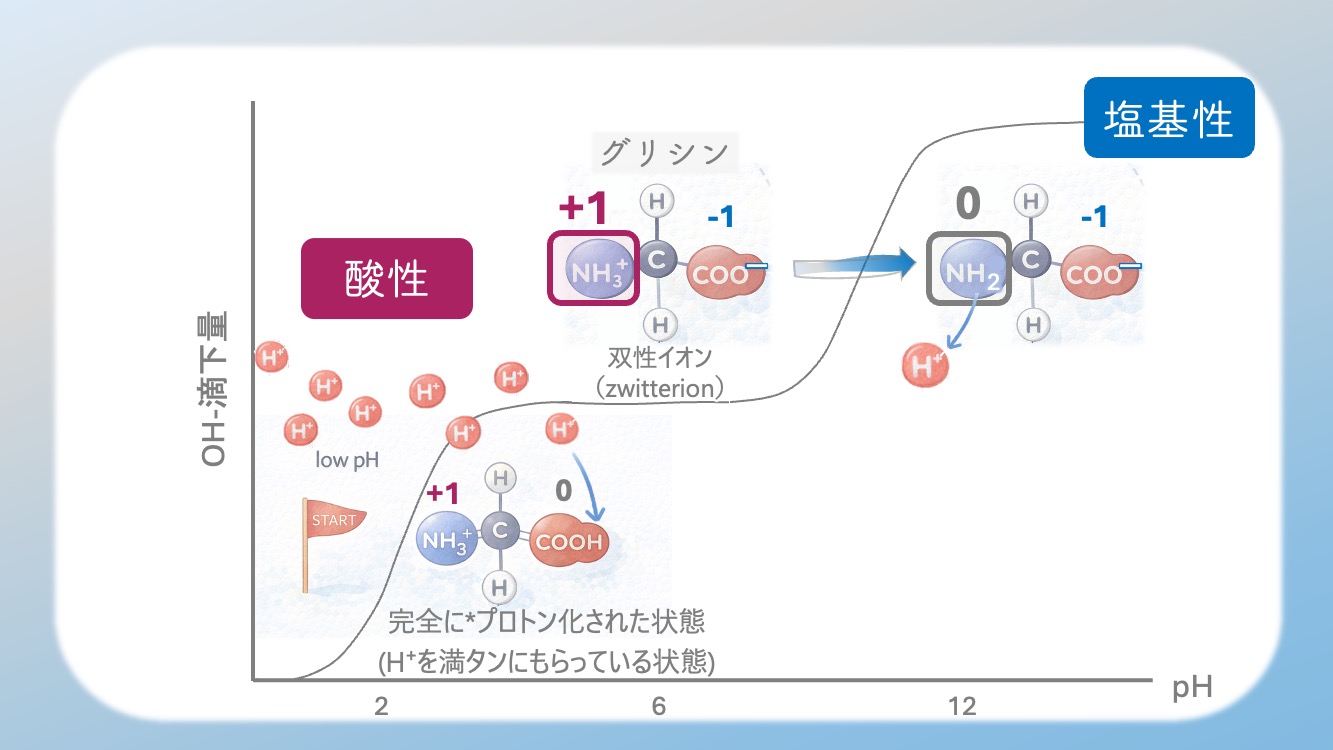
完全にプロトン化された状態なんだ。
言いかえると、
受け取れるだけの最多の H⁺ を受け取った状態だよ。

H⁺ をたくさん持ったスタート地点 と考えるといいよ。
左端は、プロトンが多い。
だから最もプロトン化された状態で出発する
んだね。

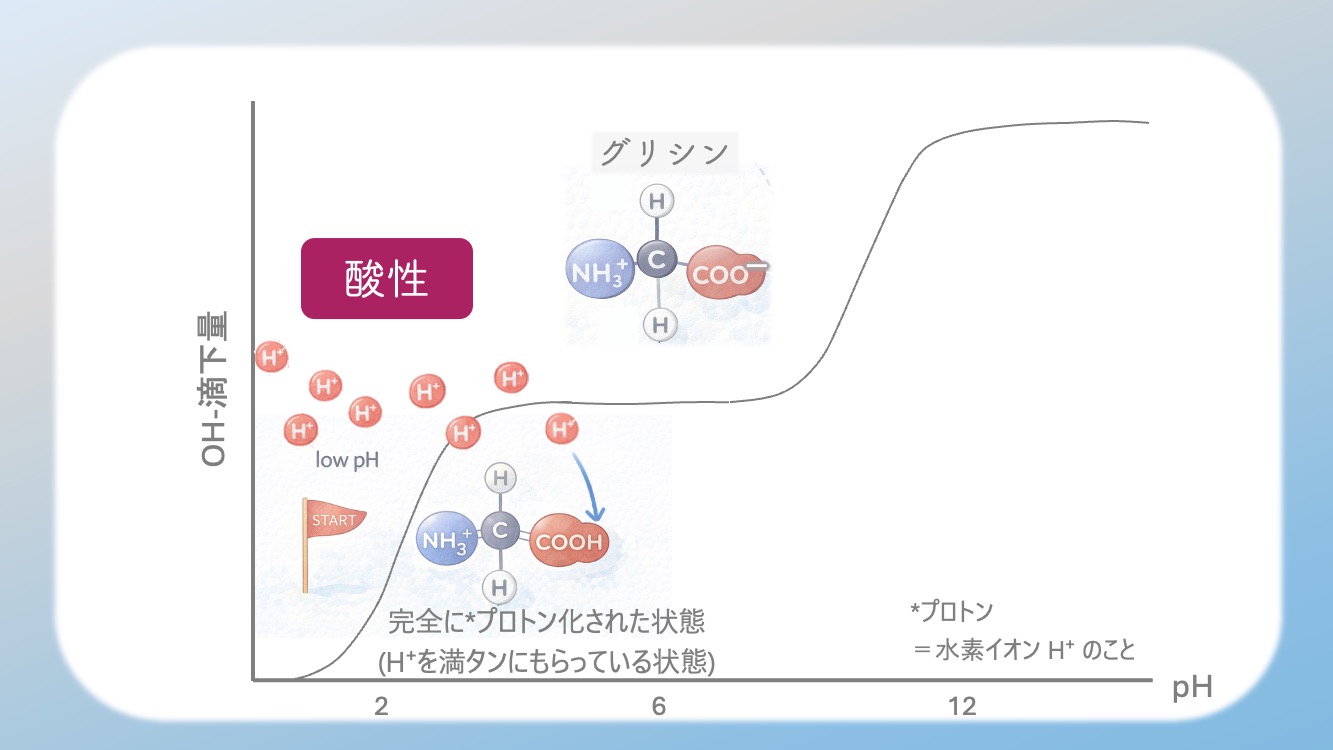
4.最初に変わるのは COOH。一気に理解が進む

まず最初に変化しやすいのは
COOH なんだ。



まわりの H⁺ がだんだん少なくなると、
待ってました!とばかり
H⁺ がCOOH から外れようとするんだ。
酸性から塩基性へ向かうとき、
もともと外れやすい
COOH からH+が外れるんだね。


NH3⁺ はまだ H⁺ を持ったままなんだ。

絶対に安定、という意味ではないよ。

H⁺ をつけたままでいるほうが有利というか、
楽なんだ。

「アミノ酸のイオン性」で詳しく話しているよ。
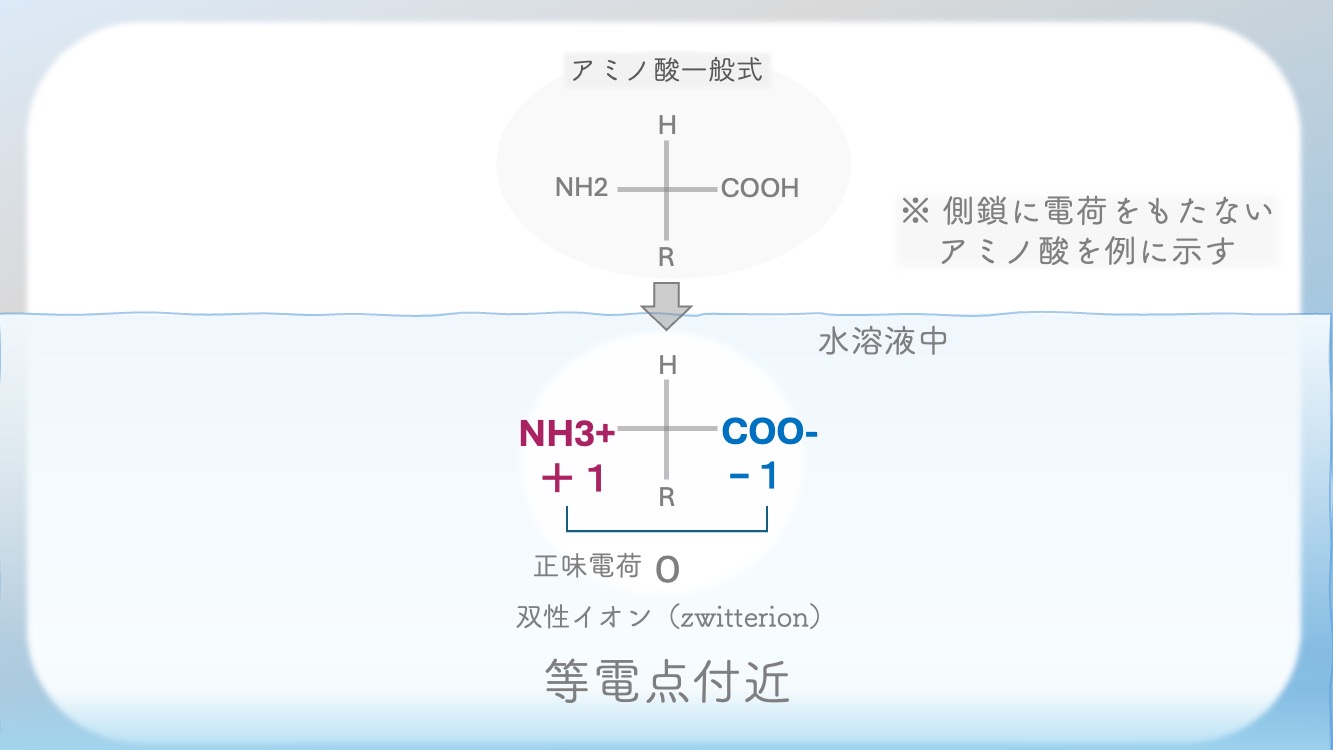
COO⁻ と NH3⁺ を両方持つ形になるんだ。


両性イオン(双生イオン・zwitterion) だよ。
マイナスもある。
でも全体としては net charge 0。


分子全体としては正味電荷は 0。

この両性イオンがいちばん多くなるんだ。
プラスもマイナスもあるのに、
全体では 0 なんだ。

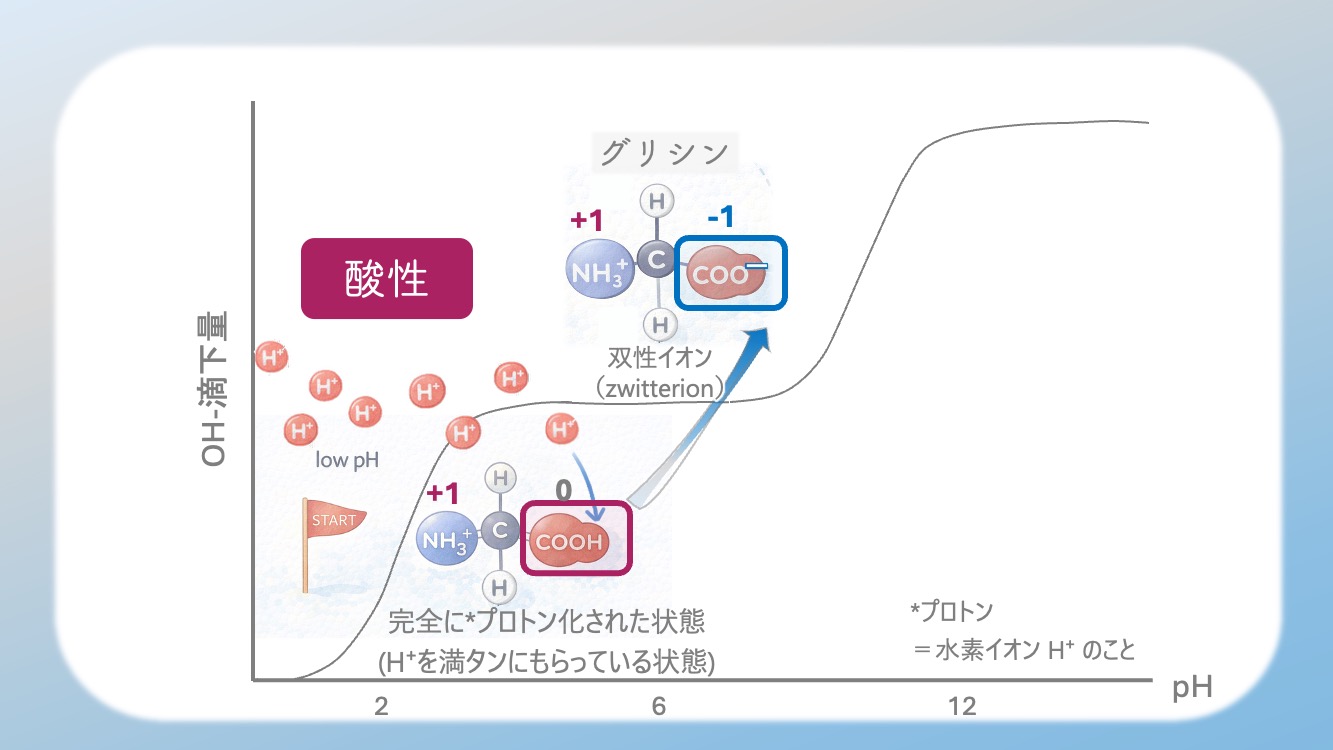
5.【最重要】pKa と緩衝域が ここでつながる

ここで、滴定曲線の見方が少し見えてくるよ。
最初の段差は、
COOH から H⁺ が外れていく変化 を
表しているんだ。
そしてその変化の真ん中あたり、
つまり 半分くらい外れたところ が
pKa なんだよ。
なるほど。
pKa って、どの pH で
その H⁺ が半分くらい外れるかを表す数値なんだね。


そう。pKa とは、
H⁺ の外れやすさを表す値だよ。
たとえば、pKa が小さいということは、
低いpHでH+を離すということ。
つまり「H⁺ を持ち続ける」より「H⁺ を放す」ほうに
傾きやすい、ということなんだ。

ブレンステッドの定義では
酸 = H⁺ を与えるものだったよね。
言い換えれば、H⁺ を手放すものと言える。
pKa が小さいとは、
より低いpHでH+を離すということ。
つまり、酸としてふるまいやすい傾向があるとも言えるね。
その結果、マイナス電荷をもつ形が増えやすい。
ただし大事なのは、
必ずしも物質全体がマイナスになるとは限らない、
ということなんだ。
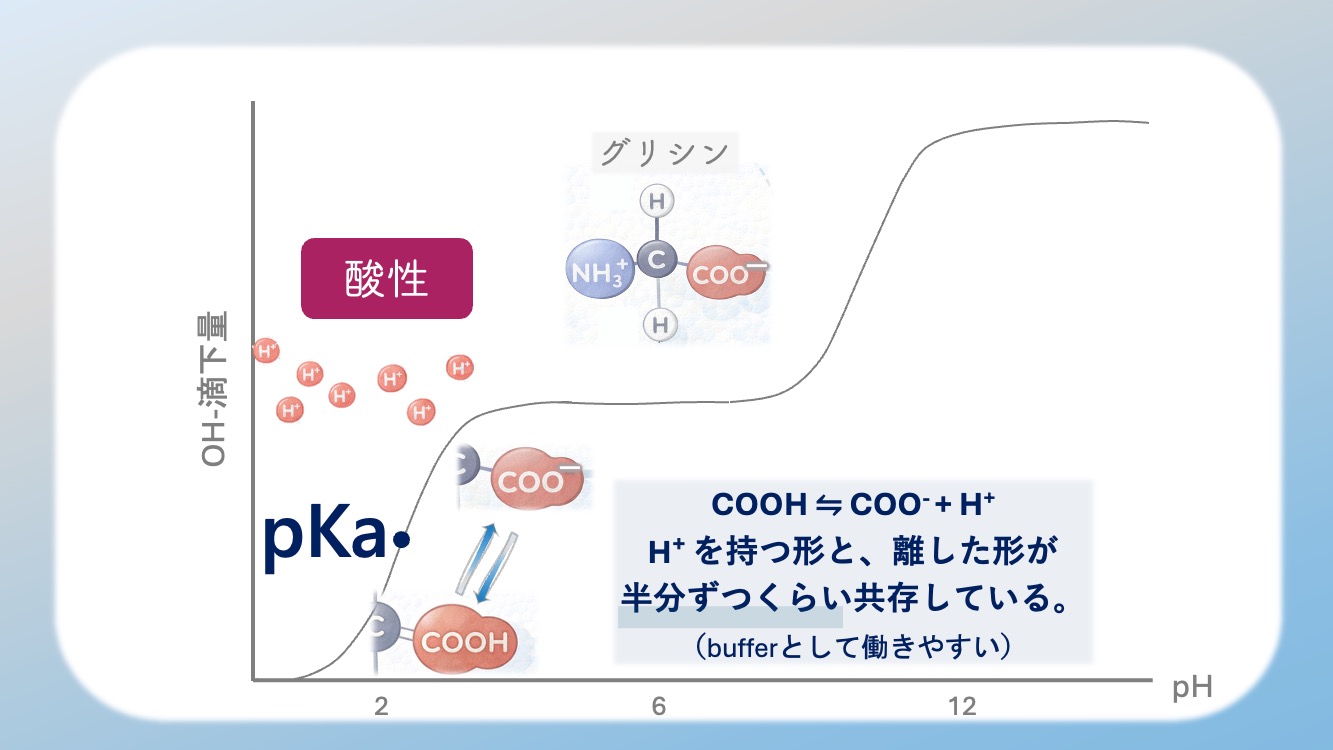
緩衝作用とは?

H⁺ を持つ形と、離した形が
半分ずつくらい共存している。

つまり緩衝作用が大きいんだよ。


pHが急に変わりにくい
という意味だよ。


少し酸やアルカリが入ると pH が変わりやすい。

すぐには強く酸性にならない。アルカリが少し入っても、
すぐには強くアルカリ性にならない。

「pHのゆれを小さくするクッション」
のようなものなんだよ。
急に変わりすぎないようにしてくれるんだ。


H⁺を受け取れる形 と H⁺を放せる形 の両方が
ほぼ同じ量でいるとき、
緩衝作用が大きいんだ。


pKa の近くでは
H⁺ を受け取る
H⁺ を放す
その両方に対応しやすく、
pHを変わりにくくできるんだよ。
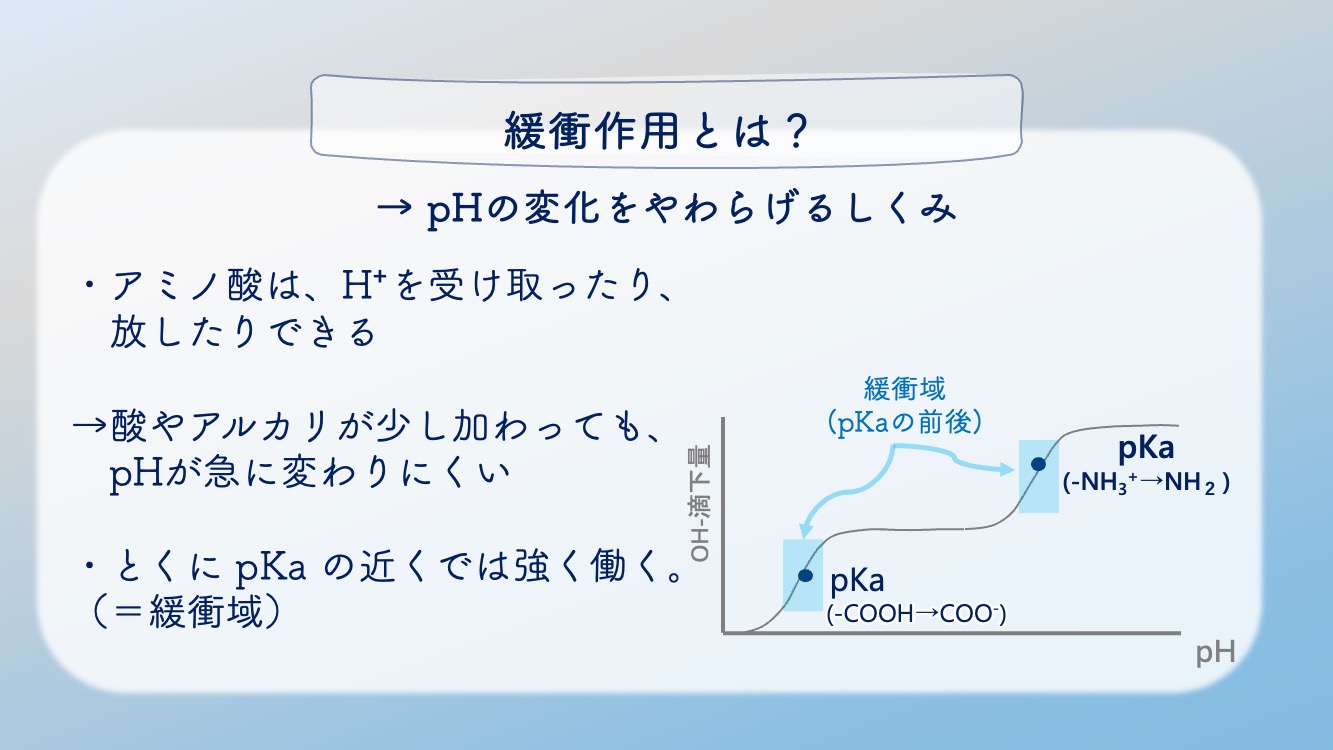

緩衝域 と呼ぶよ。
pKa の近くで、緩衝作用が大きいところ が、
緩衝域 なんだね。

6.次に動くのは NH3⁺。 2つ目の段差▲ 目次へ

今度は NH3⁺ が H⁺ を離すよ。
今度は NH3⁺ のほうが変わるんだね。


すでに COO⁻ になっているので、
NH3⁺ が H⁺を手放すと
全体としてはマイナスが強くなる。

OH⁻ を加えるにつれて、グリシンはしだいに
負に帯電していくんだ。

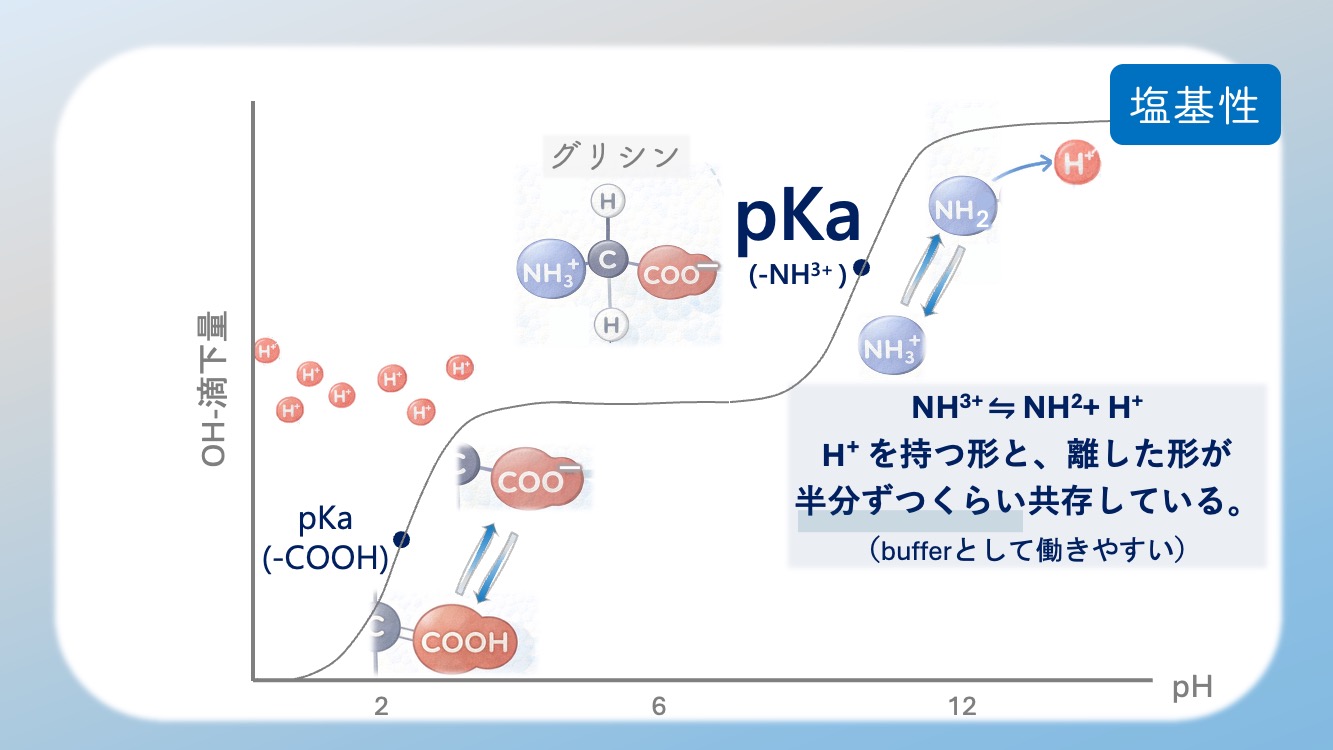
ここで2つ目の段差ができる。
そして、その真ん中あたりに、
もう1つの pKa があるよ。
NH3⁺ の pKa は約 9.6 なんだね。
COO-と比べてpKaが高いね。
かなり塩基性に傾かないと、
H⁺ が外れないということだね。

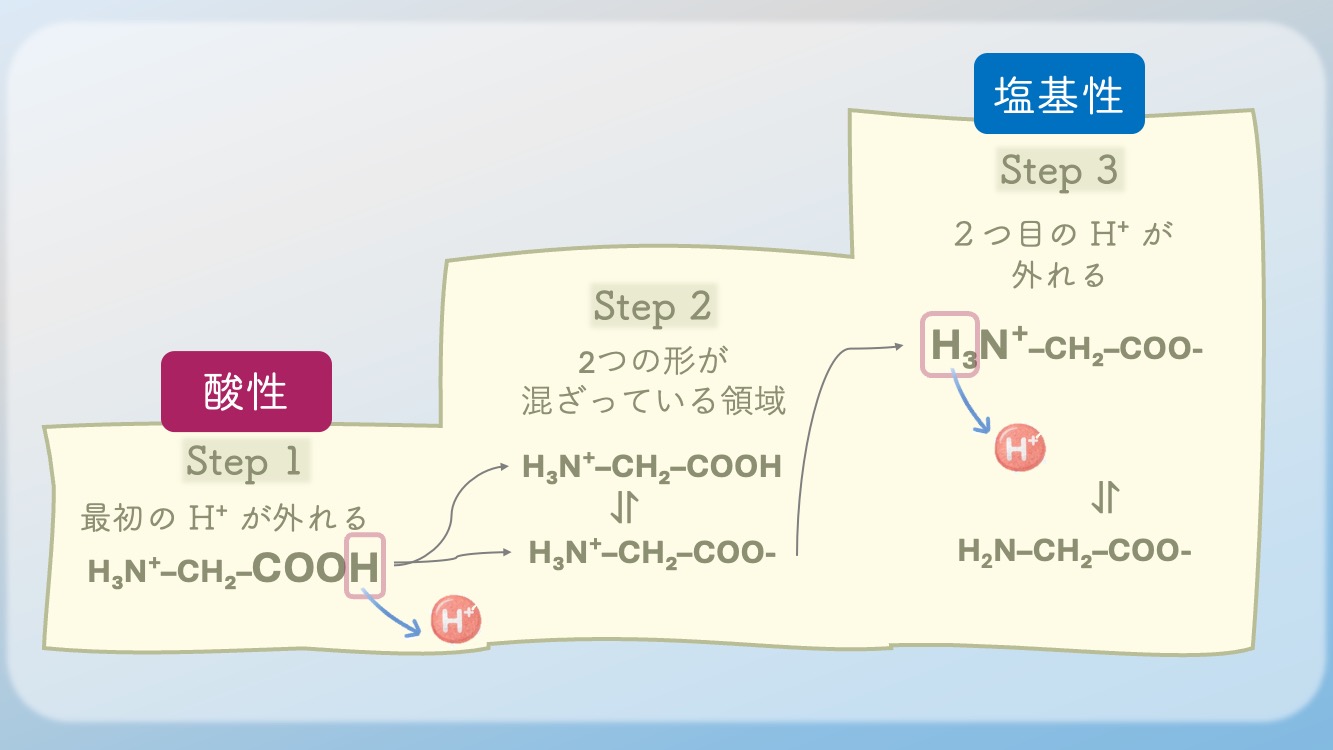
7. なぜ S字なのか? 段階ごとの脱プロトン化で見る▲ 目次へ

あの独特な S字 になると思う?


そう。その理由はシンプルだよ。
それは、H⁺ が一気に
全部外れるわけではないからなんだ。

最初に外れやすい場所がある。
次に外れる場所がある。
その途中には、
半分ずつ混ざる領域がある。
この変化が、
なだらかな部分 と
立ち上がる部分 を作るんだよ。

段階ごとの脱プロトン化の記録
と言えるね。
順番に外れていくからなんだね。

8. 等電点は“なんとなく真ん中”ではない▲ 目次へ


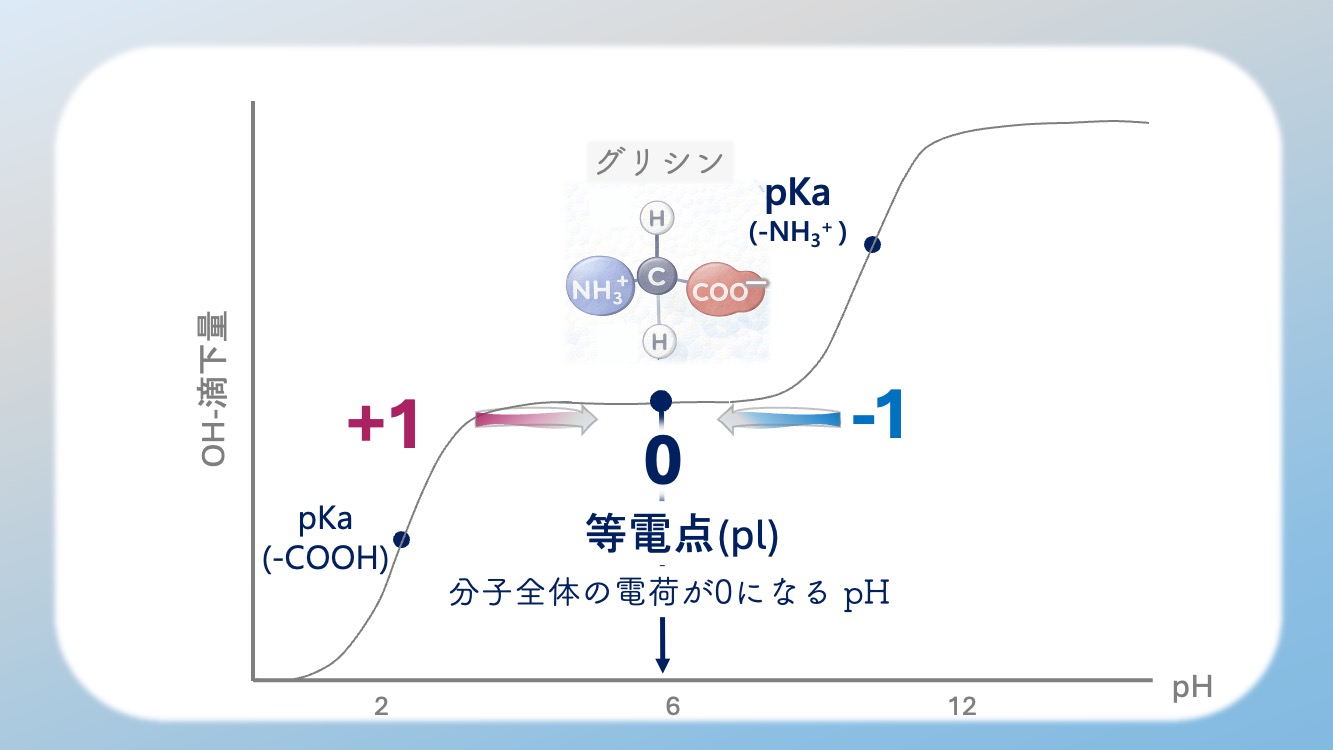
分子全体のnet chargeがゼロ、言い換えると
正味電荷が 0 になる pH のことなんだ。

それは 両性イオン(双性イオン・zwitterion) が
いちばん多いあたりになるよ。

その形が、
分子全体としてちょうど正味電荷 0 だからなんだ。
計算でも求められるの?


グリシンのように、
正味電荷 0 の形をはさむ pKa が 2つある場合は、
pI = (pKa1 + pKa2) / 2 で求めるよ。
グリシンなら、
pI = (2.34 + 9.60) / 2 = 5.97 だね。
大事なのは、
全部の pKa を足すのではなく、
正味電荷 0 の形をはさむ 2つの pKa を使う
ことだよ。
2つ目の pKa の
ちょうど間くらいに、
pI が来るってこと?


そのとおり。
ここで大事なのは、
等電点は「なんとなく真ん中」ではなく、
電荷が打ち消し合う形が中心になる場所
ということなんだよ。
電荷が 0 になることが大事なんだね。

9. 試験ではこの3つ “どこがいつ変わるか”を見る▲ 目次へ

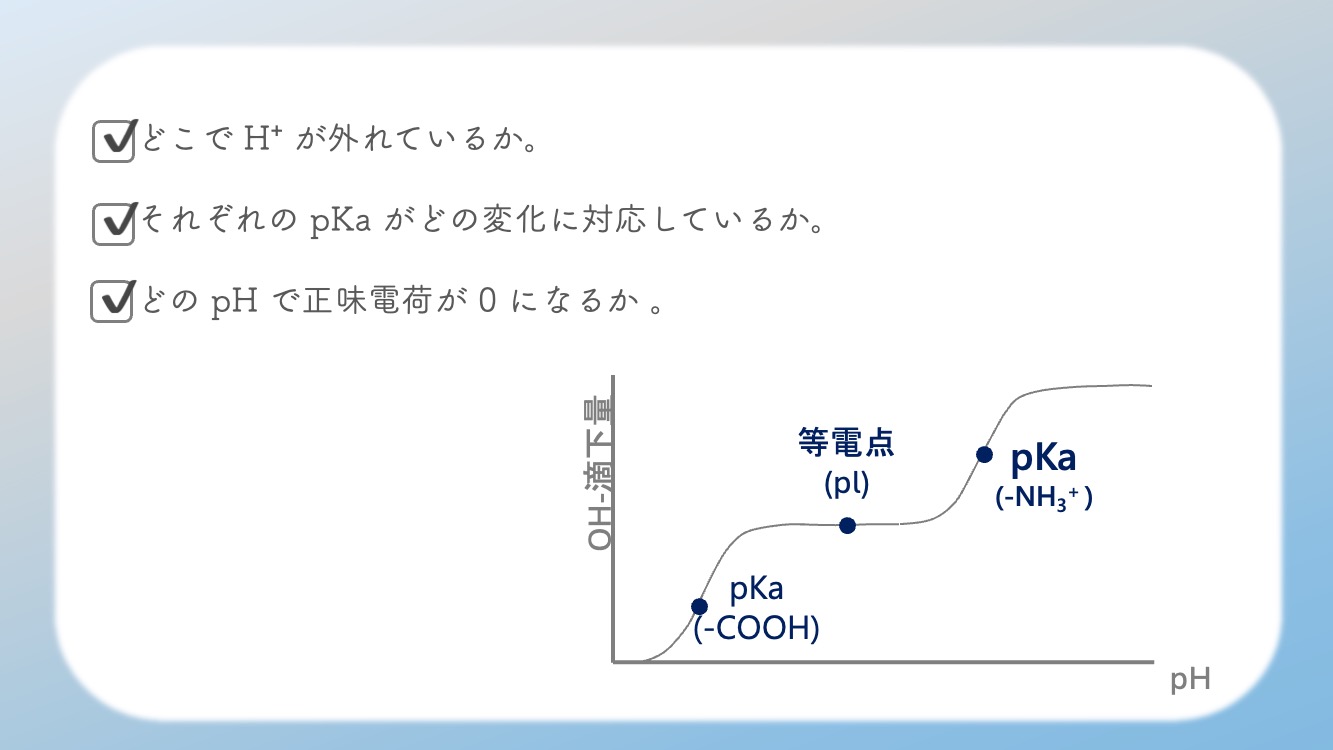
まず見るべきはこの3つだよ。
1つ目:どこで H⁺ が外れているか。
2つ目:それぞれの pKa がどの変化に対応しているか。
3つ目:どの pH で正味電荷が 0 になるか。

滴定曲線は「形」を覚えるのではなく
どの部位がいつ脱プロトン化するか
を追うことが、得点につながるんだ。
今日一緒に勉強したことで
その考え方が身についたよ。

10. ここだけ押さえれば大丈夫グリシン 滴定曲線の最短ルート▲ 目次へ

・低い pH では、H⁺ をたくさん持っている。
・最初に COOH から H⁺ が外れる。
・中間で 両性イオン(双性イオン)zwitterion になる。
・次に NH3⁺ から H⁺ が外れる。
・pKa は半分ずつの点。
・pI は net charge 0 の点。
こう並ぶと、流れがすごく見やすいね。

🐾 Dr.シロネコの応援メモ
使い終わった教科書📚はどうしていますか?医学書は価値が高いうちに整理するのが賢い方法です。次のステップへ進むための軍資金にするのも手ですよ。👍
11. 🍀ブログ特典 豆知識▲ 目次へ
等電点で、なぜタンパク質は集まりやすくなるの?

こはく。
アミノ酸と同じように
タンパク質にも等電点があるんだよ。


そう。
タンパク質の等電点
= たくさんのアミノ酸が集まった
全体の電荷が 0 になる pH
そして等電点の付近では
タンパク質が集まって沈殿しやすい。
等電点だと、どうして
タンパク質は集まりやすくなるの?


わかりやすく説明するね。
アミノ酸やタンパク質には、
プラスやマイナスの電荷があるよね。
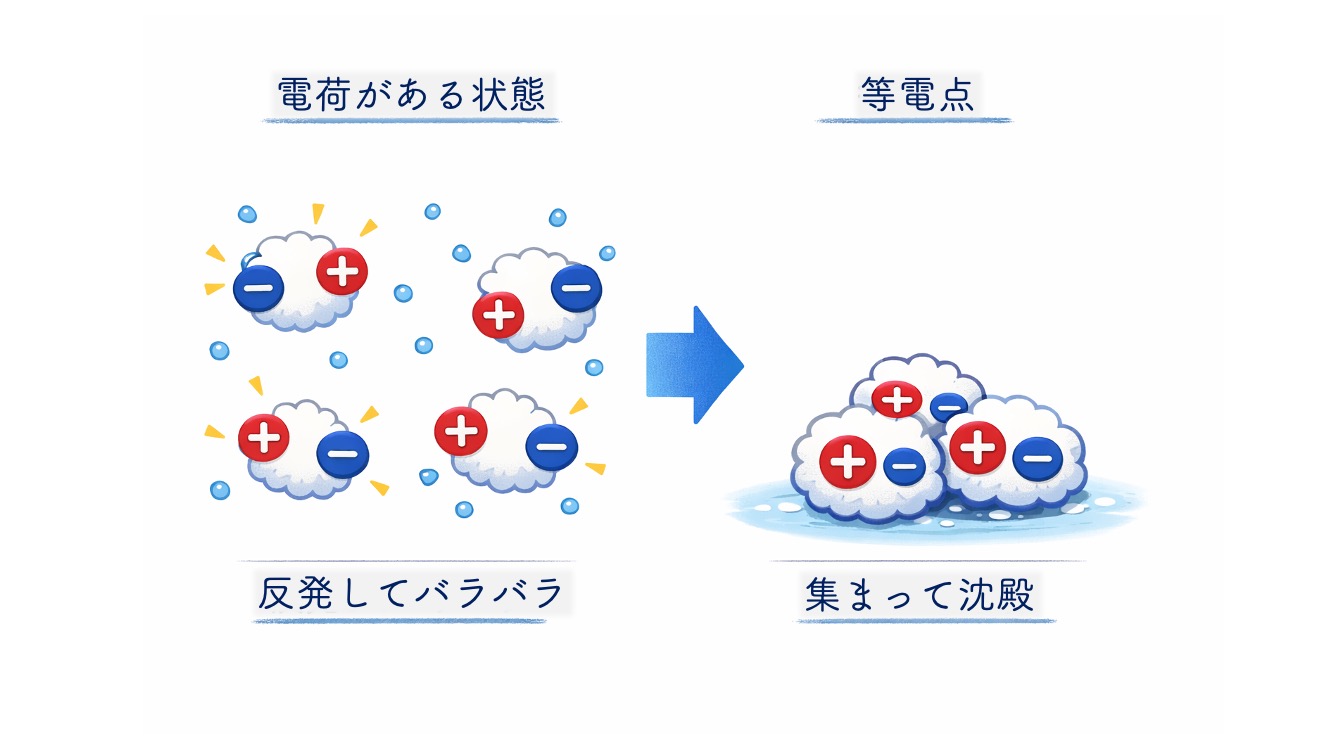
この電荷があるおかげで、
分子どうしは反発し合い、
水の中でも散らばって存在しやすいんだ。
反発し合う様に
分子同士が近づきすぎにくくなるんだね。


ところが、等電点では話が少し変わるよ。
等電点とは、
分子全体の正味電荷が 0 になる pH のことだったね。
このとき、分子全体としては
プラスでもマイナスでもなくなるため、
分子どうしの電気的な反発が小さくなるんだよ。


分子どうしが近づきやすくなるんだ。
その結果、
・水に溶けにくくなる。
・分子どうしが集まりやすくなる。
・沈殿しやすくなる。
ことがあるよ。
つまり、等電点では「ばらばらでいにくくなる」んだ。
だから、集まって沈みやすくなることがあるんだね。


これは、タンパク質を取り出したり、
分けたりするときの大事な考え方なんだ。
実験では、pH を等電点に近づけて
タンパク質を沈殿させる ことがあるよ。
参考文献/References
▲ 目次へ
① 世界的に有名な生化学の「三大教科書」
01
Lehninger Principles of Biochemistry
英語: Nelson DL, Cox MM. (2021). Lehninger Principles of Biochemistry, 8th Edition.
日本語: デービッド・ネルソン、マイケル・コックス(著)中山和久 他(監訳) (2023年). レ-ニンジャーの新生化学: 生化学と分子生物学の基本原理 (上)
今日のブログ記事に関する特徴: アミノ酸の滴定曲線について、なぜカルボキシ基がアミノ基より先に電離するのかを、近接する官能基の電子的な相互作用(静電的相互作用)から論理的に解説しています。
02
Biochemistry (Stryer)
英語: Berg JM, Tymoczko JL, Gatto Jr. GJ, Stryer L. (2019). Biochemistry, 9th Edition.
日本語: 入村達郎 他(監訳) (2021年). ストライヤー生化学 第10版.
今日のブログ記事に関する特徴: グリシンの pKa と生理学的意義を端的にまとめており、特にタンパク質の三次元構造を維持する上で、滴定曲線から導かれる電荷の状態がいかに重要であるかを強調しています。
03
Harper’s Illustrated Biochemistry
英語: Victor WR, Anthony PW, Peter JK, David AB. (2022). Harper’s Illustrated Biochemistry, 32nd Edition.
日本語: 上代淑人(監訳) (2023年). イラストレイテッド ハーパー・生化学 原書32版
今日のブログ記事に関する特徴: 医師国家試験などの基礎となる臨床的な視点が強く、血液の pH 緩衝能とアミノ酸の緩衝域の関係性を、図解(イラスト)を多用して実践的に解説しています。
② 初心者でも読みやすい・人気のテキスト 3選
01
Lippincott’s Illustrated Reviews: Biochemistry
英語: Abali EE, Cline SD, Franklin DS, Viselli SM. (2021). Lippincott Illustrated Reviews: Biochemistry, 8th Edition.
日本語: 石崎泰樹 他(監訳) (2022年). リッピンコット イラストレイテッド 生化学 原書8版.
今日のブログ記事に関する特徴: 非常に精巧な「コンセプト図」が特徴です。滴定曲線の各ステップでアミノ酸がどのような形(構造)をしているかが一目でわかるよう色分けされており、視覚的な学習に最適です。
02
はじめの一歩の生化学・分子生物学
石浦章一(著) (2013年). はじめの一歩の生化学・分子生物学 第3版.
今日のブログ記事に関する特徴: 「なぜ pH が変わると形が変わるのか?」という初学者の素朴な疑問に対し、数式を極力減らして日本語のストーリーで丁寧に解説しており、今回のブログの解説スタイルと非常によく合致しています。
03
マンガでわかる生化学
武蔵野公嗣(著) (2005年).
今日のブログ記事に関する特徴: 抽象的な pKa や等電点といった概念を、キャラクター同士の掛け合いや視覚的なメタファーで表現しています。「滴定曲線は単なる線ではなく物語である」という理解を助ける一冊です。






