13.【完全版】電子配置KLMNとspdfを最短で攻略!

▲ 目次へ
本ブログ『はじめての生化学』の内容は、医師・医学博士(MD/PhD)である筆者が、医学生、薬学生、看護学生、管理栄養士養成課程など、医療・健康科学を志す方々の国家試験対策および学術的教育を目的として執筆したものです。読者の皆様の安全と、正しい科学リテラシーを守るため、以下の事項を必ずお読みいただき、遵守してください。
正しい医学リテラシーを持って、科学の探求をお楽しみください。
【完全版】電子配置は「ホテルの部屋割り」で一発解決!KLMNとspdfを攻略
※本記事にはアフィリエイトリンクが含まれる可能性があります。
丸暗記を卒業し、薬理や代謝を「論理」で支配する。その本質である電子の動きを掴むことが、
あなたを市場価値の高い専門家へと押し上げます。
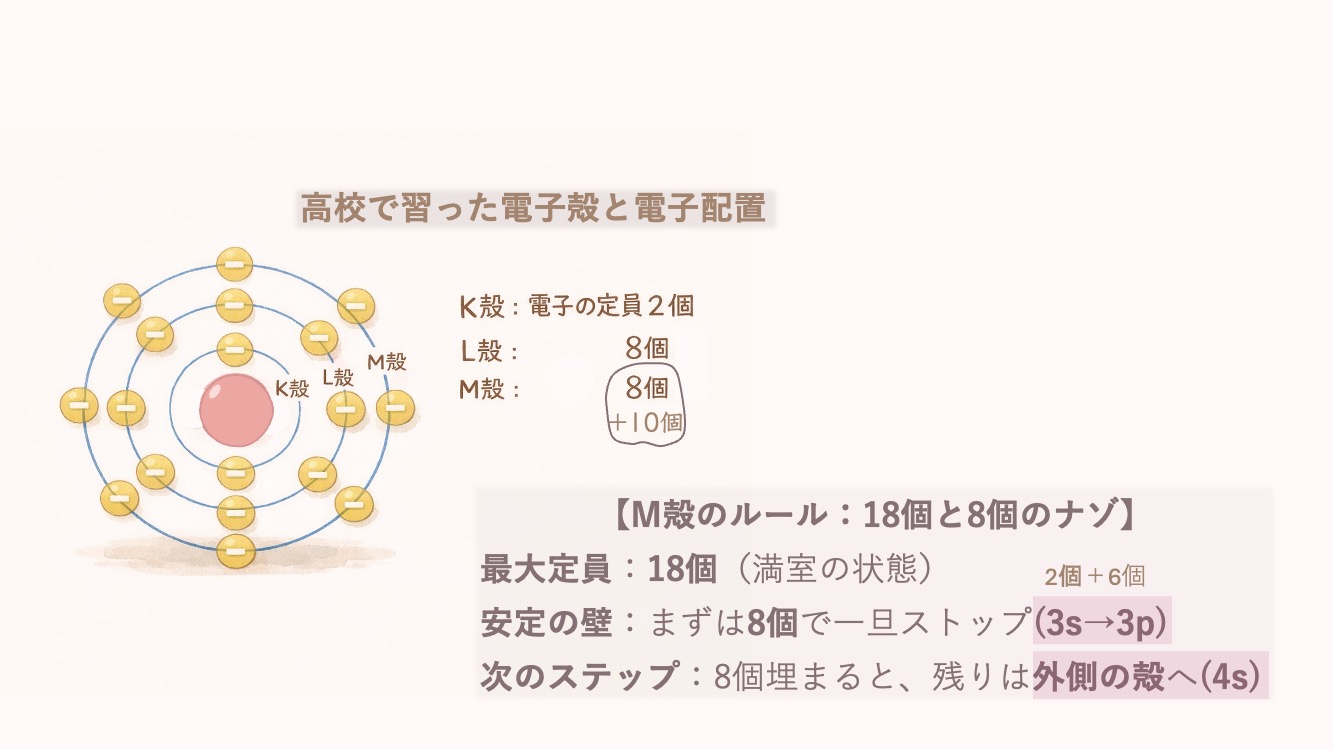
「高校では K殻(2個)・L殻(8個) と習ったのに、
大学では急に spd とか出てくる……。」
「電子配置が複雑で、これ以上丸暗記するのは限界…」
と悩んでしまうのは、あなただけではありません。
実は、私もかつて全く同じようにそのギャップを目の当たりにし、
まずは「さて、どうやって捉えようか?」と考えました。
そして丁寧に図を書きながら、整理しました。
この分野はやはり”自分で手を動かす”ことが大事かとおもいます。
今日は私が実際どうやってこのつながりを
整理したのかご紹介します。
「何から進めていけば良いかわからない…」
「このまま暗記し続けて本当に理解できるか不安…」
やみくもに進めて迷わないための鍵は、
「ホテルの部屋割り🏨」で全体像を把握することです。
すっきり整理して、解説しますね。
📚 目次
1. ホテルの「階数」:主殻(KLMN)
▲目次へ
原子は、中心にある**「原子核」と、そのまわりを回る「電子」というパーツで構成されています。 たとえるなら、原子核が「太陽」で、電子がそのまわりを公転する「惑星」**のような関係です。
もう少しくわしくみていこう。
電子が回る輪を主殻(しゅかく)と呼びます。
これは高校で習った「K殻・L殻・M殻……」のことですね。
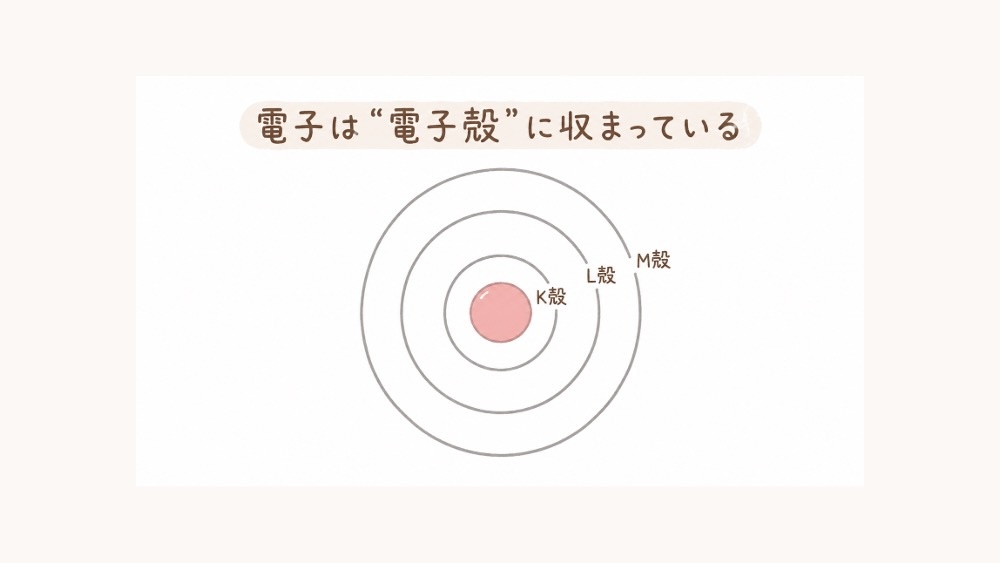
こんなふうに、原子核に近い内側から順に名前が決まっています。
これをホテルの「1階、2階……」という階数に見立てて考えてみよう。
上の階に登るにつれ、お部屋の数が増えていますね。
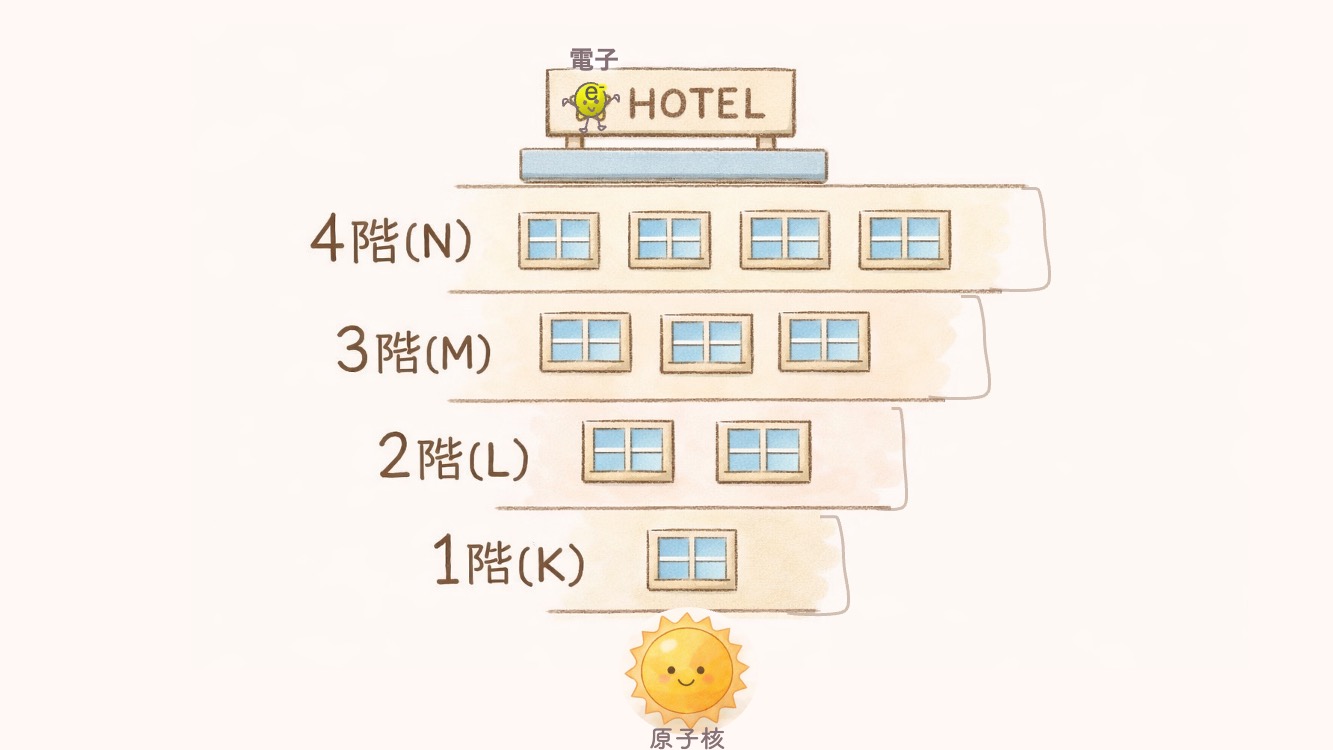
なるほど…どうしてAからじゃないの?



| 主殻(階数) | 番号 (n) | 電子の最大定員 (2n²)個 |
|---|---|---|
| K殻 | 1 | 2 × 1² = 2個 |
| L殻 | 2 | 2 × 2² = 8個 |
| M殻 | 3 | 2 × 3² = 18個 |
| N殻 | 4 | 2 × 4² = 32個 |
上の階に登るほど、部屋が増えて、電子がたくさん入るんだね。
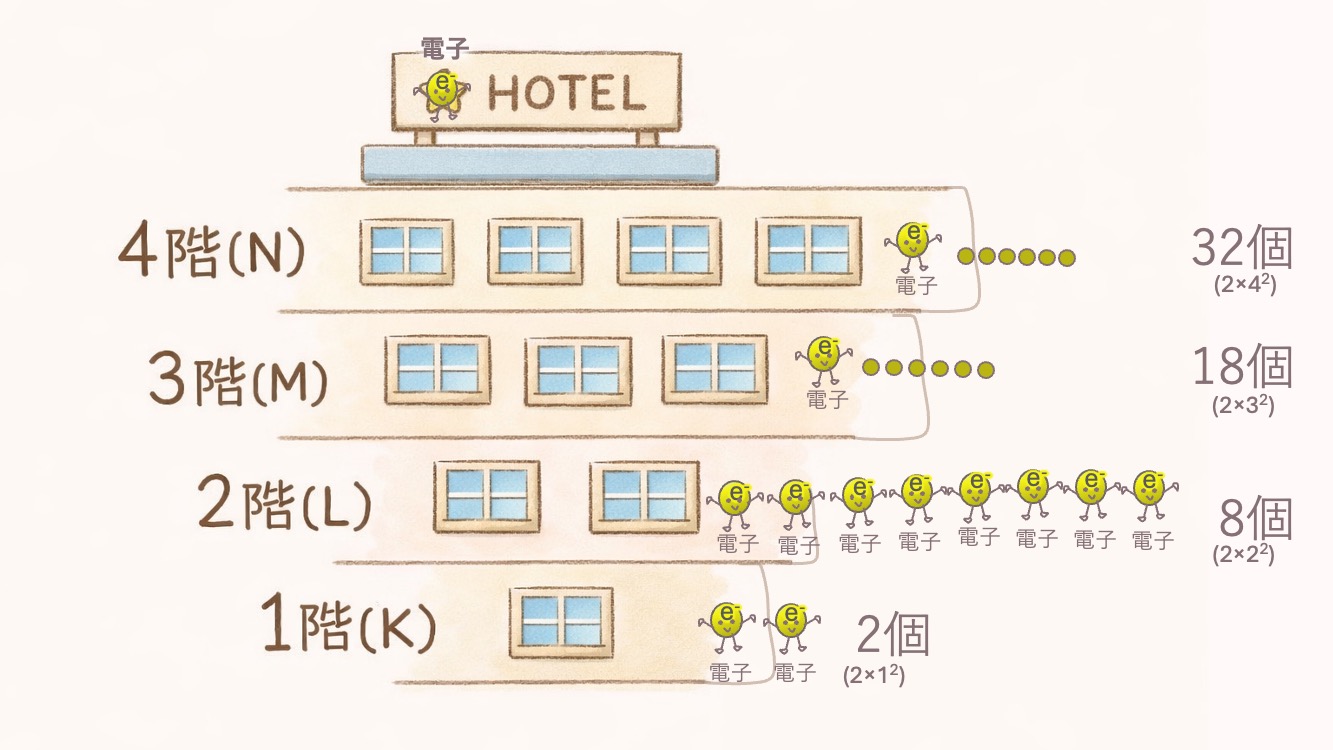
2. 副殻(spdf):部屋のタイプ
▲目次へ
大学ではもうちょっとだけ詳しく習うよ。
実は主殻は、エネルギー状態⚡️がわずかに異なる 副殻(方位量子数) から
構成されているのです。
簡単に言うとこれは、それぞれの階にある「シングルルーム(s)」「ツインルーム(p)」といった部屋のタイプのようなものです。
各階(K,L,M,N,..)を構成する部屋=s,p,d,f,…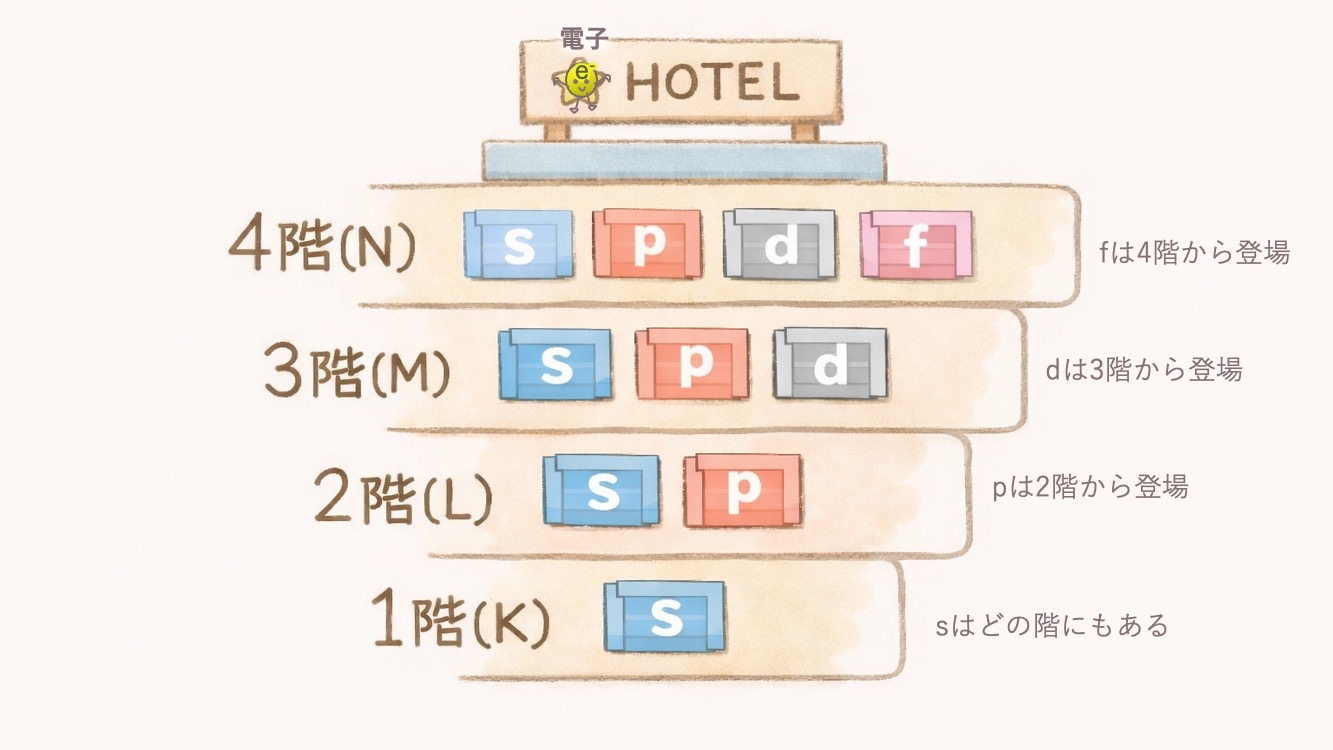
・1階(K殻)は部屋タイプs(s軌道)だけ。
・2階(L殻)には、部屋タイプs(s軌道)とp(p軌道)があります。
・3階(M殻)には、部屋タイプs(s軌道)・p(p軌道)・d(d軌道)があります。
・4階(N軌道)には、部屋タイプs(s軌道)・p(p軌道)・d(d軌道)・f(f軌道)が
あります。
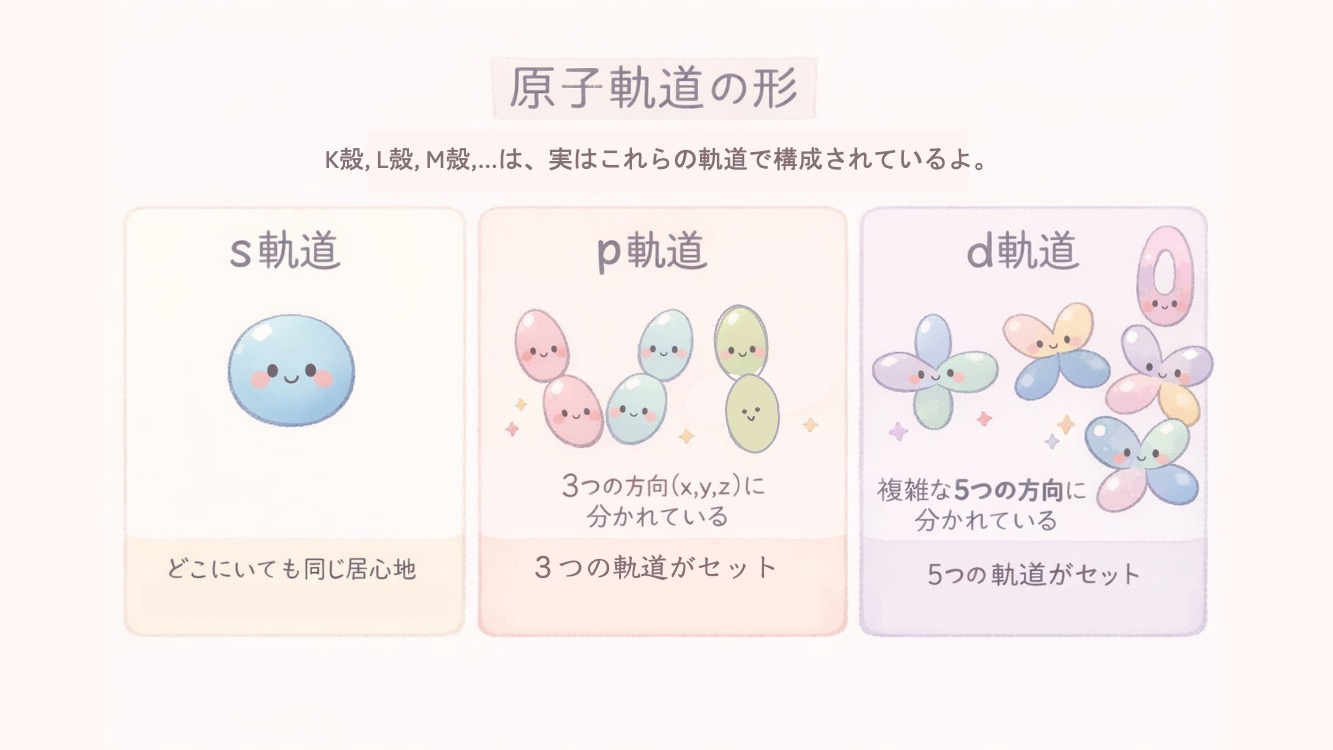
それぞれの部屋(軌道)は、形が違ったり、”3部屋で1セット”など、特徴があるよ。
- •
s軌道:球状の部屋。どの主殻(階)にも必ず1つある。 - •p軌道:亜鈴(ダンベル)状の部屋。L殻から登場する。3方向(x, y, z)の軌道が1セットになっていて、このセット全体でp軌道と呼ばれる。
- •d軌道:さらに複雑な形。M殻から登場し、5つの軌道が1セット。
- •f軌道:非常に複雑。N殻から登場し、7つの軌道で1セット
3. 主殻と副殻の組み合わせ
▲目次へ
各主殻の中に、どの副殻がいくつ含まれているかは決まっています。
各殻で1s,2s,3s,…などと区別するよ。
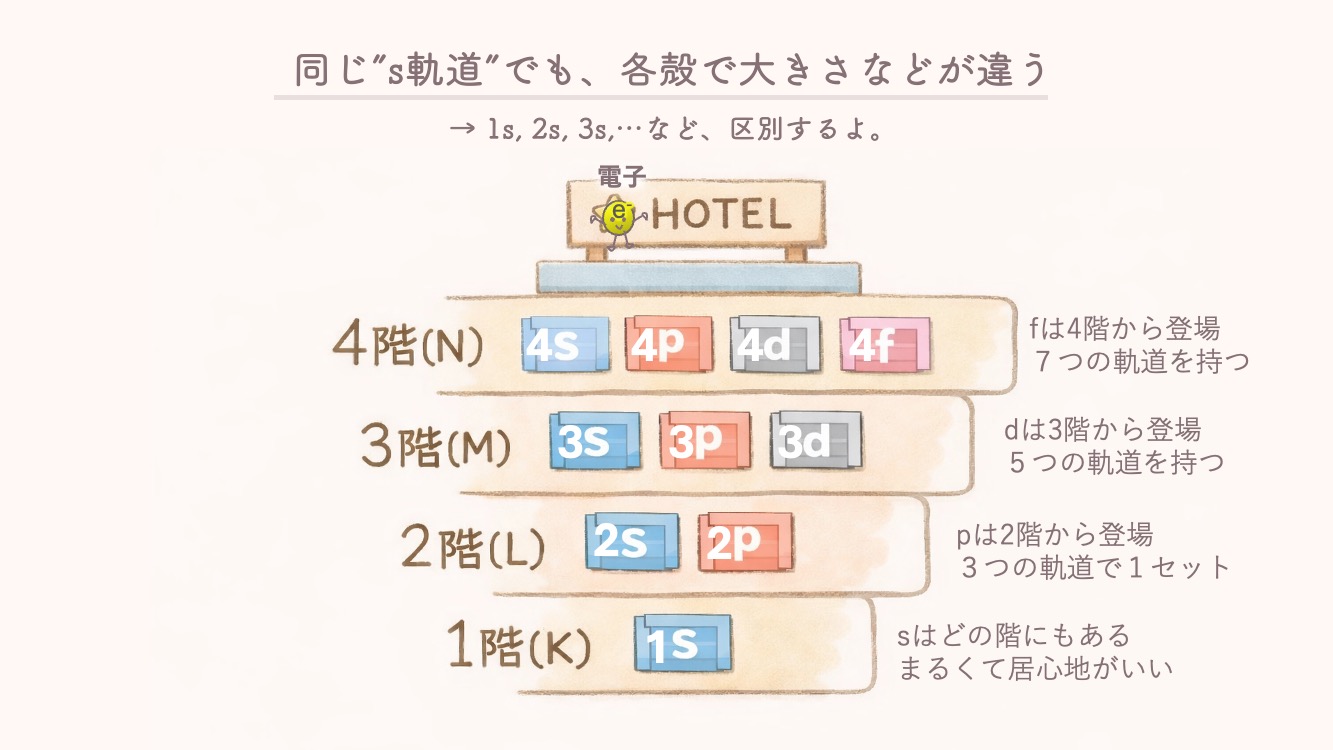
主殻の番号 n と同じ数だけ副殻の種類が存在します。
-
- •K殻 (1階:n=1→1種類の部屋):1s のみ
- •L殻(2階:n=2→2種類の部屋):2s, 2p
- •M殻 (3階:n=3→3種類の部屋):3s, 3p, 3d
- •N殻 (4階:n=4→4種類の部屋):4s, 4p, 4d, 4f
各軌道(部屋)は - 部屋タイプs(s軌道):1セット1部屋
- 部屋タイプp(p軌道):1セット3部屋
- 部屋タイプd(d軌道):1セット5部屋
- 部屋タイプf (f軌道):1セット7部屋
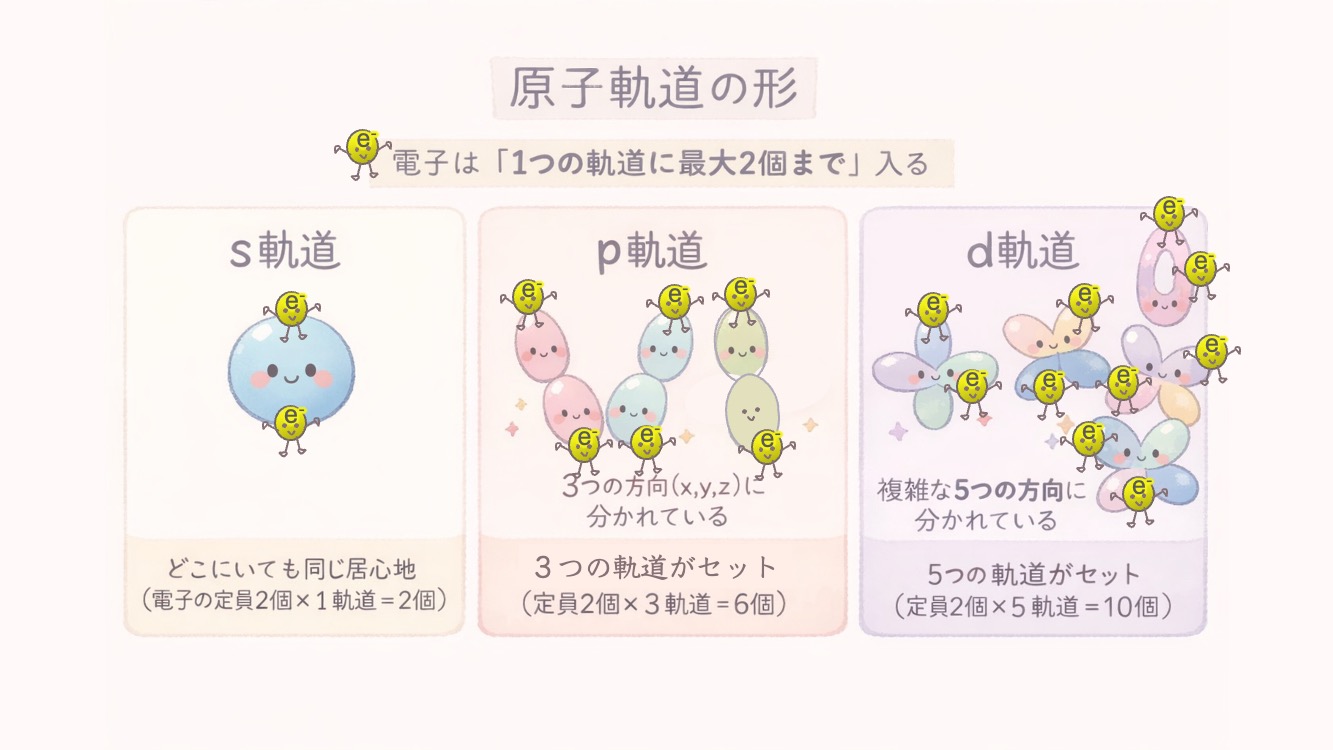
電子は1つの軌道に最大2個まで入るので
- •K殻 (n=1):1s のみ(合計1部屋 = 電子2個)
- •L殻 (n=2):2s, 2p(合計1+3=4部屋 = 電子8個)
- •M殻 (n=3):3s, 3p, 3d(合計1+3+5=9部屋 = 電子18個)
- •N殻 (n=4):4s, 4p, 4d, 4f(合計1+3+5+7=16部屋 = 電子32個)

ここまでのことを
クイズで遊びながら、楽しくおぼえよう😆✨
【ここまでを覚えよう】電子配置・副殻構造クイズ
4. 電子が入る順番(エネルギーの逆転)
▲目次へ
次に、電子が部屋を埋める順番を説明するね。
電子は基本的に「エネルギーの低い(安定した)部屋」から順に埋まっていきます。
やっぱり電子も落ち着いてリラックスしたいのです。😌
ここで重要なのが、「内側の殻がすべて埋まってから外側へ」とは限らない という点です。
1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p …

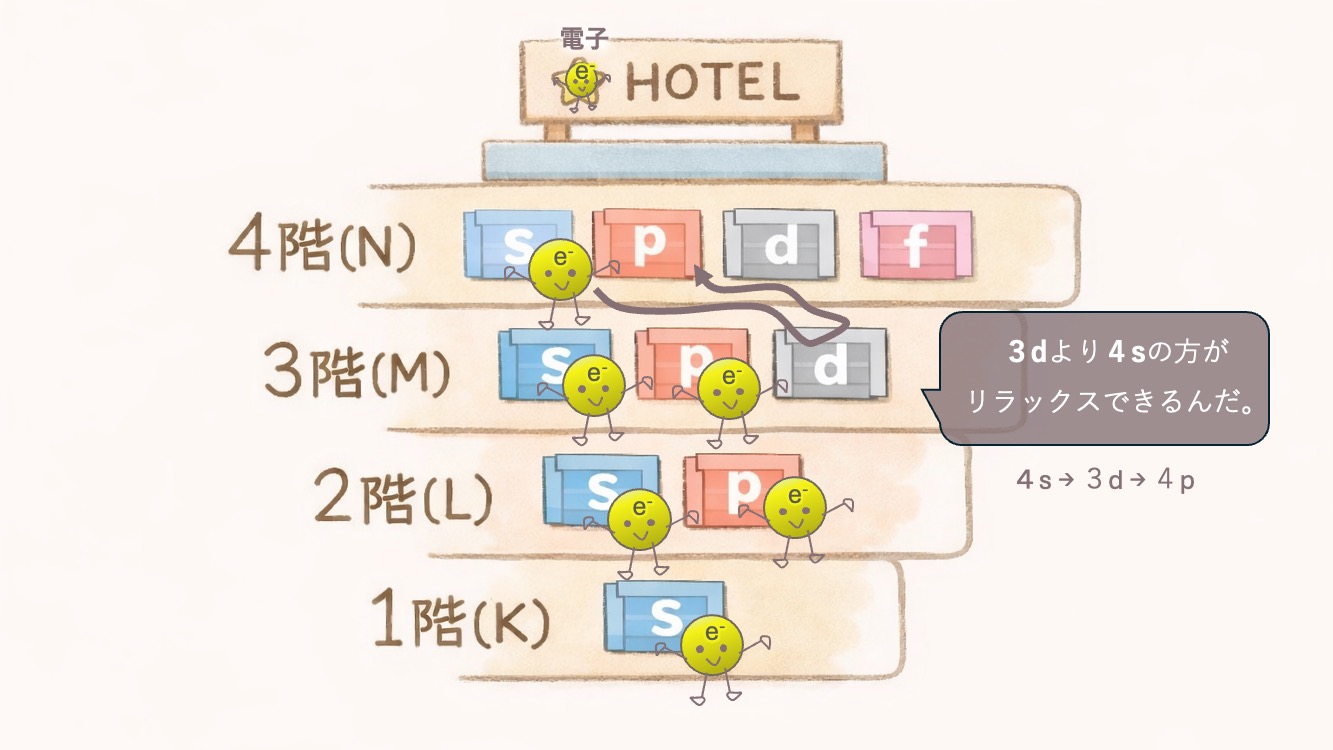
これで”M殻のルール”のなぞが解けたね。
5. Dr.しろねこのまとめ
▲目次へ
このように「入れ物(殻)」と「中身(軌道)」を分けて考えると、複雑な電子配置もパズルのように整理しやすくなります。
丸暗記を卒業して、化学の「意味とつながり」を楽しんでいこう!この記事が役に立ったと思ったら、ぜひブックマークして復習に使ってね。
🍀 特典:確認クイズ10題
▲目次へ
参考文献/ References
▲目次へ
💡 Dr.しろねこからのアドバイス
・もっと厳密な図解や数式で納得したい人→『アトキンス物理化学』
・この知識がどう生命現象に繋がるかワクワクしたい人→『キャンベル生物学』
チェックしてみてね!
1. Atkins’ Physical Chemistry
- 英語: Peter Atkins, Julio de Paula, and James Keeler (2022). Atkins’ Physical Chemistry (12th ed.). Oxford University Press.
- 日本語: ピーター・アトキンス、ジュリオ・デ・パウラ、ジェームス・キーラー 著、中野 幸夫 他 訳(2023年 第12版)『アトキンス物理化学(上・下)』東京化学同人
- 紹介: 「電子配置の数理的な美しさを知るならこれ」
「なぜK殻から始まるのか」という歴史的背景から、軌道の形が導き出される物理的根拠までを網羅。エネルギーの逆転現象を厳密に解説してます(面白いです)。ブログの「なぜ?」を深く解決してくれます。
2. Shriver & Atkins’ Inorganic Chemistry
- 英語: Mark Weller, Fraser Armstrong, Jonathan Rourke, and Tina Overton (2018). Inorganic Chemistry (7th ed.). Oxford University Press.
- 日本語: M. Weller, F. Armstrong 他 著、田中 勝久 他 訳(2021年 第7版)『シュライバー・アトキンス無機化学(上・下)』東京化学同人
- 紹介: 「spdfの個性を極めるならこれ」
「spdf」の由来や、複雑な軌道の形が元素の性質にどう影響するかを詳述。4sが先に埋まるルールが周期表の形をいかに決定づけているかを論理的に理解できる、無機化学のに定評のあるテキストです。
3. Campbell Biology
- 英語: Lisa A. Urry, Michael L. Cain, Steven A. Wasserman, Peter V. Minorsky, and Rebecca Orr (2020). Campbell Biology (12th ed.). Pearson.
- 日本語: 池内 昌彦、伊藤 元己 他 監訳(2023年刊行)『キャンベル生物学 原著11版』丸善出版
- 紹介: 「化学を生物学の言葉で解釈するならこれ」
電子配置の知識が、生命を形作る分子の形にどう繋がるのかを、壮大なストーリーで解説してくれます。「なぜ医療系大学で学ぶ自分が、化学を学ぶ必要があるの?」という迷いや焦りに、医療・生命科学の視点から答えをくれるバイブルです。






