18. アミノ酸の分類を理屈で解く。電気陰性度の『0.5の境界線』から見える水溶性と疎水性の正体

【CBT・国家試験対策】
アミノ酸分類の迷いを断つ!水和と極性のメカニズムを完全図解
※本記事にはアフィリエイトリンクが含まれる可能性があります。
丸暗記を卒業し、薬理や代謝を「論理」で支配する。
その本質である電子の動きを掴むことが、
あなたを市場価値の高い専門家へと押し上げます。
1. アミノ酸の性格を支配するたった1つの物理法則
▲目次へ
なぜ、あるアミノ酸は水に溶け、あるものは油のように弾くのか。
「水に溶ける=イオン化」だと思っていませんか?
アミノ酸の運命を分けるのは、電離ではなくたった0.4の「電気陰性度」の差。
原子たちの電子争奪戦、その勝敗がタンパク質の形を決めています。
📚 目次:アミノ酸の性質と電気陰性度を完全マスター!
2. 電気陰性度とは? : 分子の中で起きている「電子の強奪戦」
▲目次へ
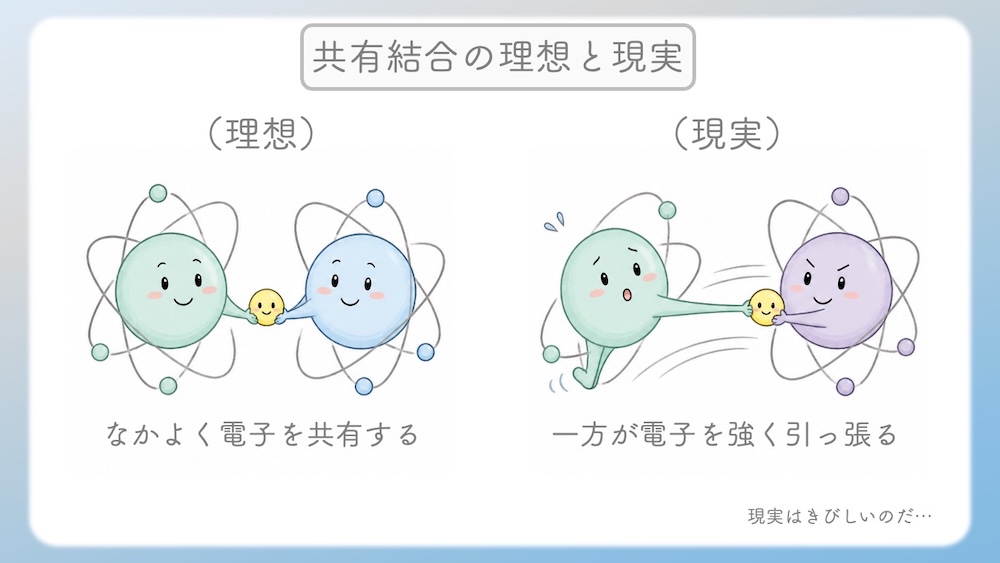


その「電子を欲しがる強さ」の違いが、アミノ酸の運命を左右するんだよ。
電気陰性度とは、電子を引き寄せる力を意味します。
原子同士が結合(共有結合)するとき、そこには必ず「電子の奪い合い」が発生します。
- ● 理想(平等な共有)
本来、共有結合は2つの原子が電子を出し合い、平等に分け合うはずのものです。しかし、現実には「平等」なケースは稀です。 - ● 現実(不平等な共有)
原子には、電子を欲しがる強さに個性があります。一方が電子を強引に自分の方へ引き寄せ、もう一方が引きずられている。これが分子の中で起きている日常です。
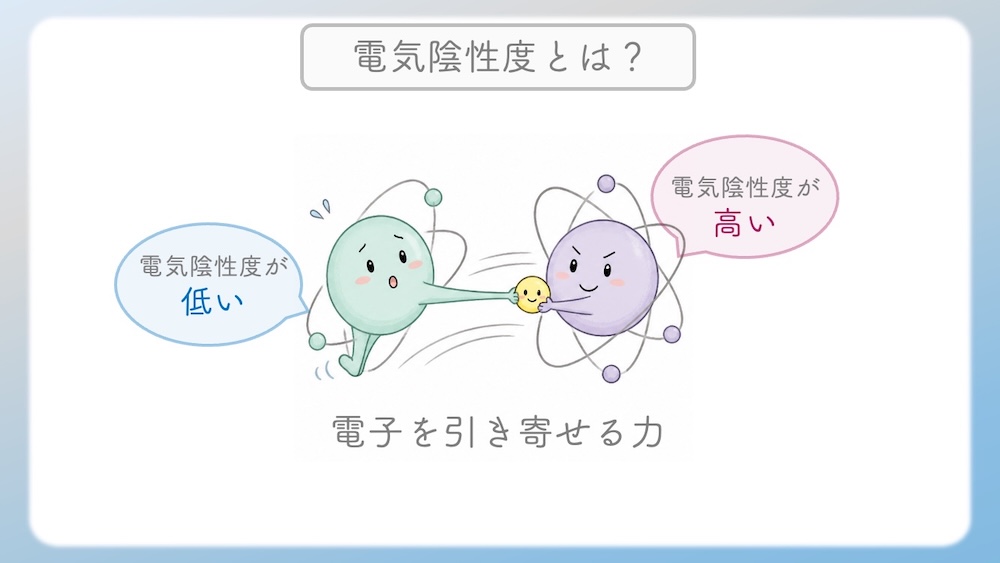
電気陰性度の定義
この「共有している電子を自分の方へグイグイ引き寄せる強さ」を数値化したものが電気陰性度です。
3. 【秒で覚える】最強のFON(フォン)と骨格のCH(炭水):数値より大事な力関係の「階段」
▲目次へ
電子を引き寄せる力は原子ごとに違います。
しかし、試験対策として全ての数値を暗記する必要はありません。
アミノ酸の性質を理解する上で、まず「原子界には絶対的な力関係(カースト)がある」という大前提を押さえてください。この力の差が、実際の分子の中で「電子の奪い合い」を引き起こします。


「最強のFON」と「骨格のCH」という呪文を使えば、一瞬で力関係が整理できるよ。
医療系の基礎として欠かせない5人のメンバーと、その「戦闘力(数値)」を見てみましょう。
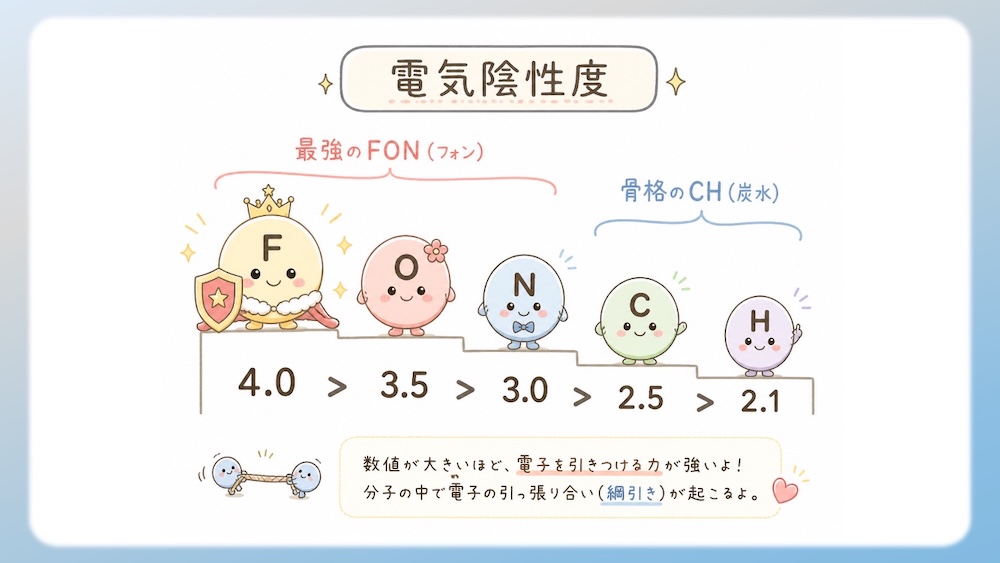
- F(フッ素):4.0
- O(酸素):3.5
- N(窒素):3.0
- C(炭素):2.5
- H(水素):2.1
ここで大切なのは数値そのものよりも、
「誰が誰より強いのか」という順番と
「どれくらいの差があるか」という距離感です。
効率的な覚え方
この5人は、以下のセットで覚えると一瞬で引き出せます。
覚え方: 最強の FON(フォン) と、骨格の CH(炭水)!
最強の王者 F がトップ。そこから O・N・C までは、綺麗な階段状に 「0.5ずつ」 戦闘力が下がっていくのがわかりますね。
この3.5や3.0という高い数値を持つ原子が、弱気な H(2.1) と結合すると、電子を容赦なく自分のほうへ引き寄せます。
一方で、骨格を作る C(2.5)と H(2.1)の差は、わずか「0.4」 しかありません。この数値の近さが、電子の奪い合いが起きない「平和な結合(非極性)」を生み出します。
【復習】アミノ酸の運命を握る「5人の序列」クイズ
4. 周期表と強さの関係(なぜ右上が強いの?):物理が苦手でもスッとわかる陽子と距離の法則
▲目次へ
F > O > N > C > H
この序列には、魔法のような偶然ではなく、シンプルな物理のルールがあります。物理を履修していなくても大丈夫。
“引っ張り合うとは?”と気楽にイメージすれば一瞬で理解できるよ。


理由はシンプル。「磁石の強さ」と「距離」、この2つだけで決まっているんだよ。
まずは、電子を”引き寄せる力”について考えましょう。
マイナスの電子を引っ張るのは、原子の中心にあるプラスの力、すなわち「陽子」です。この電子を引っ張る力が強くなるのは、たったの2つの場合だけです。
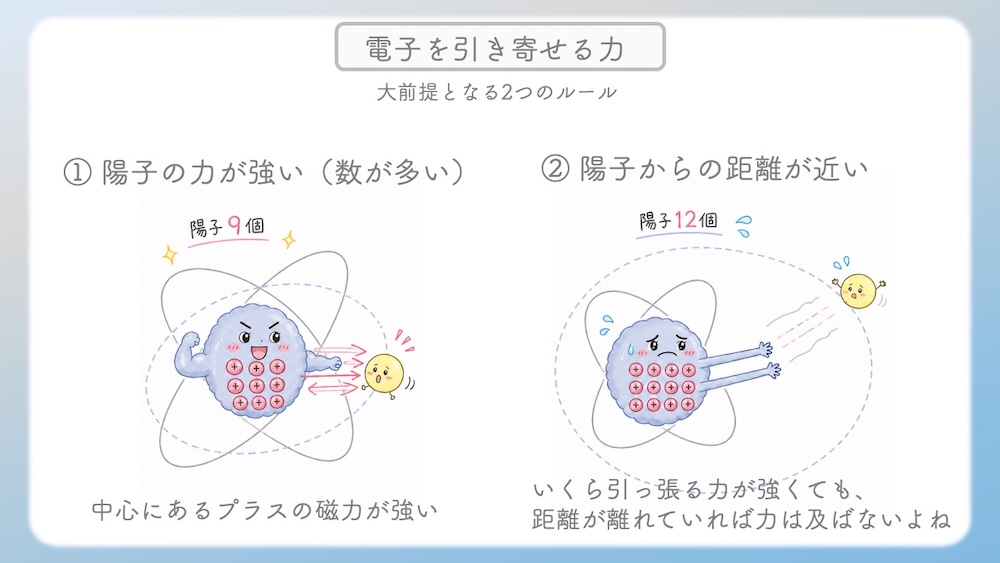
大前提となる2つのルール
① 陽子の力が強い(数が多い)
中心にあるプラスの磁力が強ければ、当然、外を回る電子を引く力も強くなります。つまり、「陽子の数が多いほど、引っ張るパワーが強い」ということです。
② 陽子からの距離が近い
磁石と同じで、「中心に近いほど、力はダイレクトに伝わる」のです。いくら引っ張る力が強くても、距離が離れていれば力は及びません。
周期表で「右上」が最強になる理由
● 右に行くほど強くなる(陽子の数が増える)
周期表を「右」に進むほど、原子核の中にある陽子の数が増えていきます。これによって、電子を自分のほうへ引き寄せる「磁石としてのパワー」が強まります。
● 上に行くほど強くなる(距離が近くなる)
周期表の「上」にいる原子ほど、電子軌道の数が少なく、中心に近くなります。だからこそ、陽子の力が弱まることなく電子をガッチリ掴めるのです。
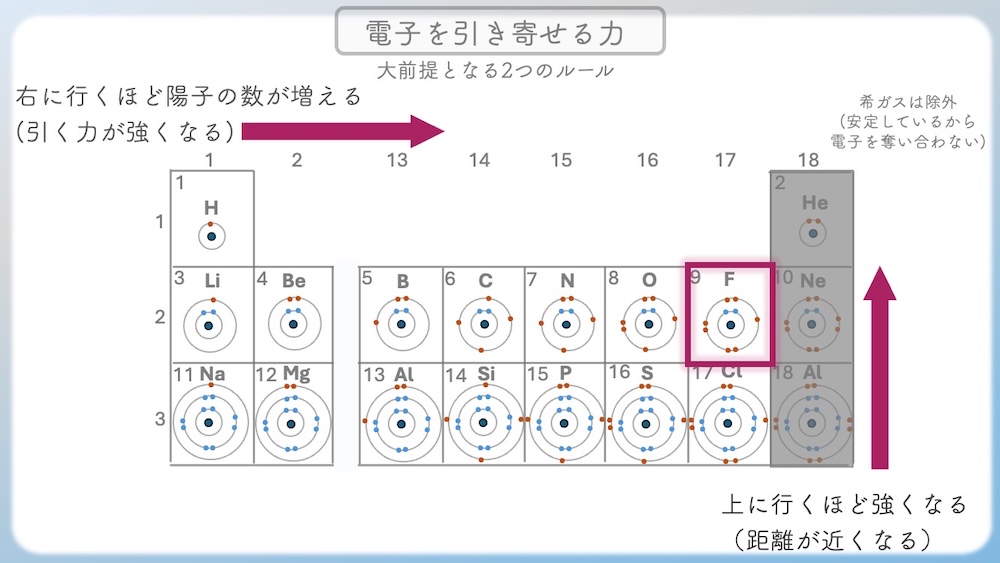
結論:最強のハンターは「右上」にいる!
この2つの条件をどちらも満たしているのが、周期表の右上エリア(F・O・N)です。
- 右にあるから、中心のパワー(陽子)が強い。
- 上にあるから、距離が近くて力がよく届く。
「右上ほど電子を奪い取るハンターになる」と分かれば、構造式を見たときに「酸素(O)が隣の水素(H)から電子を奪って、極性を作っているな!」と、暗記に頼らず見抜けるようになります。
第二章:9割が誤解している「水に溶ける」の真実
5. 水の極性:H₂O が「万能の溶媒」と呼ばれる理由(電気双極子)
▲目次へ
「水に溶けるって、具体的に何がおきているの?」
普段はあまり考えもしない、当たり前のこと。
でも知識の差が大きくその解答を左右します。
あなたならどう答えますか?
この章では先ほど学んだ「電気陰性度」の差が、
実際の水分子にどのような影響を与えているのかを紐解いていきましょう。
電子の引き寄せが生む「電荷の偏り」
水分子(H₂O)の中では、酸素(O)と水素(H)の間で電子の引き寄せ合いが起きています。数値を比較すると、その差は一目瞭然です。
酸素 (O):3.5
水素 (H):2.1
このパワーバランスの結果、共有されている電子はグイッと酸素側へ引き寄せられます。
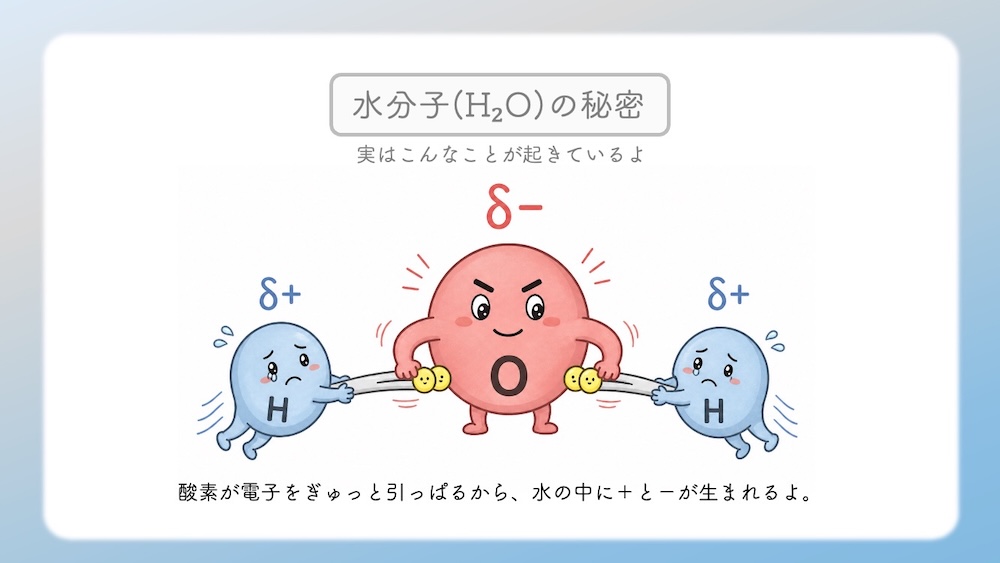
● 酸素側: マイナスの電気を持つ電子が集まるため、少しだけマイナスを帯びる
● 水素側: 電子を奪われる形になるため、少しだけプラスを帯びる


この偏りを「極性」と呼ぶんだ。水分子は、いわば「プラスとマイナスを持つ小さなユニット」として振る舞っているんだよ。
「電気の偏り」が水分子に個性を与える
水分子は一つの分子でありながら、分子内で電気の分布に『偏り』があり、プラスっぽい部分とマイナスっぽい部分をあわせ持っています。
この性質こそが、多くのアミノ酸や物質を”溶かす”ことができる「万能の溶媒」としての力の源になっています。
水がただの液体ではなく、目印(電気の偏り)を持っていることを理解すると、この後の「水に溶ける💦」という現象の仕組みが驚くほどスムーズに繋がっていきます。
6. 【よくある勘違い】:水はバラバラにならない!H⁺ と OH⁻ にまつわる致命的な勘違い
▲目次へ
「水に溶けるって、具体的に何がおきているの?」
ここで多くの人が誤解しているポイントを正しましょう💯
ほとんどの水は H₂O の形のまま、バラバラにならずに「電気的偏りをもつ分子」として振る舞っています。
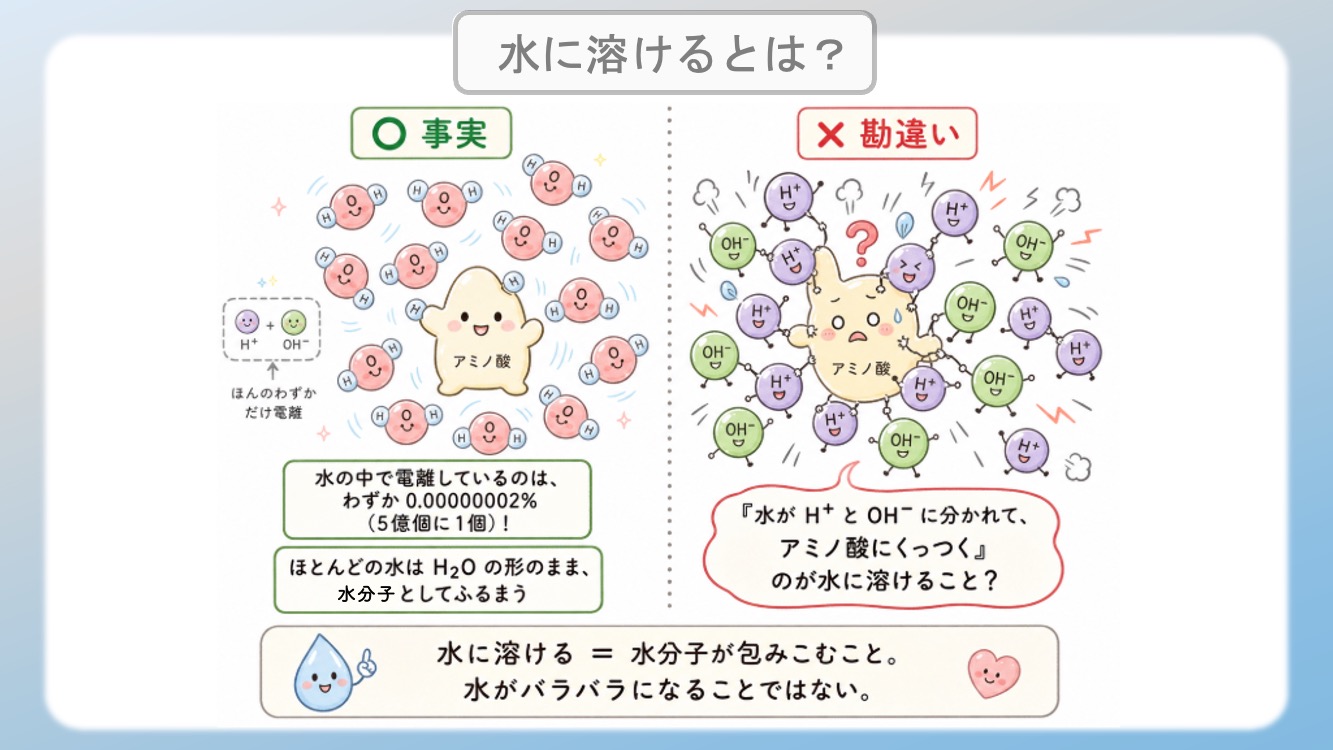
じゃあ、残りの 4億9999万9999個は H₂O のまま、くっついてるってこと?


鋭いね!その通り。
「水に溶ける」を考えるときに、最初からイオンに分けて考えちゃうと、この後の「親水性・疎水性」の本質が見えなくなるんだ。
まずは「水は、形を保った分子」であることを脳に焼き付けておこう。
水分子はバラバラにならずに「H₂O」のまま仕事をする!
7. 水に溶けるとは?:水分子が H₂O の形のままアミノ酸を包囲する動態
▲目次へ
では、本当の意味で「水に溶ける」とはどういう状態でしょうか?
それは、水分子たちが「H₂O の形のまま、相手を包み込んで、孤独にさせる」ことです。
アミノ酸は「壊れる」のではなく「孤立」する
アミノ酸の粉末が水に溶けるとき、粉末の状態ではアミノ酸同士が寄り添って固まっています。ここに水分子がやってくると、アミノ酸を一つずつ引き剥がしていきます。
1. アミノ酸のプラスの部分には…
水のマイナス(O)側が引き寄せられて群がります。
2. アミノ酸のマイナスの部分には…
水のプラス(H)側がくるりと向きを変えて群がります。
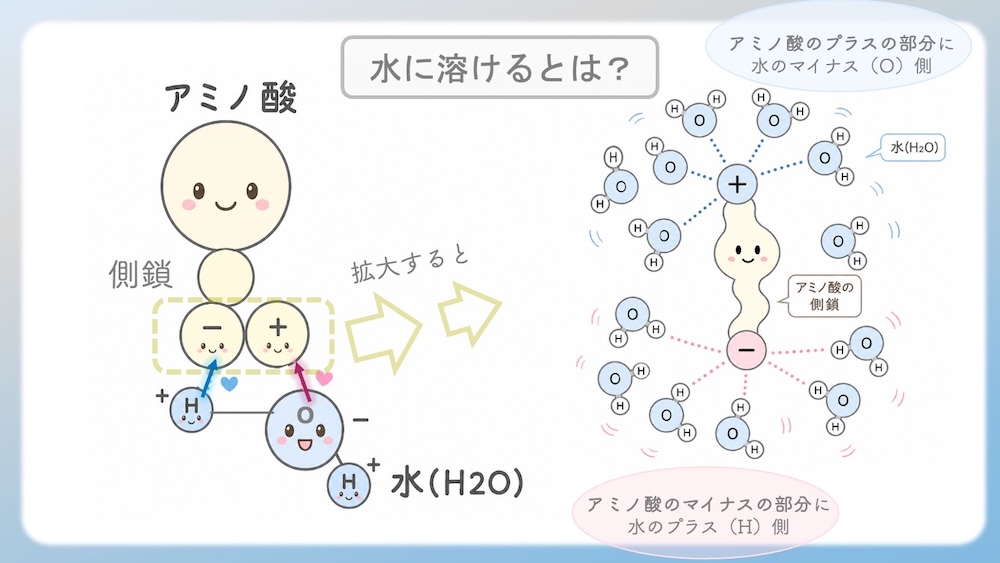


磁石のバリアで守られているから、もうアミノ酸同士で固まることができないんだ。
「水和」という名のバリア
このように、水分子がアミノ酸の周囲を隙間なく取り囲んだ状態を「水和」と言います。
水分子にぐるりと囲まれたアミノ酸は、もう他の仲間(アミノ酸)とくっつくことができなくなります。
水分子という「バリア」に包まれて、水の中を一人で自由に動き回れるようになった状態。これこそが、私たちが目にする「溶けて見えなくなった」状態の正体です。
8. 水溶性・疎水性の分かれ道: アミノ酸分類の「0.5の境界線」を見抜く極意
▲目次へ
これまで学んできた「電気陰性度」の知識が、ここで一気に繋がります。アミノ酸の側鎖(R基)を見て、それが水に溶けるのか、それとも油のように水を弾くのかを判断する決定的な基準を整理しましょう。
8-1. なぜ「側鎖(R基)」を見るだけで、アミノ酸の性格がわかるのか?
▲目次へ
アミノ酸には「どの構造も共通して持っている本体」と「種類によって形が違うパーツ(R基)」があります。本体部分はもともと水と仲が良い構造をしています。
つまり、そのアミノ酸が全体として水に溶けるかどうかは、唯一の「付け替えパーツ」であるR基が、水を呼ぶ力を持っているかどうかで決まるのです。このパーツの性格を見極めるのが、電気陰性度の差「0.5」という数字です。
8-2. 【親水性の正体】なぜセリンは、水分子に「エスコート」されるのか?
▲目次へ
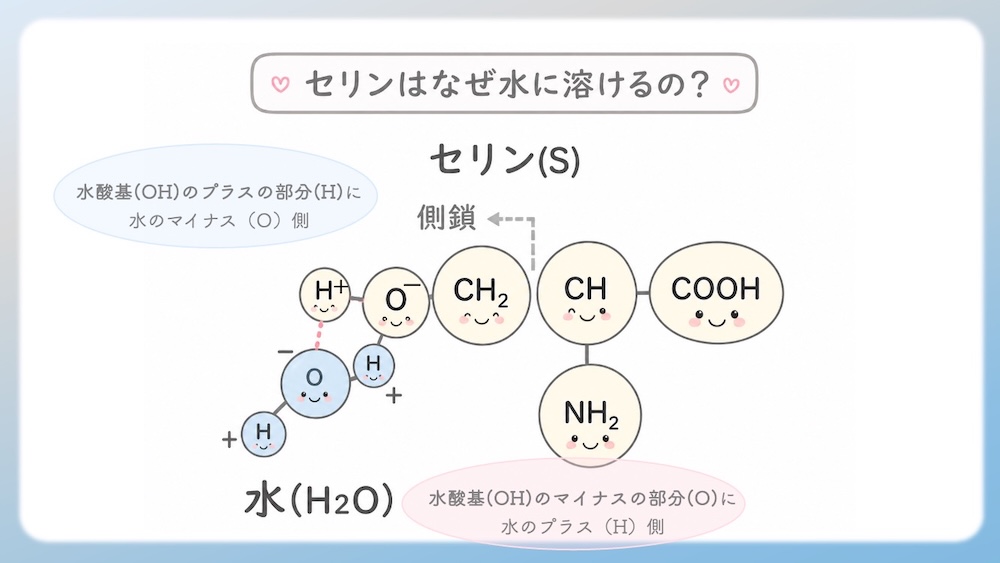
アミノ酸が水に溶けるとき、分子の内部では何が起きているのでしょうか。 セリンなどの「水溶性(親水性)」アミノ酸を例に、その仕組みを紐解いてみましょう。
1. 強力な「電気の目印」がある
セリンの側鎖にある O-H結合(ヒドロキシ基)に注目してください。
- 酸素(O):3.5
- 水素(H):2.1
- その差:1.4
この「1.4」という大きな数値の差によって、結合部分にははっきりとしたプラスとマイナスの電気の偏りが生まれます。水分子にとって、これは非常に見つけやすい「目印」となります。
2. 水分子が包囲する
この目印を見つけると、水分子たちは吸い寄せられていきます。
● マイナス側(O): 水分子の「プラス(H)側」が近寄る
● プラス側(H): 水分子の「マイナス(O)側」が近寄る
このように、水分子がセリンの -OH をぐるりと囲んでバリアを作る状態を「水和」と呼びます。水分子にエスコートされることで、セリンは水の中に安定して存在(溶解)できるのです。


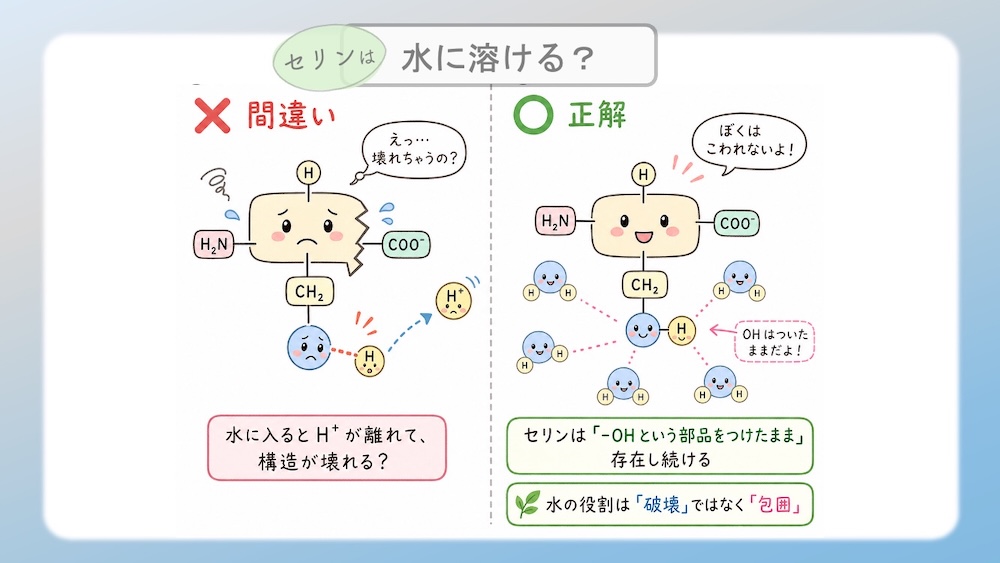
【重要】よくある勘違い:アミノ酸は「バラバラ」にならない
× 間違い: 水に入ると H+ が離れて、アミノ酸の構造が壊れる。
○ 正解: セリンは 「-OH という部品をつけたまま」 の形で存在し続ける。
水分子の役割は「破壊」ではなく「包囲」
水分子が行うのは、結合を壊すことではなく、あくまで「包み込む(エスコートする)」ことです。「部品(OH)が取れる」のではなく、「部品に水分子が群がっている」状態こそが、親水性の正しい理解です。
まとめ: セリンが水に溶けるのは、壊れるからではありません。
「強い目印(1.4の差)」を持っているおかげで、水分子というボディーガードに守られながら、水の中を自由に動き回れるようになるからなのです。
水酸基(OH)をもつアミノ酸は溶けやすい。と丸暗記するのも、もちろんいい。
試験の点数を確実にとることが最優先だとおもう。
でもその理由を理解すると、
あらゆる分子の見方がガラッとかわるよね。
今日のブログ記事が、難解な生化学の壁を壊し
あなたの視界を広げてくれたらうれしい。
8-3. 【疎水性の正体】なぜバリンは、水分子に「無視」されるのか?
▲目次へ
では反対に「水に溶けないって、具体的に何がおきているの?」
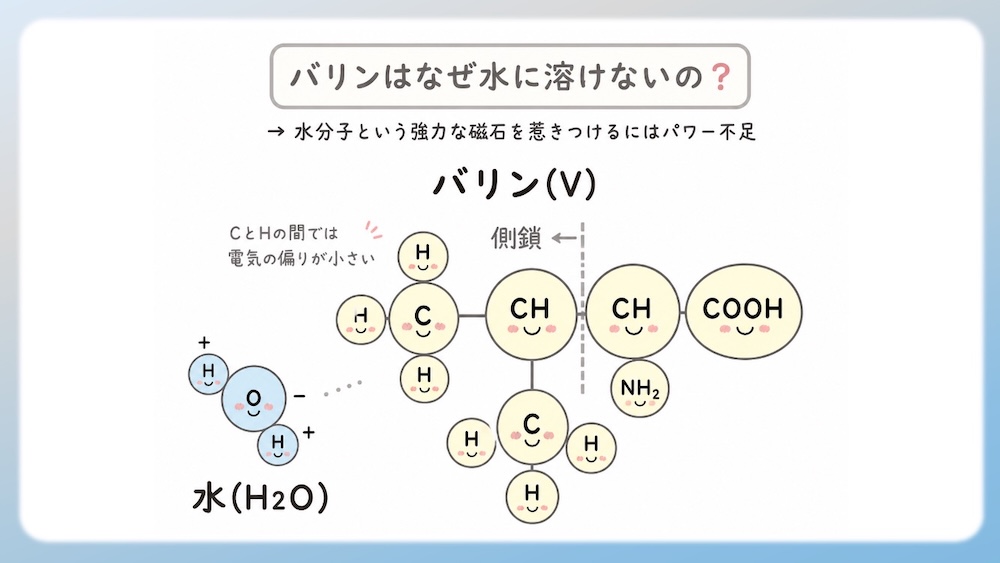
アミノ酸の中には、水と仲良くできるものだけでなく、頑なに水を寄せ付けない「疎水性」のグループがあります。代表格であるバリンを例に、水に溶けない仕組みを物理の視点で紐解いてみましょう。
1. なぜ「0.4」の差では水に溶けないのか?
原子同士の引き合う力(電気陰性度)に注目してみましょう。
- 炭素(C):2.5
- 水素(H):2.1
- その差:0.4
化学の世界では、この程度の偏りは「誤差」の範囲、つまり「非極性」とみなされます。これでは、水分子という強力な磁石を惹きつけるにはパワー不足なのです。
2. バリンの側鎖は「ツルツルの壁」
バリンの側鎖は、すべて炭素(C)と水素(H)だけで構成されています。どこを見ても「0.4」というわずかな引き寄せ合いしか起きていないため、水分子から見れば「どこにもくっつく場所がないツルツルの壁」のような状態です。
3. 水分子に「無視」された結果
強い磁力を持った仲間同士で集まりたがる水分子は、目印を持たないバリンを素通りします。その結果、バリンは「疎水性(水を弾く)アミノ酸」に分類されることになるのです。


その通り。一般的には「0.5以上の差」がないと、水分子を惹きつける「取っ手」になれないといわれているよ。
バリンの側鎖は、水にとっては掴みどころのない壁なんだよ。
まとめ: バリンが水に溶けないのは、側鎖が「CとH」だけでできており、その力の差が「0.4」という水分子を惹きつけるには小さすぎる数値だから!
8-4. 水分子の心理:彼らが「自分と同じくらい強い個性」を好む理由
▲目次へ
引き合っているの?」


”電荷の偏り”による電気的な引き合いと言われているよ。
量子力学的に言えば、電子の動きで磁場が発生しているとも言えるけど、
化学や生化学では”電荷の偏りによる静電気的相互作用”として処理するよ。
ただし、全ての現象は100%解明されているわけではない。現在使われている知識が絶対に正しいとは思わないようにしたほうがいいね。全てはグレーなんだ。」


約1.4という電気陰性度の差がある。
この差によって共有結合の電子が酸素側に引き寄せられ、
分子内にプラス寄りとマイナス寄りの部分が生まれる。
この状態が『極性』だね」


「うん。
そのように同じ分子内でプラスとマイナスが
離れて存在している物理的な状態を
『電気双極子』と呼んで区別するんだよ」
水中に存在するんだね💦」


水分子同士が近づいた場合、何がおこると思う?
水分子のプラス(H側)と
別の水分子のマイナス(O側)が引き付け合うんだ。
これが水素結合の正体だよ」
くっついているってこと?」


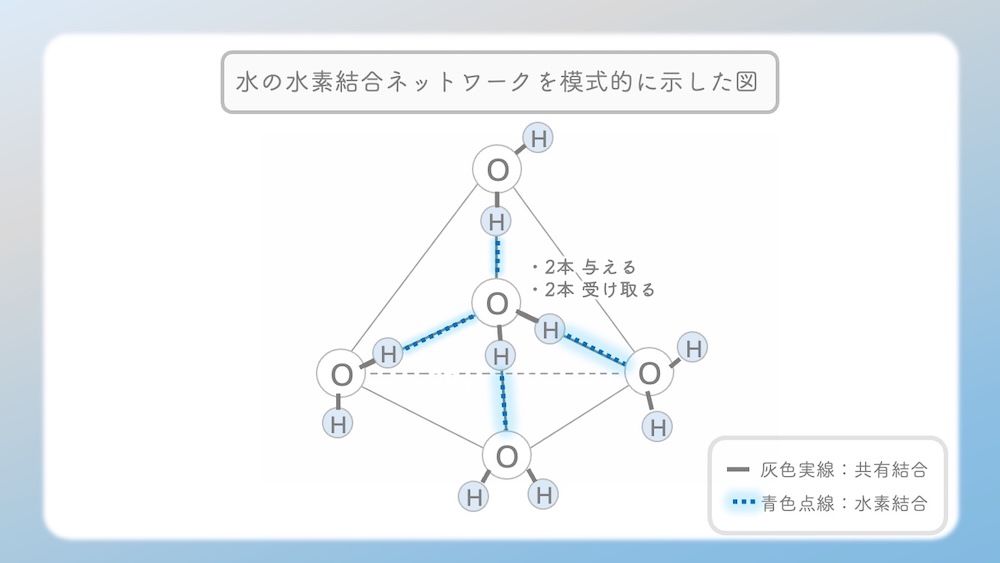
水の中では、この水素結合で
水分子同士がスクラムを組むように
存在しているんだよ」
一部ほどいてまで、特定のアミノ酸に近寄っていくということは、相手にも、それなりに強く引き寄せる
『魅力』があるってことなんだね」

【まとめ】水分子の結合と「魅力」の法則
● 極性と電気双極子
原子間の電気陰性度の差によって電荷が偏ることを「極性」といい、その結果として分子内にプラスとマイナスの極が生じている物理的な状態を「電気双極子」と呼びます。
● 水素結合の仕組み
水分子同士を引き寄せているのは磁力ではなく、電気双極子間の電気的な引き合い(静電気的相互作用)です。一方の分子の水素側(δ+)と、他方の酸素側(δ-)が相互作用することで水素結合が形成されます。
● スクラムと溶解性
水分子は水素結合によって互いに「スクラム」を組むように安定しています。特定のアミノ酸がこのスクラムに加わる(=水に溶ける)ためには、水分子同士の引き合いに割り込めるだけの強い「電気的な魅力」がアミノ酸側にも必要になります。
● 相手が O-H や N-H の場合
電荷の偏りがはっきりしている部分があると、水分子はそこに引き寄せられます。
水分子の少しプラスの部分は、相手のマイナス寄りの部分へ。
水分子の少しマイナスの部分は、相手のプラス寄りの部分へ。
このように、水分子と強く引き合える部分を持つアミノ酸は、水の中に受け入れられやすくなります。
これが親水性です。
● 相手が C-H(炭化水素)の場合
電荷の偏りがほとんどない部分は、水分子を強く引き寄せることができません。
水分子にとっては、わざわざ自分たちの水素結合のネットワークをほどいてまで近づく理由が少ないのです。
そのため水分子は、その部分とはあまり相互作用せず、水分子同士でつながり続けようとします。
これが疎水性です。
目安となる「0.5」の境界線
| 電気陰性度の差 | 結合の分類 | 水との関係 |
|---|---|---|
| 0.0 〜 0.4 | 非極性共有結合 | 疎水性 |
| 0.5 〜 1.7 | 極性共有結合 | 親水性 |
| 1.7 〜 | イオン結合 | 完全に電荷を持つ |
※数値は諸説ありますが、アミノ酸の骨格を作る C-H の「0.4」は、ギリギリ水に無視されるという絶妙な数値なのです。


まとめ:水分子のスクラムに「割り込めるか」
▲目次へ
アミノ酸を分類する際、大事なのは「わずかでも差があるかどうか」ではありません。バリンのように側鎖が「0.4の差」しかない C-H ばかりのアミノ酸が疎水性なのは、水分子にとって彼らが「あまりに電荷の偏りが無く、引きつける力に欠けるから」なのです。
ミクロの綱引きが生命を形作る
アミノ酸が水に溶けるか、溶けないか。
その小さな違いがタンパク質の複雑な折りたたみを決め、私たちの筋肉や酵素を作り上げています。
すべては、原子たちの「電子の奪い合い」から始まっているのです。
🐾 Dr.シロネコの応援メモ
使い終わった教科書📚はどうしていますか?医学書は価値が高いうちに整理するのが賢い方法です。次のステップへ進むための軍資金にするのも手ですよ。👍
第三章 実力診断!国家試験・CBTレベル突破テスト
クイズを解いて、アウトプットする習慣をつけよう。
【実力判定】アミノ酸と電気陰性度の攻略クイズ(全10問)
▲目次へ
✅ 正解を確認する
正解:C) 側鎖(R基)
全てのアミノ酸で共通している部分(アミノ基・カルボキシ基)はもともと親水性です。アミノ酸ごとの個性を決めているのは、種類によって異なる「側鎖」の部分です。
✅ 正解を確認する
正解:B) 電子
原子が共有結合をしている相手から、どれくらい自分の方へ「電子」を引き寄せるかを表した数値です。
✅ 正解を確認する
正解:D) 右上
周期表の右上にある原子(酸素など)は、原子核が電子を引っ張る力が強く、電気陰性度が大きくなります。
✅ 正解を確認する
正解:A) O > N > C
酸素(3.5)> 窒素(3.0)> 炭素(2.5)の順です。「最強のFON(フォン)」と覚えましょう。
✅ 正解を確認する
正解:B) 酸素原子(O)
酸素(3.5)は水素(2.1)より電子を引く力が強いため、電子が酸素側に偏り、酸素がマイナスの電気を帯びます。
✅ 正解を確認する
正解:C) 0.5以上
差が0.5以上あると、水分子が引き寄せられるほどの明確な極性が生まれます。
✅ 正解を確認する
正解:A) 非極性共有結合
0.4の差は「誤差」の範囲とみなされ、電気的な偏りがほとんどない「非極性」に分類されます。
✅ 正解を確認する
正解:C) 水分子がアミノ酸の周りを磁石のように囲むこと
これを「水和」と呼びます。水分子はアミノ酸を壊すのではなく、包囲してエスコートすることで水中に分散させます。
✅ 正解を確認する
正解:B) 水分子を惹きつける「目印(極性)」が弱すぎるから
C-H結合の差は0.4であり、水分子のスクラムに割り込めるほどの魅力(極性)がないため、無視されてしまいます。
✅ 正解を確認する
正解:A) OとHの電気陰性度の差が1.4と大きいから
1.4という大きな差があるため、水分子が引き寄せられます。
【実力診断:応用編】臨床に繋がる重要ポイント
▲目次へ
✅ 正解を確認する
正解:B) タンパク質の内部(水から隠れる側)
水分子に無視される(疎水性)アミノ酸同士は、水から逃げるように内側に集まります。これを「疎水性相互作用」と呼び、タンパク質が正しい形を作る原動力になります。
✅ 正解を確認する
正解:B) C-H結合が多く、極性がほとんどない物質
細胞膜の内部は「油(脂質)」の性質を持っています。バリンのように極性がない(疎水性)物質は、油に溶け込みやすいため、膜を通り抜けやすくなります。
電気陰性度の差によって生じた「プラス(H)」と「マイナス(OやN)」が引き合う力を水素結合と呼びます。これがアミノ酸の「水への溶けやすさ」を支配しています。
10. 参考文献
▲目次へ
1. Lehninger Principles of Biochemistry(生化学のバイブル)
Nelson DL, Cox MM. Lehninger principles of biochemistry. 8th ed. New York: W. H. Freeman; 2021.
日本語:レーニンジャーの新生化学(上・下) 第7版(監訳:中山 和久)
発行年: 2019年(第7版)
※英語版は2021年に第8版が出ていますが、日本語版は現在この第7版が最新です
今日のブログ記事に関する特徴:
酸素(O)や窒素(N)が電子を強く惹きつけることで生じる電荷の偏りが、
タンパク質の立体構造(水素結合や疎水性相互作用)を形作る根本的な力であることを、
生化学の土台として詳細に解説しています。
2. Harper’s Illustrated Biochemistry(図解が豊富な医歯薬学生向けの名著)
Kennelly PJ, Botham KM, McGuinness OP, Rodwell VW, Weil PA. Harper’s illustrated biochemistry. 32nd ed. New York: McGraw Hill; 2022.
日本語:ハーパー・生化学 原書30版(監訳:清水 孝雄)
発行年: 2016年(原書30版)
※最新の英語版に対応する日本語版は準備中ですが、学習のスタンダードとして広く使われています
今日のブログ記事に関する特徴:
電荷の偏りによる「極性」が、水に対する溶けやすさや生体膜の透過性に
どう影響するかなど、生体内の現象と関連付けた図解が豊富です。
臨床に向けた実践的な理解を助けてくれます。
3. Atkins’ Physical Chemistry(電気陰性度の物理的背景を知るための名著)
Atkins P, de Paula J, Keeler J. Atkins’ physical chemistry. 12th ed. Oxford: Oxford University Press; 2022.
日本語:アトキンス 物理化学(上・下) 第10版(訳:中野 幸夫 他)
発行年: 2017年(第10版)
今日のブログ記事に関する特徴:
原子が共有結合の電子を引き寄せる強さである「電気陰性度」の数値的な定義や、
分子内にプラスとマイナスの電荷をあわせ持つ「電気双極子」の物理的性質を、
最も深く掘り下げて解説しています。





